
|
|
Appunti delle lezioni, cheat sheet
Terapia ospedaliera. Cheat sheet: in breve, il più importante
Elenco / Appunti delle lezioni, cheat sheet Sommario
1. Reumatismi. Eziologia e patogenesi Il reumatismo (malattia di Sokolsky-Buyo) è una malattia infiammatoria sistemica del tessuto connettivo con una localizzazione predominante del processo nel sistema cardiovascolare, che si sviluppa in persone predisposte ad esso (di norma, si tratta di giovani) a causa di un'infezione acuta con streptococco di gruppo b-emolitico MA. Questa definizione della malattia è stata data nel 1989 da V. A. Nasonov. La sconfitta di altri organi e sistemi nei reumatismi è di secondaria importanza e non ne determina la gravità e la successiva prognosi. Eziologia. Gli streptococchi beta-emolitici di gruppo A causano infezioni delle vie respiratorie superiori. Ecco perché l'insorgenza dei reumatismi, di regola, è preceduta da angina, esacerbazione della tonsillite cronica e nel sangue dei pazienti, una maggiore quantità di antigene streptococcico e anticorpi anti-streptococco (ASL-O, ASG, ASA, antideossiribonucleasi B (anti-DNasi B)) vengono rilevati. Nello sviluppo dei reumatismi giocano un ruolo l'età e i fattori sociali (condizioni di vita sfavorevoli, malnutrizione), conta anche una predisposizione genetica (i reumatismi sono una malattia a trasmissione poligenica, è ben nota l'esistenza di famiglie “reumatiche”) che consiste in una risposta iperimmune agli antigeni dello streptococco, propensione dei pazienti a processi autoimmuni e immunocomplessi. Patogenesi. Nei reumatismi si verifica una risposta immunitaria complessa e diversificata (reazioni di ipersensibilità di tipo immediato e ritardato) a numerosi antigeni streptococcici. Quando un'infezione entra nel corpo, vengono prodotti anticorpi antistreptococcici e si formano immunocomplessi (antigeni dello streptococco + anticorpi contro di essi + complemento), che circolano nel sangue e si depositano nel letto microcircolatorio. Le tossine e gli enzimi dello streptococco hanno anche un effetto dannoso sul miocardio e sul tessuto connettivo. A causa di un difetto geneticamente determinato nel sistema immunitario, gli antigeni streptococcici e gli immunocomplessi non vengono eliminati completamente e rapidamente dal corpo dei pazienti. Di conseguenza, i processi autoimmuni si sviluppano in base al tipo di ipersensibilità di tipo ritardato e nel sangue dei pazienti si trovano linfociti che reagiscono con il tessuto cardiaco. Queste cellule sono di grande importanza nell'origine delle lesioni d'organo (principalmente il cuore). Nel tessuto connettivo con reumatismi si verificano cambiamenti di fase: gonfiore mucoide - alterazioni fibrinoidi - necrosi fibrinoide. L'espressione morfologica dei disturbi immunitari sono reazioni cellulari: infiltrazione di linfociti e plasmociti, formazione di granulomi reumatici o Ashofftalalaevskaya. Il processo patologico termina con la sclerosi. Quando il cuore è danneggiato, il processo infiammatorio può diffondersi a tutte le membrane del cuore (pancardite) o in isolamento a ciascuna delle membrane. 2. Quadro clinico dei reumatismi Tutte le manifestazioni della malattia possono essere suddivise in cardiache ed extracardiache. È possibile descrivere il quadro clinico della malattia da queste posizioni. Stadio I: viene rivelata la connessione della malattia con l'infezione trasferita. In casi tipici, 1-2 settimane dopo un mal di gola o una malattia respiratoria acuta, la temperatura corporea aumenta, a volte fino a 38-4 °C, con fluttuazioni durante il giorno entro 1-2 °C e forte sudorazione (di solito senza brividi). La manifestazione più comune di reumatismi è il danno cardiaco - cardiopatia reumatica: danno simultaneo al miocardio e all'endocardio. I pazienti lamentano un lieve dolore o disagio nella regione del cuore, una leggera mancanza di respiro durante l'esercizio, interruzioni o palpitazioni sono molto meno comuni. La reumocardite nei giovani pazienti, di regola, è grave: fin dall'inizio della malattia, si notano grave mancanza di respiro durante l'esercizio ea riposo, dolore costante al cuore e palpitazioni. La pericardite, così come le manifestazioni extracardiache dei reumatismi, sono rare. Con lo sviluppo della pericardite secca, i pazienti notano solo un dolore costante nella regione del cuore. Con la pericardite essudativa, caratterizzata dall'accumulo di essudato sieroso-fibrinoso nel sacco cardiaco, il dolore scompare, poiché gli strati pericardici infiammati vengono separati dall'essudato accumulato. La più caratteristica dei reumatismi è la sconfitta del sistema muscolo-scheletrico sotto forma di poliartrite reumatica. Anche le lesioni reumatiche dei reni sono estremamente rare, rilevate solo nello studio delle urine. La sindrome addominale (peritonite) si verifica quasi esclusivamente nei bambini e negli adolescenti con reumatismi primari acuti. Nella fase II della ricerca diagnostica, l'individuazione dei segni di danno cardiaco ha poca importanza. Nella cardiopatia reumatica primaria, il cuore di solito non è ingrandito. L'auscultazione rivela un tono I smorzato, a volte l'aspetto di un tono III, un lieve soffio sistolico all'apice. Questa sintomatologia è dovuta a cambiamenti nel miocardio. In caso di danno alla valvola aortica si può udire un soffio protodiastolico al punto di Botkin e si può preservare la sonorità del II tono. Nei pazienti con poliartrite, si nota una deformità articolare a causa dell'infiammazione della membrana sinoviale e dei tessuti periarticolari, dolore alla palpazione dell'articolazione. L'eritema anulare (segno quasi patognomonico dei reumatismi) è estremamente raro (nell'1-2% dei pazienti). Nella III fase della ricerca diagnostica, i dati degli studi di laboratorio e strumentali consentono di stabilire l'attività del processo patologico e chiarire il danno al cuore e ad altri organi. Indicatori di fase acuta: neutrofilia con spostamento a sinistra del conteggio dei leucociti; un aumento del contenuto di 2-globuline, seguito da un aumento del livello di globuline; aumento del contenuto di fibrinogeno; la comparsa della proteina C-reattiva; La VES aumenta. Parametri immunologici, aumento dei titoli degli anticorpi antistreptococcici (antiialuronidasi e antistreptochinasi più di 1:300, anti-O-streptolisina più di 1:250). 3. Diagnosi di reumatismi Con il progressivo esordio dei reumatismi, la diagnosi sindromica proposta da AI Nesterov nel 1973 (vedi tabella 1) conta: sindrome clinica ed epidemiologica; sindrome cardiovascolare (vedi tabella 2). Tabella 1
Tabella 2
4. Diagnosi differenziale dei reumatismi La poliartrite reumatica deve essere differenziata da quelle non reumatiche (vedi tabella). tavolo
5. Trattamento dei reumatismi L'intero complesso del trattamento dei reumatismi consiste nella terapia antimicrobica e antinfiammatoria, misure volte a ripristinare l'omeostasi immunologica. Si raccomanda di utilizzare una dieta equilibrata razionale, concentrarsi sull'adattamento all'attività fisica, sulla preparazione al lavoro, sul trattamento chirurgico tempestivo di pazienti con difetti cardiaci complessi. A tutti i pazienti durante la fase attiva dei reumatismi viene mostrata la penicillina (1-200 UI per 000 dosi al giorno, ogni 1 ore), che ha un effetto battericida su tutti i tipi di streptococco A. Il corso del trattamento è di 500 settimane durante la fase attiva dei reumatismi, in futuro è necessario un trasferimento al farmaco prolungato bicillina-000 (6 unità). Con l'intolleranza alla penicillina, può essere prescritta l'eritromicina 4 mg 2 volte al giorno. I farmaci con effetto antinfiammatorio, che vengono utilizzati nel moderno trattamento della fase attiva dei reumatismi, sono glucocorticosteroidi, salicilici, derivati dell'indolo, derivati dell'acido fenilacetico, ecc. Il prednisolone viene utilizzato a 20-30 mg al giorno (per 2 settimane, quindi la dose viene ridotta di 2,5-5 mg ogni 5-7 giorni, in totale per un ciclo di 1,5-2 mesi) per primari e ricorrenti con III e II attività di grado del processo di cardiopatia reumatica, con poliserosite e corea, con lo sviluppo di insufficienza cardiaca dovuta a cardite attiva. Gli agenti corticosteroidi influenzano il metabolismo del sale idrico, pertanto nel trattamento devono essere utilizzati cloruro di potassio 3-4 g / die, panangina e altri, con ritenzione di liquidi - antagonisti dell'aldosterone (veroshpiron fino a 6-8 compresse al giorno), diuretici (lasix 40 -80 mg / die, furosemide 40-80 mg / die, ecc.), con euforia - tranquillanti, ecc. Anche i farmaci antinfiammatori non steroidei sono ampiamente utilizzati per i reumatismi: le dosi medie di acido acetilsalicilico sono 3-4 g al giorno, meno spesso 5 g al giorno o più. L'acido acetilsalicilico viene utilizzato 1 g 3-4 volte al giorno dopo i pasti per 1-3 mesi o più con tolleranza normale e soggetto a controllo degli effetti collaterali. L'uso di successo del derivato dell'acido indolacetico - indometacina nei reumatismi da oltre 20 anni. Ha un pronunciato effetto terapeutico: i sintomi soggettivi della cardite (cardialgia, palpitazioni, mancanza di respiro) scompaiono entro l'8-10° giorno di terapia e i segni oggettivi - entro il 14-16° giorno. La scomparsa della poliartrite e della poliserosite avviene ancora più velocemente. Nel trattamento dei reumatismi è importante la combinazione di tre fasi principali: ospedale - clinica - resort. Nella fase I, il trattamento viene effettuato con i farmaci sopra elencati. Dopo aver ridotto l'attività dei reumatismi e la normalizzazione delle condizioni del paziente, vengono trasferiti allo stadio II - trattamento in un sanatorio reumatologico. L'obiettivo principale di questa fase è continuare il trattamento con farmaci antinfiammatori non steroidei. La fase III include l'osservazione del dispensario e il trattamento preventivo. 6. Classificazione delle cardiomiopatie. Eziologia della cardiomiopatia dilatativa (DCM) Le cardiomiopatie sono lesioni miocardiche primarie isolate di natura non infiammatoria ad eziologia sconosciuta (idiopatica), non sono associate a difetti valvolari o shunt intracardiaci, ipertensione arteriosa o polmonare, malattia coronarica o malattie sistemiche (come collagenosi, amiloidosi, emocromatosi, ecc.), inoltre, nella fase finale della malattia si sviluppano grave insufficienza cardiaca congestizia e complesse violazioni del ritmo cardiaco e della pervietà. La classificazione delle cardiomiopatie è la seguente: 1) cardiomiopatia dilatativa: a) idiopatico; b) tossico; c) infettivo; d) con collagenosi; 2) ipertrofico; 3) restrittivo; 4) displasia aritmica del ventricolo destro; 5) una combinazione di uno dei 4 tipi di cardiomiopatie con ipertensione arteriosa. La cardiomiopatia dilatativa (DCM) è una malattia del muscolo cardiaco caratterizzata da un'espansione diffusa di tutte le camere del cuore (principalmente il ventricolo sinistro), in cui è in primo piano la patologia della funzione di pompaggio del cuore e, di conseguenza , insufficienza cardiaca cronica (da cui il secondo nome è congestizia, quando il cuore non è in grado di pompare completamente il sangue e "ristagna" nei tessuti e negli organi del corpo). La parete muscolare del cuore rimane invariata o ipertrofica in varia misura. Le malattie ei fattori che hanno preceduto lo sviluppo del DCMP sono descritti nella tabella seguente (vedi tabella). Tavolo. Malattie e fattori che hanno preceduto lo sviluppo del DCM
Questa è la forma più comune di danno al muscolo cardiaco. L'incidenza è di 5-8 casi ogni 100 persone all'anno. Non esiste una chiara storia familiare per questi pazienti. Gli uomini si ammalano 000-2 volte più spesso delle donne. 7. Patogenesi della cardiomiopatia dilatativa (DCM) Patogenesi. Come risultato del processo infiammatorio nel muscolo cardiaco (miocardite), le singole cellule muoiono nelle sue varie parti. L'infiammazione in questo caso è di natura virale e le cellule colpite dal virus diventano agenti estranei per il corpo. Di conseguenza, quando gli antigeni compaiono nel corpo, si sviluppa un complesso di reazioni di risposta immunitaria, volte alla loro distruzione. A poco a poco, le cellule muscolari morte vengono sostituite dal tessuto connettivo, che non ha la capacità di estensibilità e contrattilità inerente al miocardio. A causa della perdita delle funzioni miocardiche di base, il cuore perde la sua capacità di funzionare come pompa. In risposta a ciò (come reazione compensatoria), le camere del cuore si espandono (cioè si dilatano) e si verifica ispessimento e ispessimento nella parte rimanente del miocardio (cioè si sviluppa la sua ipertrofia). Per aumentare l'apporto di ossigeno agli organi e ai tessuti del corpo, si verifica un aumento persistente della frequenza cardiaca (tachicardia sinusale). Questa risposta compensatoria migliora solo temporaneamente la funzione di pompaggio del cuore. Tuttavia, le possibilità di dilatazione e ipertrofia del miocardio sono limitate dalla quantità di miocardio vitale e sono individuali per ogni caso specifico della malattia. Con il passaggio del processo allo stadio di scompenso, si sviluppa insufficienza cardiaca cronica. Tuttavia, in questa fase, entra in gioco un altro meccanismo compensatorio: i tessuti del corpo aumentano l'estrazione di ossigeno dal sangue rispetto a un corpo sano. Ma questo meccanismo è insufficiente, poiché una diminuzione della funzione di pompaggio del cuore porta a una diminuzione dell'apporto di ossigeno a organi e tessuti, necessario per il loro normale funzionamento, mentre aumenta la quantità di anidride carbonica in essi contenuta. In 2/3 dei pazienti nelle cavità dei ventricoli nelle ultime fasi della malattia si formano trombi parietali (a causa di una diminuzione della funzione di pompaggio del cuore, nonché della contrazione irregolare del miocardio nelle camere del cuore), seguito dallo sviluppo di embolia nella circolazione polmonare o sistemica. Alterazioni patologiche e patomorfologiche del cuore. La forma del cuore diventa sferica, la sua massa aumenta da 500 a 1000 g, principalmente a causa del ventricolo sinistro. Il miocardio diventa flaccido, opaco, con evidenti strati biancastri di tessuto connettivo, c'è una caratteristica alternanza di cardiomiociti ipertrofici e atrofici. Al microscopio viene rilevata la fibrosi diffusa, può essere combinata sia con l'atrofia che con l'ipertrofia dei cardiomiociti, in cui vi è un aumento significativo del volume dei nuclei, il numero di mitocondri, l'iperplasia dell'apparato del Golgi, un aumento del numero di miofibrille , libero e associato ai ribosomi del reticolo endoplasmatico, un'abbondanza di granuli di glicogeno. 8. Quadro clinico e diagnosi della cardiomiopatia dilatativa (DCM) Non ci sono segni specifici della malattia. Il quadro clinico è polimorfico ed è determinato da: 1) sintomi di insufficienza cardiaca; 2) disturbi del ritmo e della conduzione; 3) sindrome tromboembolica. Nella maggior parte dei casi, la prognosi della malattia è determinata dalla sconfitta del ventricolo sinistro del cuore. Prima dell'inizio dell'insufficienza cardiaca, il DCM è latente. Le lamentele più frequenti di insufficienza cardiaca già insorta sono lamentele relative a prestazioni ridotte, maggiore affaticamento, mancanza di respiro durante lo sforzo e quindi a riposo. Di notte, ha una tosse secca (l'equivalente dell'asma cardiaco), in seguito - tipici attacchi di asma. I pazienti presentano dolore anginoso caratteristico. Con lo sviluppo della congestione nella circolazione sistemica, appare pesantezza nell'ipocondrio destro (a causa di un ingrossamento del fegato), gonfiore delle gambe. Diagnostica. Quando si diagnostica la malattia, un segno importante è un aumento significativo del cuore (non ci sono segni di cardiopatia valvolare o ipertensione arteriosa). La cardiomegalia si manifesta con l'espansione del cuore in entrambe le direzioni, determinata dalla percussione, così come lo spostamento del battito apicale a sinistra e in basso. Nei casi più gravi si sente un ritmo di galoppo, tachicardia, mormorii di relativa insufficienza delle valvole mitrale o tricuspide. Nel 20% dei casi si sviluppa fibrillazione atriale. La pressione sanguigna è generalmente normale o leggermente elevata (a causa di insufficienza cardiaca). Gli studi biochimici del sangue e delle urine possono rilevare varie sostanze tossiche e carenze vitaminiche. I metodi di ricerca strumentale consentono di rilevare: 1) segni di cardiomegalia; 2) cambiamenti in indicatori di dinamica haemo centrale; 3) disturbi del ritmo e della conduzione. Il fonocardiogramma conferma i dati auscultatori sotto forma di un ritmo di galoppo, una rilevazione abbastanza comune del soffio sistolico. I raggi X hanno rivelato un aumento significativo dei ventricoli e un ristagno di sangue nella (piccola) circolazione polmonare. L'ecocardiografia aiuta a rilevare la dilatazione di entrambi i ventricoli, l'ipocinesia della parete posteriore del ventricolo sinistro, il movimento paradosso del setto interventricolare durante la sistole. Viene eseguito uno studio radioisotopico del cuore (scintigrafia miocardica) per chiarire lo stato della funzione di pompaggio del cuore e per determinare le zone del miocardio morto. Angiocardiograficamente, vengono rilevati gli stessi cambiamenti dell'ecocardiogramma. La biopsia miocardica viva non è informativa per determinare l'eziologia della cardiomiopatia. In alcuni casi, la biopsia può rilevare un antigene virale o un aumento del contenuto di LDH, nonché un deterioramento della produzione di energia da parte dei mitocondri. 9. Differenziale/diagnosi della cardiomiopatia dilatativa (DCM) Si produce principalmente con miocardite e distrofie miocardiche, cioè con quelle condizioni che a volte vengono irragionevolmente chiamate cardiomiopatie secondarie. La biopsia miocardica fornisce un aiuto significativo nella diagnosi differenziale della cardiomiopatia dilatativa e delle malattie cardiache, che si verificano con un pronunciato aumento di essa: 1) con miocardite diffusa grave, l'infiltrazione cellulare dello stroma si trova in combinazione con alterazioni distrofiche e necrotiche nei cardiomiociti; 2) con amiloidosi primaria che si manifesta con danno cardiaco (la cosiddetta variante cardiopatica dell'amiloidosi primaria), vi è una significativa deposizione di amiloide nel tessuto interstiziale del miocardio, combinata con l'atrofia delle fibre muscolari; 3) con emocromatosi (una malattia causata da una violazione del metabolismo del ferro), nel miocardio si trovano depositi di pigmento contenente ferro, vari gradi di distrofia e atrofia delle fibre muscolari e si osservano la proliferazione del tessuto connettivo. Come variante del DCM, possono essere considerate cardiomiopatie indotte da farmaci e tossiche. Numerosi agenti possono causare danni tossici al miocardio: etanolo, emetina, litio, cadmio, cobalto, arsenico, isproterenolo e altri veleni. I cambiamenti patoistologici nei tessuti del muscolo cardiaco si manifestano sotto forma di distrofie focali. L'esempio più eclatante di cardiomiopatia tossica è la cardiomiopatia che si verifica nelle persone che bevono quantità eccessive di birra. Nella fase acuta della cardiomiopatia da cobalto si nota la presenza di degenerazione idropica e grassa, distruzione di organelli intracellulari e necrosi focale dei cardiomiociti. Cardiomiopatia alcolica. L'etanolo ha un effetto tossico diretto sui cardiomiociti. Macroscopicamente, il miocardio è flaccido, simile all'argilla, a volte si osservano piccole cicatrici. Le arterie coronarie sono intatte. L'esame microscopico mostra una combinazione di distrofia (idropica e grassa), atrofia e ipertrofia dei cardiomiociti, forse la presenza di focolai di lisi e sclerosi dei cardiomiociti. Le aree interessate del miocardio contrastano con quelle invariate. L'esame al microscopio elettronico di campioni di biopsia cardiaca mostra l'espansione cistica del reticolo sarcoplasmatico e del sistema T dei cardiomiociti, caratteristica della cardiomiopatia alcolica. Complicazioni della cardiomiopatia alcolica - morte improvvisa a causa di fibrillazione ventricolare o insufficienza cardiaca cronica, sindrome tromboembolica. 10. Trattamento e prevenzione della cardiomiopatia dilatativa (DCM) I principi generali per il trattamento della DCM non differiscono significativamente dal trattamento dell'insufficienza cardiaca cronica. Nei casi di DCM secondaria, viene inoltre effettuato il trattamento della precedente malattia (cardiopatia valvolare, ecc.) E vengono prese tutte le misure per eliminare le cause della DCM. I vasodilatatori periferici sono abbastanza efficaci, specialmente con la concomitante sindrome anginosa (nitrong, sustak, nitrosorbide). Con la sindrome anginosa, diventa necessario utilizzare farmaci antianginosi, preferibilmente nitrati prolungati (sustak, nitrong, nitrosorbide). Gli adrenobloccanti sono efficaci (sono prescritti in assenza di segni di insufficienza cardiaca). Tra i moderni metodi di trattamento chirurgico del DCM, il più efficace è il trapianto di cuore (trapianto). Tuttavia, le possibilità di effettuare questa operazione sono notevolmente limitate. Per questo, in alternativa al trapianto cardiaco nelle moderne cure, per aumentare l'aspettativa di vita dei pazienti affetti da DCMP, sono stati sviluppati e sono in corso interventi di chirurgia ricostruttiva, volti ad eliminare l'insufficienza delle valvole cardiache mitralica e tricuspide. Un'alternativa al trapianto cardiaco nei pazienti con DCM è l'asportazione parziale del ventricolo sinistro al fine di ridurne le dimensioni (intervento di Battista). Non molto tempo fa, per il trattamento dei pazienti con DCMP, sono stati sviluppati modelli speciali di pacemaker che consentono di rendere sincrono il lavoro dei ventricoli del cuore. Ciò porta a un miglioramento del riempimento dei ventricoli del cuore con il sangue e un aumento della funzione di pompaggio del cuore. La DCM nei bambini è di 5-10 casi ogni 100 bambini all'anno. L'effetto maggiore nel trattamento della cardiomiopatia dilatativa nei bambini piccoli si ottiene con una combinazione di corticosteroidi e glicosidi (prednisolone e digossina). Sullo sfondo della monoterapia con prednisolone, si verifica una diminuzione della frequenza cardiaca. La monoterapia con digossina porta ad una diminuzione della tachicardia e della dispnea. Data l'impossibilità di prescrivere farmaci citostatici nei bambini piccoli, poiché è stato osservato un numero significativo di complicanze terapeutiche, è più ottimale in pediatria utilizzare glicosidi cardiaci a lunga durata d'azione in combinazione con ormoni corticosteroidi per la cardiomiopatia dilatativa. Prevenzione. La prevenzione del DCMP consiste nell'esclusione di alcol, cocaina e un attento monitoraggio delle prestazioni cardiache durante la chemioterapia del tumore. È utile per indurire il corpo fin dalla tenera età. L'astinenza completa dall'alcol nel DCM alcolico migliora la contrattilità cardiaca e può eliminare la necessità di un trapianto di cuore. 11. Classificazione delle cardiomiopatie. Eziologia della cardiomiopatia ipertrofica (HCM) La cardiomiopatia ipertrofica (HCM) è una malattia non coronarica del miocardio ventricolare (principalmente il sinistro), caratterizzata da una massiccia ipertrofia delle loro pareti con protrusione del setto interventricolare (IVS) nella cavità del ventricolo destro, che può essere notevolmente ispessita , una diminuzione del volume interno dei ventricoli, una contrattilità normale o aumentata del miocardio ventricolare e un rilassamento alterato (disfunzione diastolica). La più comune è l'ipertrofia isolata del setto interventricolare (stenosi subaortica ipertrofica isolata - IHSS) o della parte apicale dei ventricoli. Classificazione. Classificazione dell'HCM per localizzazione dell'ipertrofia (ED Wigle et al., 1985 con aggiunte). I. Ipertrofia ventricolare sinistra. 1. Ipertrofia asimmetrica, in cui si verifica ipertrofia miocardica delle singole pareti o segmenti dei ventricoli (inclusa ipertrofia IVS - 90% con o senza ostruzione del tratto di efflusso del ventricolo sinistro, ipertrofia medioventricolare - 1%, ipertrofia ventricolare apicale sinistra - 3%, parete libera ipertrofia ventricolo sinistro e parte posteriore dell'IVS - 1%). 2. L'ipertrofia simmetrica (concentrica) del ventricolo sinistro, quando l'ipertrofia miocardica si estende a tutte le pareti dei ventricoli, si verifica nel 5% dei casi. II. Ipertrofia del pancreas. Nel caso in cui l'ipertrofia miocardica impedisca il normale deflusso di sangue dai ventricoli del cuore, si parla di una forma ostruttiva di HCM. In altri casi, l'HCM non è ostruttivo. Eziologia. La malattia può essere sia congenita che acquisita. L'HCM congenita è ereditata in maniera autosomica dominante. All'interno della stessa famiglia si possono osservare varie forme e varianti di HCM. Molto spesso, viene ereditata l'ipertrofia asimmetrica del setto interventricolare. La forma acquisita di HCM si verifica nei pazienti anziani con una storia di ipertensione arteriosa. La prevalenza è 0,02-0,05%. Le ragioni per lo sviluppo dell'HCM acquisito non sono completamente comprese. Secondo una delle ipotesi proposte, gli individui con HCM acquisita nel periodo prenatale sviluppano un difetto dei recettori adrenergici del cuore coinvolti nella regolazione dell'attività cardiaca, in particolare della frequenza cardiaca. Di conseguenza, la sensibilità alla noradrenalina e ormoni simili, che aumentano la frequenza cardiaca, aumenta in modo significativo, il che influisce sullo sviluppo dell'ipertrofia miocardica in essi e, infine, sull'HCM. quadro patologico. Disorientamento disorientato, irregolare e caotico di cardiomiociti e miofibrille nei cardiomiociti, la fibrosi miocardica è una violazione dell'architettura del muscolo cardiaco. 12. Quadro clinico e diagnosi della cardiomiopatia ipertrofica (HCM) quadro clinico. L'HCM è caratterizzata da un'estrema varietà di sintomi, che è la causa di una diagnosi errata. La presenza e la tempistica della comparsa dei disturbi nell'HCM sono determinati principalmente da 2 fattori: la forma dell'HCM e la localizzazione della lesione. La camera più potente del cuore è il ventricolo sinistro, quindi, con l'ipertrofia del miocardio delle sue pareti, i disturbi potrebbero non comparire per molto tempo. La sconfitta isolata del ventricolo destro di cuore si incontra estremamente di rado. Il quadro clinico dell'HCM è: 1) segni di ipertrofia miocardica ventricolare (principalmente a sinistra); 2) un segno di funzione ventricolare diastolica insufficiente; 3) segni variabili di ostruzione del tratto di efflusso del ventricolo sinistro. Diagnostica. Nel processo di ricerca diagnostica, il più significativo è il rilevamento di soffio sistolico, polso alterato e battito apicale spostato. Per la diagnosi di HCM, i dati dell'ecocardiografia sono della massima importanza, consentendo di chiarire le caratteristiche anatomiche della malattia, la gravità dell'ipertrofia miocardica, l'ostruzione del tratto di efflusso del ventricolo sinistro. Si rivelano i seguenti segni: ipertrofia asimmetrica dell'IVS, più pronunciata nel terzo superiore, sua ipocinesi; movimento sistolico del lembo anteriore della valvola mitrale nella direzione anteriore; contatto del lembo anteriore della valvola mitrale con l'IVS in diastole. Segni aspecifici sono: ipertrofia dell'atrio sinistro, ipertrofia della parete posteriore del ventricolo sinistro, diminuzione della velocità media della copertura diastolica del lembo anteriore della valvola mitrale. All'ECG, qualsiasi cambiamento specifico si trova solo con ipertrofia ventricolare sinistra sufficientemente sviluppata. La diagnostica a raggi X è importante solo nella fase avanzata della malattia, quando è possibile determinare un aumento del ventricolo sinistro e dell'atrio sinistro, un'espansione della parte discendente dell'aorta. Sul fonocardiogramma vengono conservate le ampiezze dei toni I e II, che è un segno differenziale di HCM dalla stenosi dell'orifizio aortico e viene rilevato anche un soffio sistolico di varia gravità. I metodi di ricerca invasivi (sondaggio delle parti sinistre del cuore, angiografia con contrasto) non sono attualmente obbligatori, poiché l'ecocardiografia fornisce informazioni abbastanza affidabili per fare una diagnosi. Il sondaggio cardiaco viene utilizzato sotto il controllo della televisione a raggi X. Tecnica di esecuzione del metodo: perforando una grande arteria in anestesia locale con l'ulteriore introduzione di un apposito catetere nella cavità cardiaca, si misura il gradiente di pressione (differenza) tra il ventricolo sinistro e l'aorta in partenza da esso. Normalmente, questo gradiente non dovrebbe essere. 13. Trattamento e prevenzione della cardiomiopatia ipertrofica (HCM) Trattamento. Il trattamento farmacologico dell'HCM si basa su farmaci che migliorano il riempimento sanguigno dei ventricoli del cuore durante la diastole. Questi farmaci sono un gruppo di b-bloccanti (anaprilina, atenololo, metoprololo e propranololo, 160-320 mg/die, ecc.) e un gruppo di calcio ionantagonisti (verapamil, ma con cautela). La novokinamide disopiramide riduce anche la frequenza cardiaca e ha un effetto antiaritmico. All'inizio del trattamento vengono utilizzate piccole dosi di questi farmaci, quindi si verifica un graduale aumento del dosaggio fino al massimo tollerato dal paziente. I β-bloccanti sono usati con cautela nel diabete mellito, nell'asma bronchiale e in alcune altre malattie. Quando si tratta con questi farmaci, è necessario il monitoraggio costante della pressione sanguigna e della frequenza cardiaca. Una diminuzione della pressione inferiore a 90/60 mm Hg è pericolosa. Arte. e frequenza cardiaca inferiore a 55 al minuto. Se un paziente presenta disturbi del ritmo pericolosi che non possono essere trattati con beta-bloccanti o antagonisti degli ioni calcio, nel trattamento di tali pazienti vengono utilizzati anche altri farmaci antiaritmici. La nomina di anticoagulanti è raccomandata per le aritmie parossistiche e la fibrillazione atriale, nonché in presenza di coaguli di sangue nelle camere cardiache (warfarin, ecc.). Durante il periodo di trattamento con questi farmaci, è necessario monitorare regolarmente una serie di indicatori del sistema di coagulazione del sangue. Con un sovradosaggio significativo di anticoagulanti, sono possibili emorragie esterne (nasale, uterina, ecc.) E interne (ematomi, ecc.). Il trattamento chirurgico viene eseguito nei pazienti con HCM ostruttiva quando il trattamento medico non è efficace o quando il gradiente tra il ventricolo sinistro e l'aorta è superiore a 30 mm Hg. Arte. (viene eseguita l'operazione di miotomia o miectomia - escissione o rimozione di una parte del miocardio ipertrofico del ventricolo sinistro). Vengono anche eseguite la sostituzione della valvola mitrale e l'ablazione IVS non chirurgica. Prevenzione. Tutti i pazienti con HCM, in particolare quelli con forma ostruttiva, sono controindicati negli sport in cui è possibile un aumento pronunciato dell'attività fisica in un breve periodo di tempo (atletica, calcio, hockey). La prevenzione della malattia consiste nella diagnosi precoce, che consente di iniziare il trattamento precoce della malattia e prevenire lo sviluppo di una grave ipertrofia miocardica. Un ecocardiogramma deve essere eseguito nei parenti genetici del paziente. Anche lo screening dell'ECG e dell'EchoCG, che vengono eseguiti durante la visita medica annuale, sono importanti per la diagnosi. Nei pazienti con HCM ostruttiva, deve essere eseguita la profilassi dell'endocardite infettiva (profilassi antibiotica, ecc.), poiché la presenza di ostruzione crea le condizioni per lo sviluppo di questa condizione pericolosa per la vita. 14. Cause di cardiomiopatia restrittiva (RCMP) Cardiomiopatia restrittiva (RCMP) - (dalla parola latina strictio - "restrizione") - un gruppo di malattie del miocardio e dell'endocardio, in cui, a causa di fibrosi pronunciata e perdita di elasticità dovuta a vari motivi, c'è un fisso limitazione del riempimento dei ventricoli in diastole. RCMP include: endocardite fibroplastica parietale di Lefler (trovata in paesi con clima temperato, descritta da W. Loffler et al., 1936) e fibrosi endomiocardica (trovata nei paesi dell'Africa tropicale, descritta da D. Bedford et E. Konstman). Cause dell'RCM. La RCM primaria è molto rara e l'unica causa provata della sua insorgenza è la cosiddetta sindrome ipereosinofila (malattia di Leffler, endocardite fibroplastica parietale di Leffler). Si verifica principalmente negli uomini di età compresa tra 30 e 40 anni. Con la sindrome ipereosinofila si verifica un'infiammazione dell'endocardio, che nel tempo culmina in una significativa compattazione dell'endocardio e nella sua ruvida adesione al miocardio adiacente, che porta ad una forte diminuzione dell'estensibilità del muscolo cardiaco. La sindrome di Lefler è anche caratterizzata da eosinofilia persistente per 6 mesi o più (1500 eosinofili per 1 mm3), danno agli organi interni (fegato, reni, polmoni, midollo osseo). Nella stragrande maggioranza dei casi, l'origine di RCMP è secondaria, per altri motivi, tra i quali i più comuni sono: 1) amiloidosi - una malattia associata a una violazione del metabolismo proteico nel corpo; contemporaneamente, nei tessuti dei vari organi, si forma una proteina anormale (amiloide) che si deposita in grandi quantità; quando il cuore è danneggiato, l'amiloide provoca una diminuzione della sua contrattilità ed estensibilità; 2) emocromatosi - una violazione del metabolismo del ferro nel corpo, accompagnata da un aumento del contenuto di ferro nel sangue, il suo eccesso si deposita in molti organi e tessuti, incluso il miocardio, causando così una diminuzione della sua estensibilità; 3) sarcoidosi - una malattia di eziologia sconosciuta, caratterizzata dalla formazione di ammassi cellulari (granulomi) in organi e tessuti; i polmoni, il fegato, i linfonodi e la milza sono più spesso colpiti; e lo sviluppo di granulomi nel miocardio porta a una diminuzione della sua estensibilità; 4) malattie dell'endocardio (fibrosi endocardica, fibroelastosi endocardica, ecc.), Quando c'è un significativo ispessimento e compattazione dell'endocardio, che porta anche a una forte limitazione dell'estensibilità del miocardio. La fibroelastosi dell'endocardio, in particolare, può verificarsi solo nei bambini; questa malattia non è compatibile con la vita a causa dello sviluppo precoce di una grave insufficienza cardiaca. 15. Quadro clinico e diagnosi di cardiomiopatia restrittiva (RCMP) quadro clinico. Le manifestazioni della malattia sono estremamente polimorfiche e sono determinate dai sintomi dei disturbi circolatori nel cerchio piccolo o grande (a seconda della lesione primaria del ventricolo destro o sinistro). I reclami possono essere assenti o possono essere dovuti a congestione nella circolazione polmonare o sistemica. I pazienti di solito si lamentano di mancanza di respiro, che compare per la prima volta durante l'esercizio, e con il progredire della malattia, si osserva mancanza di respiro a riposo. A causa di una diminuzione della funzione di pompaggio del cuore, il paziente lamenta affaticamento e scarsa tolleranza a qualsiasi carico. Nel tempo, si uniscono gonfiore delle gambe, ingrossamento del fegato e idropisia dell'addome. Periodicamente appare un battito cardiaco irregolare e, con lo sviluppo di blocchi persistenti, potrebbero verificarsi svenimenti. La prima fase dello sviluppo della malattia (necrotica) è caratterizzata dalla comparsa di febbre, perdita di peso, tosse, eruzioni cutanee e tachicardia. Diagnostica. Il riconoscimento di RCM è estremamente difficile. È possibile parlare con sicurezza di questa patologia solo dopo l'esclusione di un certo numero di malattie che si verificano in modo simile (come la miocardite idiopatica del tipo Abramov-Fiedler, la pericardite essudativa, la cardiopatia valvolare). Quando si esaminano i pazienti con RCMP, si riscontrano sintomi caratteristici dell'insufficienza cardiaca congestizia (edema, epatomegalia e ascite), nonché una pronunciata pulsazione delle vene del collo. Durante l'auscultazione, il rilevamento di un cuore ingrossato, un lieve soffio sistolico tardivo e un forte tono precoce III è di grande importanza. Uno studio ECG rivela una moderata ipertrofia del miocardio ventricolare, nonché vari disturbi del ritmo e della conduzione dell'impulso cardiaco, cambiamenti non specifici nell'onda T dell'ECG. L'ecocardiografia è uno dei metodi più informativi per diagnosticare la malattia; rivela un ispessimento dell'endocardio, un cambiamento nella natura del riempimento dei ventricoli del cuore, una diminuzione della funzione di pompaggio del cuore, il rapido movimento del lembo anteriore della valvola mitrale durante la diastole e il rapido movimento precoce della parete posteriore del ventricolo sinistro verso l'esterno. La risonanza magnetica consente di ottenere informazioni sull'anatomia del cuore, determinare inclusioni patologiche nel miocardio e misurare lo spessore dell'endocardio. Quando si esaminano i parametri dell'emodinamica centrale, viene determinata un'aumentata pressione di riempimento in entrambi i ventricoli e la pressione finale nella sinistra supera quella nel ventricolo destro. La ventricolografia rivela una maggiore contrazione del ventricolo sinistro, contorni lisci delle sue pareti, a volte con un difetto di riempimento all'apice (prova di obliterazione). Ci sono segni di insufficienza valvolare, in particolare la valvola mitrale o tricuspide. 16. Diagnosi differenziale, trattamento e prevenzione della cardiomiopatia restrittiva (RCMP) Diagnosi differenziale. Nella diagnosi differenziale dell'RCMP, è molto importante tenere conto della somiglianza della malattia nelle manifestazioni esterne con la pericardite costrittiva, ma il metodo di trattamento per queste malattie è diametralmente opposto. La biopsia dal vivo del miocardio e dell'endocardio viene solitamente utilizzata contemporaneamente al sondaggio cardiaco, che consente di avere maggiori informazioni per chiarire la natura della malattia e ulteriori trattamenti. In casi estremamente rari, quando i metodi diagnostici di cui sopra non consentono di distinguere l'RCMP dalla pericardite costrittiva, viene eseguita una revisione diretta del pericardio sul tavolo operatorio. Tutti i pazienti con RCMP necessitano di un esame clinico, biochimico e aggiuntivo completo per determinare le cause non cardiache della malattia. Trattamento. Il trattamento della malattia presenta notevoli difficoltà. La maggior parte dei farmaci utilizzati per curare l'insufficienza cardiaca potrebbe non portare i risultati sperati a causa del fatto che, a causa delle caratteristiche della malattia, è impossibile ottenere un miglioramento significativo della compliance miocardica (in alcuni casi vengono prescritti antagonisti degli ioni calcio per questo scopo). I diuretici (aldactone) sono usati per eliminare i liquidi in eccesso nel corpo. Per eliminare i disturbi persistenti della conduzione, potrebbe essere necessario installare (impiantare) un pacemaker permanente. Ciò è causato da malattie come la sarcoidosi e l'emocromatosi, che portano allo sviluppo di RCMP secondario, sono soggette ad autotrattamento. Nel trattamento della sarcoidosi vengono utilizzati farmaci ormonali (prednisolone, ecc.) E nell'emocromatosi, un regolare salasso (per ridurre la concentrazione di ferro nel corpo). Il trattamento dell'amiloidosi miocardica dipende direttamente dalle cause della sua insorgenza. Si consiglia di utilizzare farmaci anticoagulanti per la trombosi nelle camere del cuore. Si ricorre al trattamento chirurgico nei casi di RCMP causato da danno endocardico. Durante l'operazione, se possibile, viene asportata la parte dell'endocardio che ha subito modifiche. In alcuni casi, se c'è insufficienza delle valvole atrioventricolari, viene eseguita la loro protesi. Alcune forme di danno miocardico amiloide vengono trattate con un trapianto di cuore. Prevenzione della RCM. Sfortunatamente, le misure preventive per questa malattia sono limitate. Principalmente è necessaria la diagnosi precoce di cause potenzialmente rimovibili di amiloidosi, sarcoidosi, emocromatosi, ecc.. Per raggiungere questi obiettivi, è di grande importanza condurre una visita medica annuale della popolazione. 17. Eziologia dell'endocardite infettiva (IE) L'endocardite infettiva (IE) è una malattia consistente in lesioni poliposi-ulcerative dell'apparato valvolare del cuore (spesso con lo sviluppo di insufficienza valvolare) o dell'endocardio parietale (meno spesso è interessato l'endotelio dell'aorta o la grande arteria più vicina) . La malattia è causata da vari microrganismi patogeni ed è accompagnata da una lesione sistemica degli organi interni (reni, fegato, milza) sullo sfondo di un'alterata reattività dell'organismo. Eziologia. Gli agenti patogeni della malattia sono molto spesso il gruppo di microrganismi coccalici: streptococchi (lo streptococco viridans era precedentemente isolato nel 90% dei casi), stafilococchi (dorati, bianchi), enterococco, pneumococco. Negli ultimi anni, a causa dell’uso diffuso degli antibiotici, la gamma dei patogeni microbici è cambiata. La malattia può essere provocata dalla flora gram-negativa (Escherichia coli, Pseudomonas aeruginosa, Proteus, Klebsiella); è emerso l'importante ruolo dei funghi patogeni, Sarcinus, Brucella e dei virus. Le malattie causate da questi agenti patogeni sono più gravi, in particolare l'endocardite causata da un'infezione fungina (di solito si verifica a causa dell'uso irrazionale di antibiotici). Tuttavia, in un certo numero di pazienti il vero agente eziologico della malattia non viene rilevato (la frequenza dei risultati delle emocolture negative è del 20-50%). Spesso, l'infezione si verifica nel sito di una protesi valvolare - la cosiddetta protesica IE, che si sviluppa principalmente entro 2 mesi dall'intervento chirurgico di sostituzione della valvola cardiaca. In questo caso, l'agente eziologico della malattia ha spesso una natura streptococcica. Pertanto, le fonti di infezione e batteriemia nell'IE sono molto diverse (interventi chirurgici nel cavo orale, operazioni e procedure diagnostiche nell'area urogenitale, intervento chirurgico sul sistema cardiovascolare (compresa la sostituzione della valvola), permanenza prolungata del catetere in vena, frequenti infusioni endovenose e studi di metodi endoscopici, emodialisi cronica (shunt arterovenoso), somministrazione di farmaci per via endovenosa). Esistono le cosiddette IE primarie, che si sono sviluppate su valvole intatte, così come IE sullo sfondo di alterazioni congenite e acquisite nel cuore e nel suo apparato valvolare - endocardite secondaria. Questi cambiamenti consentono di distinguere i pazienti in gruppi di rischio separati: difetti cardiaci (congeniti e acquisiti), prolasso della valvola mitrale, aneurismi artero-venosi, aneurismi post-infartuati, shunt, condizione dopo l'intervento chirurgico sul cuore e sui grandi vasi. 18. Patogenesi e classificazione delle endocarditi infettive (IE) Patogenesi. Il meccanismo di sviluppo di IE è complesso e non sufficientemente studiato. Nello sviluppo della malattia si possono distinguere 3 fasi. Lo stadio I (infettivo-tossico) procede con vari gradi di gravità dell'intossicazione. C'è una crescita di batteri, la distruzione delle valvole, che porta allo sviluppo di malattie cardiache; nella stessa fase, il processo è spesso generalizzato a causa della diffusione ematogena dell'infezione: pezzi di cuspidi o colonie di microrganismi possono separarsi dalla valvola, le cuspidi possono rompersi. Stadio II - immuno-infiammatorio, in cui i microrganismi fissati sulle valvole causano un'autosensibilizzazione prolungata e un danno iperergico agli organi e ai tessuti del corpo (generalizzazione immunitaria del processo). Lo stadio III - distrofico - si verifica con la progressione del processo patologico: le funzioni di un certo numero di organi sono disturbate, si verifica insufficienza cardiaca e renale, che aggrava ulteriormente il decorso della malattia (vedi tabella). Classificazione tabellare di IE
Viene inoltre fatta una distinzione tra IE attivo e inattivo (guarito). Esiste anche una classificazione chirurgica, in cui sono presenti: 1) la lesione è limitata ai lembi valvolari; 2) la lesione si estende oltre la valvola. L'IE acuta (rapidamente progressiva, si sviluppa in 8-10 settimane) è rara, di solito in persone che non hanno precedentemente avuto malattie cardiache, e si manifesta clinicamente con un quadro di sepsi generale. L'IE subacuta (più comune) dura 3-4 mesi, con un'adeguata terapia farmacologica può verificarsi la remissione. L'IE prolungata dura molti mesi con periodi di esacerbazione e remissione, è caratterizzata da manifestazioni cliniche lievi. Con un decorso sfavorevole, si verificano gravi complicazioni e i pazienti muoiono per insufficienza cardiaca progressiva, aumentando l'intossicazione settica. 19. Quadro clinico e diagnosi di endocardite infettiva (IE) quadro clinico. Le manifestazioni di IE sono presentate come sindromi. 1. Sindrome da alterazioni infiammatorie e setticemia. 2. Sindrome di intossicazione generale dell'organismo. 3. Sindrome da danno valvolare. 4. Sindrome dei disordini immunitari "di laboratorio". 5. Sindrome delle complicanze tromboemboliche. 6. Sindrome di generalizzazione delle lesioni. La diagnosi di EI si basa principalmente sulla diagnosi precoce dell'agente eziologico della malattia. A questo scopo vengono utilizzati i seguenti studi di laboratorio e strumentali. 1. Ottenere un'emocoltura positiva. 2. Esecuzione dell'NBT (test del nitrobluetetrazolio). 3. Un esame del sangue clinico per rilevare gli indicatori di fase acuta: è possibile rilevare un aumento della VES a 50 mm / h o più, leucocitosi con uno spostamento della formula dei leucociti a sinistra o (nello stadio II) leucopenia e anemia ipocromica. 4. Identificazione dei cambiamenti immunologici. 5. L'analisi delle urine viene eseguita per chiarire le lesioni di vari organi e sistemi, quando viene rilevata la glomerulonefrite, manifestata da proteinuria, cilindruria ed ematuria. 6. Un segno diagnostico diretto di IE - la presenza di vegetazione sulle valvole cardiache - viene rilevato dall'ecocardiografia. Pertanto, dall'intera varietà di sintomi, dovrebbero essere distinti quelli principali e aggiuntivi. I criteri principali per la diagnosi di IE: 1) febbre con temperatura superiore a 38 °C con brividi; 2) Macchie di Lukin; 3) noduli di Osler; 4) endocardite su valvole invariate (primarie) o sullo sfondo di difetti cardiaci reumatici e congeniti. miocardite infettiva; 5) tromboembolismo arterioso multiplo, rotture di aneurismi micotici con emorragie; 6) splenomegalia; 7) emocoltura positiva; 8) un pronunciato effetto positivo dall'uso di antibiotici. Criteri aggiuntivi per la diagnosi di IE: 1) aumento della temperatura corporea fino a 38 °C, raffreddamento; 2) emorragie sulla pelle; 3) rapida perdita di peso; 4) artrite asimmetrica di piccole articolazioni di mani, piedi; 5) anemizzazione; 6) VES superiore a 40 mm/h; 7) SRV nettamente positivo; 8) la presenza del fattore reumatoide; 9) a-globuline superiori al 25%; 10) aumento del contenuto di immunoglobuline M, E e A. 20. Trattamento e prevenzione dell'endocardite infettiva (IE) Trattamento. Il trattamento dell'IE dovrebbe essere il più precoce ed etiotropico possibile, tenendo conto dei dati batteriologici. È consigliabile una combinazione di trattamento conservativo e chirurgico. Per il trattamento dell'IE in tutte le fasce d'età, vengono utilizzati principalmente antibiotici, che hanno un effetto battericida sui microrganismi. Il farmaco di prima scelta è ancora la penicillina. La dose giornaliera - fino a 20 UI viene somministrata per via endovenosa e intramuscolare. Tuttavia, non si deve escludere il fatto che nei pazienti di età anziana e senile, quando trattati con penicillina e altri antibiotici ad alte dosi, si osserva spesso un effetto cardiotossico. Con un'eziologia sconosciuta, il trattamento inizia con dosi elevate di benzilpenicillina per via intramuscolare o endovenosa fino a 18-000 unità o più, una combinazione con streptomicina fino a 000 g/m20 al giorno o aminoglicosidi (gentamicina, tobramicina a una velocità di 000-000 mg / giorno) viene utilizzato kg al giorno). Le cefalosporine sono anche i farmaci di base usati per trattare l'IE: i più comunemente usati sono claforan, cefamisina (1-4 g/die, per via intramuscolare ed endovenosa), nonché zeporina (6-4 g/die) e kefzol (fino a 10 g/die). -10 g per via endovenosa). ed ecc.). La fusidina ha un buon effetto antistafilococcico, in alcuni casi è efficace nella resistenza dei microrganismi ad altri antibiotici (16-8 g/die). Il trattamento con antibiotici viene prescritto a lungo in un corso di 1,5-2 mesi, fino a quando l'infezione non viene completamente eliminata. Con una ridotta immunoreattività del corpo, gli agenti antibatterici vengono combinati con l'immunoterapia passiva utilizzando immunomodulatori (timalina, T-attivina, ecc.). Per prevenire la trombosi, ad esempio, in caso di endocardite che si è sviluppata sullo sfondo della sepsi angiogenica, viene creata un'ipocoagulazione controllata utilizzando eparina (20-000 unità per via endovenosa o sottocutanea). Per inibire gli enzimi proteolitici si usa il contrico (fino a 25-000 unità per via endovenosa). Quando l'IE valvolare ha contribuito alla formazione di una cardiopatia valvolare o le manifestazioni della malattia non scompaiono nonostante la massiccia terapia antibiotica, è consigliabile eseguire un trattamento chirurgico. L'obiettivo principale dell'operazione è preservare la valvola del paziente. A volte si limitano alla rimozione di vegetazioni, rotture di sutura delle valvole, ecc. Se la valvola viene quasi completamente distrutta sotto l'influenza dell'infezione, viene sostituita con una artificiale (protesi) utilizzando protesi meccaniche e biologiche. Prevenzione. La prevenzione dell'IE consiste nella sanificazione tempestiva dei focolai cronici di infezione nella cavità orale, nelle tonsille, nel rinofaringe, nei seni paranasali, nell'uso della terapia antibiotica attiva per le malattie acute da streptococco e stafilococco (tonsillite, ecc.). Si raccomanda l'indurimento del corpo. 21. Eziologia dell'asma bronchiale (BA) Ad oggi non esiste una definizione esauriente di asma, tuttavia, la definizione più completa di questa malattia è stata data da G. B. Fedoseev nel 1982. L'asma bronchiale (BA) è una malattia ricorrente, cronica e indipendente con una lesione primaria del tratto respiratorio, il cui principale e obbligatorio meccanismo patogenetico è l'alterata reattività bronchiale dovuta a meccanismi specifici (immunologici) e (o) non specifici, congeniti o acquisiti, e il principale segno clinico (obbligatorio) è un attacco d'asma e (o) una condizione asmatica ( stato asmatico) a causa di spasmo della muscolatura liscia bronchiale, ipersecrezione, discrinia e gonfiore della mucosa bronchiale. Eziologia. Una combinazione di diversi fattori gioca un ruolo importante nella comparsa dell’asma. A questo proposito, ci sono 2 forme di asma: atopica (dal latino athopia - "predisposizione ereditaria") e infettiva-allergica. La predisposizione ereditaria è dovuta alla connessione di alcuni antigeni di istocompatibilità (HCA) con la gravità dell'asma e un aumento della gravità della malattia è particolarmente spesso osservato nei portatori degli antigeni B35 e B40. I fattori interni nello sviluppo della malattia sono difetti biologici del sistema immunitario, endocrino, sistema nervoso autonomo, sensibilità e reattività bronchiale, clearance mucociliare, endotelio vascolare polmonare, sistema di risposta rapida (mastociti, ecc.), metabolismo dell'acido arachidonico, eccetera. I fattori esterni includono: 1) allergeni infettivi (virus, batteri, funghi, lieviti, ecc.); 2) allergeni non infettivi (pollini, polveri, industriali, medicinali, alimentari; allergeni di zecche, insetti e animali); 3) irritanti meccanici e chimici (metallo, legno, silicato, polvere di cotone; vapori di acidi, alcali; fumi, ecc.); 4) fattori meteorologici e fisico-chimici (cambiamenti di temperatura e umidità dell'aria, fluttuazioni della pressione barometrica, campo magnetico terrestre, sforzo fisico, ecc.); 5) stress, effetti neuropsichici e attività fisica. Gli agenti infettivi possono avere non solo un effetto allergenico, ma anche ridurre la soglia di sensibilità del corpo agli allergeni non infettivi (atopici), aumentare la permeabilità della mucosa respiratoria per loro; per formare un cambiamento nella reattività delle cellule bersaglio (mastociti, basofili, monociti, ecc.) e dei sistemi effettori. 22. Patogenesi dell'asma bronchiale (BA) Patogenesi. L'alterata reattività bronchiale è l'anello centrale nella patogenesi della malattia e può essere primaria e secondaria. Nel primo caso, la variazione della reattività è congenita e acquisita. I cambiamenti secondari nella reattività bronchiale sono una manifestazione dei cambiamenti nella reattività del sistema immunitario, endocrino e nervoso del corpo. Quindi, parlando della patogenesi dell'AD, possiamo distinguere 2 gruppi di meccanismi: immunologici e non immunologici. Tipo I (atopico, reaginico o anafilattico). In risposta all'ingestione di antigeni esoallergeni (polline, proteine animali e vegetali, batteri e farmaci), si verifica un aumento della produzione (regine), che si fissano e si accumulano sui mastociti (cellule effettrici primarie). Questa è la fase immunologica dell'AD. Successivamente, si sviluppa la fase patochimica del processo: degranulazione dei mastociti con rilascio di sostanze vasoattive, broncospastiche e chemiotattiche (istamina, serotonina, vari fattori chemiotattici, ecc.). Sotto l'influenza di sostanze biologicamente attive, inizia lo stadio fisiopatologico della patogenesi: aumenta la permeabilità del letto microcircolatorio, che porta allo sviluppo di edema, infiammazione sierosa e broncospasmo. La reazione di tipo III (tipo immunocomplesso o fenomeno di Arthus) si sviluppa sotto l'influenza di esoallergeni ed endoallergeni. La reazione avviene nella zona dell'antigene in eccesso con la partecipazione di anticorpi precipitanti appartenenti alle immunoglobuline delle classi O e M. L'effetto dannoso del complesso antigene-anticorpo formato si realizza attraverso l'attivazione del complemento, il rilascio di enzimi lisosomiali. Vi sono danni alle membrane basali, spasmo della muscolatura liscia dei bronchi, vasodilatazione, aumento della permeabilità del microcircolo Il tipo IV (ipersensibilità cellulare, di tipo ritardato) è caratterizzato dal fatto che i linfociti sensibilizzati hanno un effetto dannoso. In questo caso, i mediatori della reazione allergica sono le linfochine (agiscono sui macrofagi, sulle cellule epiteliali), gli enzimi lisosomiali e un sistema di chinine attivato. Sotto l'influenza di queste sostanze, si verificano lo sviluppo di edema, gonfiore della mucosa, broncospasmo, iperproduzione di secrezioni bronchiali viscose. I meccanismi non immunologici sono il principale cambiamento nella reattività bronchiale a seguito di difetti biologici congeniti e acquisiti. Meccanismi non immunologici agiscono sulle cellule effettrici primarie o secondarie o sui recettori della muscolatura liscia dei bronchi, dei vasi sanguigni, delle cellule delle ghiandole bronchiali. Ciò modifica la reattività delle cellule bersaglio e, soprattutto, dei mastociti, che è accompagnata da un'eccessiva produzione di sostanze biologicamente attive (istamina, leucotrieni, ecc.). Recentemente si è parlato del ruolo speciale dell'insufficienza di glucocorticoidi e dei disturbi disovarici nella patogenesi dei disturbi da ostruzione bronchiale. L'insufficienza di glucocorticosteroidi porta allo sviluppo di iperreattività dei mastociti, diminuzione della sintesi di catecolamine, attivazione delle prostaglandine F2a e interruzione del sistema immunocompetente. 23. Classificazione dell'asma bronchiale (BA) Classificazione. La predominanza dell'uno o dell'altro meccanismo nella patogenesi dell'AD consente di distinguere le sue varie caratteristiche patogenetiche. Attualmente viene utilizzata la classificazione proposta da G. B. Fedoseev (1982). Fasi di sviluppo dell'AD. I - pre-asma (condizioni che minacciano lo sviluppo: bronchite acuta e cronica, polmonite acuta e cronica con elementi di broncospasmo in combinazione con rinite vasomotoria, orticaria). II - BA clinicamente formato (considerato tale dopo il primo attacco o immediatamente all'esordio dello stato asmatico). Moduli BA: 1) immunologico; 2) non immunologico. Meccanismi patogenetici (varianti cliniche e patogenetiche) dell'AD: 1) atopico; 2) dipendente dall'infezione; 3) autoimmune; 4) disordinato; 5) squilibrio neuropsichico; 6) squilibrio adrenergico; 7) squilibrio colinergico; 8) reattività bronchiale alterata primaria. La gravità del corso di BA: 1) decorso lieve (le esacerbazioni sono rare, 2-3 volte l'anno, gli attacchi di asma a breve termine vengono fermati assumendo vari farmaci broncodilatatori all'interno); 2) moderato (riacutizzazioni più frequenti 3-4 volte l'anno, gli attacchi di asma sono più gravi e interrotti da iniezioni di farmaci); 3) decorso grave (caratterizzato da esacerbazioni frequenti e prolungate, attacchi gravi, che spesso si trasformano in uno stato asmatico). Fasi della progressione dell'asma: 1) esacerbazione (la presenza di attacchi ricorrenti di asma o condizione asmatica); 2) riacutizzazione dell'esacerbazione (gli attacchi diventano più rari e lievi, i segni fisici e funzionali della malattia sono meno pronunciati rispetto alla fase di esacerbazione); 3) remissione (le manifestazioni tipiche della BA scompaiono: non si verificano attacchi di asma; la pervietà bronchiale viene ripristinata in tutto o in parte). Complicazioni: 1) polmonare: enfisema, insufficienza polmonare, atelettasia, pneumotorace, stato asmatico, ecc.; 2) extrapolmonare: cuore polmonare (compensato e scompensato con lo sviluppo di insufficienza cardiaca destra), distrofia miocardica, ecc. 24. Diagnosi differenziale dell'asma bronchiale (BA) Diagnosi differenziale. BA è differenziato dall'asma cardiaco (vedi Tabella 1). Tabella 1 Diagnosi differenziale di AD
25. Trattamento e prevenzione dell'asma bronchiale (BA) Trattamento. Nel trattamento dell'asma si raccomanda un approccio graduale (fase 1 - la gravità minima dell'asma, fase 4 - la massima). Stadio 1: un decorso lievemente intermittente in cui i sintomi dell'asma compaiono in seguito all'esposizione a un fattore scatenante (p. es., polline o peli di animali) oa causa dell'esercizio. Il trattamento consiste in farmaci profilattici, se necessario (vengono prescritti farmaci per via inalatoria: agonisti, cromoglicato, nedocromil o farmaci anticolinergici). Se l'asma si manifesta con sintomi più frequenti, un aumento della necessità di broncodilatatori, allora diventa necessario passare alla fase successiva. Fase 2. Corso lievemente persistente. La terapia primaria comprende farmaci antinfiammatori, corticosteroidi per via inalatoria, sodio cromoglicato o nedocromil sodico. Per le esacerbazioni più gravi e prolungate, viene somministrato un breve ciclo di corticosteroidi orali. Lo stadio 3 è caratterizzato da una moderata gravità di BA. Tali pazienti richiedono l'assunzione giornaliera di farmaci antinfiammatori profilattici. La dose di corticosteroidi per via inalatoria è di 800-2000 mcg in combinazione con broncodilatatori a lunga durata d'azione. Stadio 4. Asma grave, quando non è completamente controllato. In questo caso, l'obiettivo del trattamento è quello di ottenere i migliori risultati possibili. Il trattamento primario prevede la nomina di corticosteroidi per via inalatoria ad alte dosi. Un'esacerbazione più grave può richiedere un ciclo di trattamento con corticosteroidi orali, che vengono prescritti in dosi minime o a giorni alterni. Per prevenire lo sviluppo di effetti collaterali, vengono somministrate alte dosi di corticosteroidi per via inalatoria attraverso un distanziatore. Il passaggio 5 prevede la riduzione dei farmaci di supporto. Ciò è possibile se l'asma rimane sotto controllo per almeno 3 mesi, il che aiuta a ridurre il rischio di effetti collaterali e aumenta la suscettibilità del paziente al trattamento pianificato. La "riduzione" del trattamento viene effettuata sotto il costante controllo dei sintomi, delle manifestazioni cliniche e degli indicatori delle funzioni respiratorie riducendo (cancellando) gradualmente l'ultima dose o farmaci aggiuntivi. Prevenzione. La prevenzione primaria dell'asma comprende il trattamento di pazienti in stato di pre-asma, l'individuazione di difetti biologici in individui praticamente sani con un'eredità gravata che rappresentano una minaccia per l'insorgenza dell'asma, l'eliminazione di allergeni, irritanti e altri potenzialmente pericolosi fattori che possono portare allo sviluppo della malattia dall'ambiente del paziente. Quando si trattano pazienti in uno stato di preasma, è necessario disinfettare i focolai di infezione, trattare la rinosinusopatia allergica, applicare vari metodi di trattamento non farmacologico, tra cui agopuntura e psicoterapia, terapia fisica, baroterapia, cure termali. La realizzazione di hyposensitization specifico e nonspecifico è mostrata. 26. Eziologia e patogenesi della bronchite cronica (CB) La bronchite ostruttiva cronica è una lesione infiammatoria non allergica diffusa dell'albero bronchiale, causata da prolungati effetti irritanti sui bronchi di vari agenti, che ha un decorso progressivo ed è caratterizzata da ventilazione polmonare ostruttiva, formazione di muco e funzione drenante dei bronchi albero, che si manifesta con tosse, espettorato e mancanza di respiro. La bronchite cronica è divisa in primaria e secondaria. La bronchite cronica primaria è una malattia indipendente che non è associata ad altri processi broncopolmonari o danni ad altri organi e sistemi, in cui è presente una lesione diffusa dell'albero bronchiale. L'HB secondario si sviluppa sullo sfondo di altre malattie, sia polmonari che extrapolmonari. Eziologia. Nello sviluppo del CB giocano un ruolo come fattori esogeni. La sindrome ostruttiva si sviluppa a causa di una combinazione di una serie di fattori: 1) spasmo della muscolatura liscia dei bronchi a causa di effetti irritanti di fattori esogeni e alterazioni infiammatorie della mucosa; 2) ipersecrezione di muco, alterazioni delle sue proprietà reologiche, che portano all'interruzione del trasporto mucociliare e al blocco dei bronchi con un segreto viscoso; 3) metaplasia epiteliale da cilindrica a squamosa stratificata e sua iperplasia; 4) violazioni della produzione di tensioattivo; 5) edema infiammatorio e infiltrazione della mucosa; 6) collasso di piccoli bronchi e obliterazione dei bronchioli; 7) alterazioni allergiche nella mucosa. Vari rapporti di cambiamenti nella mucosa causano la formazione di una certa forma clinica: 1) con bronchite catarrale non ostruttiva, prevalgono alterazioni superficiali delle proprietà strutturali e funzionali della mucosa; 2) con bronchite mucopurulenta (purulenta), predominano i processi di infiammazione infettiva. Tuttavia, è anche possibile una situazione in cui la bronchite catarrale a lungo termine dovuta all'aggiunta di un'infezione può diventare mucopurulenta, ecc. Nella variante non ostruttiva di tutte le forme cliniche della bronchite cronica, i disturbi della ventilazione sono leggermente pronunciati; 3) i disturbi ostruttivi inizialmente compaiono solo sullo sfondo di un'esacerbazione della malattia e sono causati da alterazioni infiammatorie nei bronchi, iper e discrinia, broncospasmo (componenti reversibili dell'ostruzione), ma poi persistono costantemente, mentre la sindrome ostruttiva cresce lentamente. 27. Quadro clinico della bronchite cronica (CB) quadro clinico. I principali sintomi di HB sono tosse, produzione di espettorato, mancanza di respiro. Con un'esacerbazione della malattia oa causa dell'ipossia con lo sviluppo di insufficienza polmonare e altre complicazioni, vengono rivelati sintomi generali (sudorazione, debolezza, febbre, affaticamento, ecc.). La tosse è la manifestazione più tipica della malattia. Secondo la sua natura e consistenza dell'espettorato, si può assumere una variante del decorso della malattia. Con una variante non ostruttiva della bronchite catarrale, la tosse è accompagnata dal rilascio di una piccola quantità di espettorato acquoso mucoso (più spesso al mattino, dopo l'esercizio oa causa dell'aumento della respirazione). All'inizio della malattia, la tosse non infastidisce il paziente; la comparsa di una tosse parossistica indica lo sviluppo di un'ostruzione bronchiale. La tosse acquisisce un'ombra abbaiante ed è di natura parossistica con un pronunciato collasso espiratorio della trachea e grandi bronchi. Con la bronchite purulenta e mucopurulenta, i pazienti sono più preoccupati per la tosse con l'espettorato. In caso di esacerbazione della malattia, l'espettorato acquisisce un carattere purulento, la sua quantità aumenta, a volte l'espettorato viene escreto con difficoltà (a causa dell'ostruzione bronchiale durante l'esacerbazione). Nella variante ostruttiva della bronchite, la tosse è improduttiva e secca, accompagnata da mancanza di respiro, con una piccola quantità di espettorato. La mancanza di respiro si verifica in tutti i pazienti con bronchite cronica in vari momenti. La comparsa di mancanza di respiro nei pazienti con "tosse a lungo termine" inizialmente con uno sforzo fisico significativo indica l'aggiunta di ostruzione bronchiale. Con il progredire della malattia, la mancanza di respiro diventa più pronunciata e costante, cioè si sviluppa un'insufficienza respiratoria (polmonare). Nella variante non ostruttiva, il CB progredisce lentamente, la mancanza di respiro di solito compare 20-30 anni dopo l'esordio della malattia. Tali pazienti non risolvono quasi mai l'insorgenza della malattia, ma indicano solo la comparsa di complicanze o frequenti esacerbazioni. C'è una storia di ipersensibilità al freddo e la maggior parte dei pazienti riferisce di fumare a lungo termine. In un certo numero di pazienti, la malattia è associata a rischi professionali sul lavoro. Quando si analizza una storia di tosse, è necessario assicurarsi che il paziente non abbia altre patologie dell'apparato broncopolmonare (tubercolosi, tumori, bronchiectasie, pneumoconiosi, malattie sistemiche del tessuto connettivo, ecc.), accompagnate dagli stessi sintomi. A volte un'anamnesi indica emottisi dovuta a una lieve vulnerabilità della mucosa bronchiale. L'emottisi ricorrente indica una forma emorragica di bronchite. Inoltre, l'emottisi nella bronchite cronica a lungo termine può essere il primo sintomo di cancro ai polmoni o bronchiectasie. 28. Diagnosi di bronchite cronica (CB) Diagnostica. L'auscultazione rivela respiro affannoso (con lo sviluppo dell'enfisema può indebolirsi) e rantoli secchi di natura diffusa, il cui timbro dipende dal calibro dei bronchi colpiti (i sibili sibilanti ben uditi all'espirazione sono caratteristici delle lesioni dei piccoli bronchi) . Con un'esacerbazione della bronchite ostruttiva, aumenta la mancanza di respiro, aumentano i fenomeni di insufficienza respiratoria. Nei casi avanzati di bronchite cronica e con l'aggiunta di complicanze, compaiono segni di enfisema polmonare, insufficienza respiratoria e cardiaca (ventricolare destra) - cuore polmonare scompensato: acrocianosi, pastosità o gonfiore delle gambe e dei piedi, alterazioni delle unghie in la forma di occhiali da orologio e le falangi terminali delle mani e dei piedi - sotto forma di bacchette, gonfiore delle vene cervicali, pulsazione nella regione epigastrica dovuta al ventricolo destro, accento del II tono nel II spazio intercostale a sinistra dello sterno, ingrossamento del fegato. Gli indicatori di laboratorio e strumentali hanno un diverso grado di significatività a seconda della fase del processo. L'esame a raggi X del torace viene eseguito in tutti i pazienti con bronchite cronica, tuttavia, di norma, non ci sono cambiamenti nei polmoni su radiografie semplici. Potrebbe esserci una deformazione della maglia del modello polmonare, a causa dello sviluppo di pneumosclerosi. L'esame radiografico gioca un ruolo importante nella diagnosi delle complicanze (polmonite acuta, bronchiectasie) e nella diagnosi differenziale con malattie con sintomi simili. La broncografia viene utilizzata solo per diagnosticare le bronchiectasie. La broncoscopia è di grande importanza nella diagnosi della bronchite cronica e nella sua differenziazione dalle malattie che manifestano un quadro clinico simile. Conferma la presenza di un processo infiammatorio; chiarisce la natura dell'infiammazione; rivela disturbi funzionali dell'albero tracheobronchiale; aiuta a identificare le lesioni organiche dell'albero bronchiale. Lo studio della funzione della respirazione esterna viene effettuato per identificare i disturbi restrittivi e ostruttivi della ventilazione polmonare. Secondo lo spirogramma, vengono calcolati l'indice di Tiffno e l'indicatore di velocità dell'aria - PSDV. La valutazione congiunta della resistenza bronchiale e dei volumi polmonari aiuta anche a determinare il livello di ostruzione. La radiopulmonografia utilizzando l'isotopo radioattivo 133Xe viene eseguita per rilevare una ventilazione irregolare associata all'ostruzione dei piccoli bronchi. L'elettrocardiografia è necessaria per rilevare l'ipertrofia del ventricolo destro e dell'atrio destro che si sviluppa con l'ipertensione polmonare. Un esame del sangue clinico rivela eritrocitosi secondaria risultante da ipossia cronica con lo sviluppo di grave insufficienza polmonare. Gli indicatori di "fase acuta" sono espressi moderatamente. L'esame microbiologico dell'espettorato e del contenuto bronchiale è importante per identificare l'eziologia delle esacerbazioni della bronchite cronica e la scelta della terapia antimicrobica. 29. Diagnosi differenziale della bronchite cronica (CB) tavolo Criteri diagnostici differenziali per CB
30. Trattamento della bronchite cronica (CB) Trattamento. Include una serie di misure che differiscono durante il periodo di esacerbazione e remissione della malattia. Durante l'esacerbazione della bronchite cronica, si distinguono due direzioni di trattamento: etiotropica e patogenetica. Il trattamento etiotropico ha lo scopo di eliminare il processo infiammatorio nei bronchi: è indicata la terapia con antibiotici, sulfamidici, antisettici, fitoncidi, ecc.. Il trattamento viene iniziato con antibiotici della serie delle penicilline (penicillina, ampicillina) o un gruppo di cefalosporine (cefamesina , tseporina) e, in assenza di effetto, vengono utilizzati gli antibiotici del gruppo di riserva (gentamicina, ecc.). La via di somministrazione più preferita è quella intratracheale (aerosol o riempimento con una siringa laringea attraverso un broncoscopio). Il trattamento patogenetico è finalizzato al miglioramento della ventilazione polmonare; ripristino della pervietà bronchiale; controllo dell'ipertensione polmonare e dell'insufficienza ventricolare destra. Il ripristino della ventilazione polmonare, oltre all'eliminazione del processo infiammatorio nei bronchi, è facilitato dall'ossigenoterapia e dalla terapia fisica. La cosa principale nel trattamento della bronchite cronica - il ripristino della pervietà bronchiale - si ottiene migliorando il loro drenaggio ed eliminando il broncospasmo. Per migliorare il drenaggio bronchiale vengono prescritti espettoranti (bevanda calda alcalina, decotti di erbe, mukaltin, ecc.), Farmaci mucolitici (acetilcisteina, bromexina; con secrezione viscosa purulenta - aerosol di enzimi proteolitici - chimopsina, tripsina); viene utilizzata la broncoscopia terapeutica. Per eliminare il broncospasmo, viene utilizzata l'eufillina (per via endovenosa, in supposte, compresse), efedrina, atropina; gli appuntamenti soli in un aerosol di preparazioni simpatomimetichesky sono possibili: fenoterol, orciprenaline solfato (asthmopenta) e una nuova medicina domestica "Soventol", farmaci anticolinergici: atrovent, troventol. Preparazioni efficaci di aminofillina prolungata (teopec, teodur, theobelong, ecc.) - 2 volte al giorno. In assenza dell'effetto di tale terapia, piccole dosi di corticosteroidi vengono somministrate per via orale (10-15 mg di prednisolone al giorno) o per via intratracheale (sospensione di idrocortisone - 50 mg). Come terapia aggiuntiva, nominare: 1) farmaci antitosse: con tosse improduttiva - libexin, tusuprex, bromexina, con tosse secca - codeina, dionina, stoptussin; 2) farmaci che aumentano la resistenza dell'organismo: vitamine A, C, gruppo B, stimolanti biogenici. Attualmente, nel trattamento della bronchite cronica, vengono sempre più utilizzati farmaci immunocorrettivi: T-attivina o timalina (100 mg per via sottocutanea per 3 giorni); all'interno - catergen, nucleinato di sodio o pentossile (entro 2 settimane), levamisolo (decaris). Trattamento fisioterapico: prescrivere diatermia, elettroforesi con cloruro di calcio, quarzo sulla zona del torace, massaggio toracico ed esercizi di respirazione. 31. Polmonite. Eziologia, patogenesi, classificazione La polmonite è una malattia infettiva e infiammatoria acuta di natura focale, in cui le sezioni respiratorie e il tessuto connettivo interstiziale dei polmoni sono coinvolti nel processo patologico. Classificazione di EV Gembitsky (1983). Per eziologia: 1) batterico (che indica l'agente patogeno); 2) virale (che indica l'agente patogeno); 3) cornitico; 4) traballante; 5) micoplasma; 6) fungino; 7) misto; 8) infettivo-allergico; 9) eziologia sconosciuta. Per patogenesi: 1) primario; 2) secondario. Caratteristiche cliniche e morfologiche: 1) parenchimale: croupous; focale; 2) interstiziale. Per localizzazione ed estensione: unilaterale; bilaterale. Per gravità: estremamente grave; pesante; moderare; mite e abortivo. A valle: tagliente; protratto (risoluzione radiologica e clinica della polmonite). Eziologia. La maggior parte della polmonite è di origine infettiva. Le polmoniti allergiche e causate dall'azione di fattori fisici o chimici sono rare. Le polmoniti batteriche vengono diagnosticate più spesso nelle persone di mezza età e negli anziani; polmonite virale - nei giovani. Nell'eziologia della polmonite batterica primaria, il ruolo principale spetta agli pneumococchi. Durante un'epidemia di influenza, aumenta il ruolo delle associazioni virali-batteriche (di solito stafilococchi), nonché dei microrganismi opportunisti. Nella polmonite secondaria, il ruolo eziologico principale è svolto dai batteri gram-negativi (polmonite da klebsiella e bacillo influenzale); in caso di polmonite da aspirazione, l'importanza dell'infezione anaerobica è grande. Patogenesi. L'agente infettivo entra dall'esterno nelle sezioni respiratorie dei polmoni attraverso i bronchi: inalazione e aspirazione (dal rinofaringe o dall'orofaringe). Per via ematogena, il patogeno entra nei polmoni principalmente nella polmonite secondaria o nella genesi trombotica della polmonite. La diffusione linfogena dell'infezione con l'inizio della polmonite si osserva solo con lesioni al torace. Significativa importanza nella patogenesi della polmonite è attribuita anche alle reazioni allergiche e autoallergiche. 32. Diagnosi di polmonite Il più significativo per la diagnosi è la presenza di una sindrome di alterazioni infiammatorie nel tessuto polmonare. Questa sindrome è costituita dai seguenti sintomi: 1) ritardo nella respirazione del lato toracico colpito; 2) accorciamento del suono della percussione nell'area della proiezione della lesione in misura maggiore o minore; 3) aumento del tremore della voce e della broncofonia nella stessa area; 4) cambiamento nella natura della respirazione (dura, bronchiale, indebolita, ecc.); 5) la comparsa di rumori respiratori patologici (rantoli e crepiti umidi e gorgoglianti). La natura della respirazione può cambiare in diversi modi. Nella fase iniziale della polmonite crouposa, la respirazione può essere indebolita, con un'espirazione prolungata; nella fase di epatizzazione, insieme ad un aumento dell'ottusità del suono della percussione, si sente la respirazione bronchiale; con la risoluzione del fuoco polmonare con una diminuzione dell'ottusità della percussione, la respirazione diventa difficile. I sintomi aiutano a fare una diagnosi eziologica: 1) il rilevamento di un'eruzione cutanea a piccole macchie, come con la rosolia, in combinazione con linfoadenopatia è caratteristica dell'infezione da adenovirus; 2) l'allargamento locale dei linfonodi indica una polmonite perifocale; 3) polmonite fungina associata a lesioni delle mucose, della pelle e delle unghie; 4) la sindrome epatolienale e un leggero ittero si verificano nelle polmoniti cornitiche e curicketsi; 5) per la tipica polmonite crouposa, l'aspetto del paziente è caratteristico: viso pallido con arrossamento febbrile sul lato della lesione, eruzioni erpetiche, gonfiore delle ali del naso durante la respirazione. Il metodo più importante per chiarire la presenza di polmonite e il grado di coinvolgimento del tessuto polmonare nel processo è la fluorografia a grande telaio e l'esame a raggi X degli organi del torace. La broncografia rivela cavità di decadimento nel tessuto polmonare, nonché la presenza di bronchiectasie, attorno alle quali, durante l'esacerbazione, sono possibili alterazioni infiltrative (polmonite perifocale). L'esame batteriologico dell'espettorato (o lavaggi bronchiali) prima della nomina di antibiotici aiuta a rilevare l'agente patogeno e determinarne la sensibilità agli antibiotici. La gravità del processo infiammatorio è giudicata dalla gravità dei parametri ematici della fase acuta e dalla loro dinamica (leucocitosi con cambiamento nella formula dei leucociti, aumento della VES, aumento del contenuto di a2-globuline, fibrinogeno, comparsa di SRV, un aumento del livello di acidi sialici). Con un decorso prolungato di polmonite e lo sviluppo di complicanze, viene studiata la reattività immunologica dell'organismo. 33. Trattamento della polmonite Trattamento. Immediatamente dopo la diagnosi, è necessario iniziare la terapia etiotropica della polmonite. Di grande importanza sono le idee empiriche su un possibile patogeno, poiché l'esame batteriologico dell'espettorato è stato effettuato per un periodo piuttosto lungo e nella maggior parte dei pazienti, anche con un approccio moderno a questo studio, dà risultati incerti e talvolta errati. Al momento, le penicilline hanno perso la loro importanza come farmaco d'elezione nel trattamento della polmonite. In relazione a quanto sopra, nel trattamento della polmonite, viene prestata molta attenzione ai macrolidi, che si sono dimostrati efficaci non solo contro lo pneumococco, ma anche contro Mycoplasma pneumoniae, Chlamydia pneumoniae. Dosaggio di antibiotici utilizzati nel trattamento della polmonite. 1. Penicilline: benzilpenicillina (500-000 UI per via endovenosa ogni 1-000 ore o 000-6 UI ogni 8 ore per via intramuscolare), ampicillina (500-000-1 g per via intramuscolare ogni 000-000 ore o 4 g ogni 0,5 ore per via endovenosa), amoxicillina (1,0-2,0 g ogni 6 ore per via orale o 8-0,5 g ogni 6-0,5 ore per via intramuscolare, endovenosa), oxacillina (1,0 g ogni 8-0,5 ore per via orale, intramuscolare, endovenosa). 2. Cefalosporine: I generazione - cefalotina (keflin) (0,5-2,0 g ogni 4-6 ore per via intramuscolare, endovenosa), cefazolina (kefzol) (0,5-2,0 g, ogni 8 ore per via intramuscolare, endovenosa), II generazione - cefuroxima (zinacef , ketocef) (0,75-1,5 g ogni 6-8 ore per via intramuscolare, endovenosa), III generazione - cefotaxime (claforan) (1,0-2,0 g, massimo fino a 12 g/die ogni 12 ore per via intramuscolare, endovenosa), ceftriaxone (longacef, rocefin) (1,0-2,0-4,0 g ogni 24 ore per via intramuscolare, endovenosa). 3. Aminoglicosidi: Genetamicina (80 mg ogni 12 ore IM, IV), Amikacina (10-15 mg/kg ogni 12 ore IM, IV), Tobramicina (Brulamicina) (3-5 mg/kg ogni 8 ore IM, IV) . 4. Macrolidi: eritromicina (0,5 g ogni 6-8 ore per via orale o 0,5-1,0 g ogni 6-8 ore per via endovenosa), rovamicina (3,0 milioni UI ogni 8-12 ore per via orale o 1,5-3,0 milioni UI ogni 8-12 ore ore per via endovenosa). 5. Fluorochinoloni: pefloxacina (leflacina) (400 mg ogni 12 ore per via orale, EV), ciprofloxacina (cyprobay) (500 mg ogni 12 ore per via orale o 200-400 mg ogni 12 ore per via endovenosa), ofloxacina (zanocina, tarivid) (200 mg ogni 12 ore per via orale). 6. Tetracicline: doxiciclina (vibramicina) (200 mg il giorno 1, nei giorni successivi - 100 mg ogni 24 ore per via orale), minociclina (minocina) (200 mg il giorno 1, nei giorni successivi - 100 mg ogni 12 ore per via orale), aztreonam (azactam) (1,0-2,0 g ogni 8-12 ore), imipenem/cilstatina (thienam) (500 mg ogni 6-8 ore per via intramuscolare). 34. Eziologia, patogenesi, quadro clinico dell'esofagite acuta L'esofagite acuta è una lesione infiammatoria della membrana mucosa dell'esofago che dura da alcuni giorni a 2-3 mesi. Eziologia e patogenesi. Fattori eziologici: malattie infettive, lesioni, ustioni, avvelenamenti, reazioni allergiche, errori nutrizionali. Tra gli agenti infettivi, i più caratteristici dell'esofagite acuta sono la difterite, la scarlattina, il tifo e il tifo, l'influenza, la parainfluenza, l'infezione da adenovirus, la parotite. I fattori dannosi fisici e chimici sono rappresentati da radiazioni ionizzanti, ustioni chimiche, cibi caldi e molto freddi e spezie. quadro clinico. L'esofagite catarrale è la forma più comune di esofagite acuta. Si verifica sullo sfondo di errori nell'alimentazione: quando si mangiano piatti piccanti, freddi, caldi, con lievi ferite, l'alcol brucia. Si manifesta clinicamente con bruciore e dolore dietro lo sterno, costringendo i pazienti a rifiutare il cibo per diversi giorni. Esofagite di grado I-II annotato endoscopicamente, raggi X - ipercinesia dell'esofago. L'esofagite erosiva si verifica con malattie infettive e allergie. I sintomi clinici sono simili a quelli dell'esofagite catarrale. L'esofagite emorragica è una rara forma clinica di esofagite erosiva. L'eziologia è la stessa dell'esofagite erosiva. Sindrome da dolore intenso ed ematemesi sono clinicamente tipiche. La clinica è dominata da disfagia e dolore intenso, aggravato dopo aver mangiato, nausea, vomito. Con il vomito vengono rilasciati film di fibrina, potrebbe esserci emottisi. L'esofagite membranosa (esfoliativa) per eziologia è chimica (ustioni dell'esofago), infettiva. Nella clinica dell'esofagite membranosa grave, prevalgono intossicazione, disfagia e sindrome del dolore. L'esofagite necrotizzante è una forma rara di infiammazione acuta dell'esofago. Il suo sviluppo è facilitato dalla ridotta immunità in malattie così gravi come sepsi, febbre tifoide, candidosi, insufficienza renale allo stadio terminale. La clinica è caratterizzata da disfagia dolorosa, vomito, debolezza generale, sanguinamento, frequente sviluppo di mediastinite, pleurite, polmonite. L'esofagite settica è una rara infiammazione locale o diffusa delle pareti dell'esofago ad eziologia streptococcica o che si manifesta quando la mucosa è danneggiata da un corpo estraneo, con ustioni, ulcerazioni, e può passare dagli organi vicini. A volte l'esofagite flemmonica acuta si presenta come una complicazione di qualsiasi forma di esofagite acuta, portando alla fusione purulenta delle pareti dell'esofago. Il quadro clinico è caratterizzato da grave intossicazione, febbre alta, dolore dietro lo sterno e al collo, vomito. All'esame, c'è gonfiore al collo, la mobilità in questa parte della colonna vertebrale è limitata. La posizione della testa è forzata, con un'inclinazione su un lato. La malattia si trasforma spesso in mediastinite purulenta. 35. Trattamento e prognosi dell'esofagite acuta Trattamento. Principi di trattamento dell'esofagite acuta: etiotropica, patogenetica e sintomatica. Trattamento etiotropico - trattamento della malattia sottostante. Nelle malattie infettive complicate da esofagite acuta, vengono utilizzati antibiotici (per via parenterale). Con pronunciati cambiamenti necrotici ed emorragici nell'esofago, si raccomanda di astenersi dal mangiare per 2-3 settimane. In questo periodo sono indicate nutrizione parenterale, somministrazione endovenosa di idrolizzati proteici, miscele di aminoacidi, intralipidi, vitamine e terapia di disintossicazione. Dopo aver ridotto l'infiammazione, vengono prescritti cibi che risparmiano termicamente e chimicamente: latte caldo, panna, zuppe di verdure, cereali liquidi. Per ridurre i sintomi locali dell'infiammazione - soluzioni interne di tannino 1%, collargol - 2%, novocaina - 1-2% prima dei pasti. Gli astringenti vengono presi in posizione orizzontale con la testata del letto abbassata. In assenza dell'effetto della somministrazione locale di preparati astringenti, vengono prescritti analgesici non narcotici per via parenterale. Per ridurre gli effetti della discinesia esofagea, i farmaci procinetici (cerucal, raglan, cisapride) vengono utilizzati per via orale prima dei pasti. Con erosioni multiple, sono indicate preparazioni di bismuto (denol, vikair), iniezioni di solcoseryl. Con l'esofagite emorragica, complicata da sanguinamento, vengono utilizzati preparati di acido aminocaproico, vikasol, dicynone. Con un'emorragia massiccia, viene prescritta una trasfusione di sangue o plasma. Con esofagite purulenta e necrotica, il paziente deve essere sottoposto a nutrizione parenterale per molto tempo, viene utilizzata una terapia massiccia con diversi antibiotici e l'ascesso viene drenato. Le stenosi esofagee sono corrette dal bougienage. In rari casi, viene posizionata una gastrostomia. Previsione. La prognosi dell'esofagite catarrale ed erosiva è favorevole. La scomparsa spontanea dei sintomi dell'esofagite è possibile, a condizione che la malattia sottostante sia adeguatamente corretta. La prognosi dell'esofagite pseudomembranosa, esfoliativa e flemmonica è grave. In tutti i casi, previa guarigione dalla malattia di base, l'esofagite termina con la formazione di stenosi cicatriziali, che richiedono un'ulteriore correzione. I pazienti con forme gravi di esofagite complicate da stenosi dell'esofago non sono in grado di lavorare. La prevenzione dell'esofagite acuta consiste in una diagnosi e un trattamento adeguati e tempestivi della malattia sottostante. 36. Eziologia, patogenesi, quadro clinico dell'esofagite cronica L'esofagite cronica è un'infiammazione cronica della membrana mucosa dell'esofago che dura fino a 6 mesi. La variante più comune è l'esofagite peptica (esofagite da reflusso), che può essere complicata dall'ulcera peptica dell'esofago. Eziologia e patogenesi. La causa principale della malattia è il costante reflusso del contenuto gastrico nell'esofago, a volte nella bile e nel contenuto intestinale, cioè l'esofagite peptica è un'ustione asettica dell'esofago da parte dell'acido dello stomaco. Nella patogenesi dell'esofagite da reflusso, sono importanti il rigurgito di contenuto acido e una violazione della purificazione e dello svuotamento dell'esofago da esso. Esistono cinque criteri per la patogenicità del reflusso nella genesi dell'esofagite peptica: frequenza, volume, rigurgito, composizione chimica, condizione della mucosa esofagea e sensibilità a un fattore chimico (l'infiammazione delle pareti riduce la sensibilità), velocità di svuotamento (clearance) , che dipende principalmente dalla peristalsi attiva, dall'azione alcalinizzante della saliva e del muco. L'insorgenza dell'esofagite da reflusso è favorita dall'ernia dell'apertura esofagea del diaframma, dall'ulcera duodenale, dai disturbi post-gastroresezione e dalle allergie. Anche la predisposizione allergica conta. L'esame morfologico dei pazienti con esofagite peptica mostra edema, iperemia della mucosa, infiltrazione della sottomucosa del segmento sopradiaframmatico dell'esofago. quadro clinico. I segni tipici dell'esofagite da reflusso includono bruciore dietro lo sterno, bruciore di stomaco, rigurgito, che è aggravato dallo stare sdraiati, disfagia e l'effetto positivo dell'assunzione di antiacidi. Potrebbe esserci dolore dietro lo sterno dopo aver mangiato, simile all'angina pectoris. L'insorgenza di dolore nell'esofagite da reflusso è associata all'irritazione peptica della parete esofagea e ai suoi spasmi durante il rigurgito del contenuto gastrico acido, nonché alla violazione della mucosa prolassata. Caratteristiche distintive di questo dolore: il suo carattere lungo e bruciante, la localizzazione nel processo xifoideo, l'irradiazione lungo l'esofago, meno spesso nella metà sinistra del torace, nessun effetto evidente dall'assunzione di antiacidi, antispastici, aumentato in posizione orizzontale, soprattutto dopo mangiare. Particolare attenzione nella diagnosi clinica dovrebbe essere prestata ai sintomi minori della disfagia, come la sensazione di un nodulo dietro lo sterno, una sensazione di cibo caldo che passa attraverso l'esofago. Un segno di esofagite che inizia gradualmente può essere la salivazione e l'abitudine di bere acqua con il cibo. L'esame obiettivo dei pazienti con esofagite da reflusso non fornisce informazioni diagnostiche significative. Le complicanze dell'esofagite da reflusso comprendono sanguinamento, ulcerazione, stenosi, accorciamento dell'esofago e tumore maligno. L'esofagite da reflusso cronico può portare allo sviluppo di un'ernia iatale assiale. 37. Diagnosi, trattamento dell'esofagite cronica Diagnosi e diagnosi differenziale. Il metodo di ricerca più prezioso per questa patologia è l'endoscopia, durante la quale si notano iperemia, edema e ispessimento delle pieghe della mucosa. È necessario differenziare l'esofagite da reflusso con l'ulcera peptica dello stomaco e del duodeno, la malattia coronarica, la colecistite cronica e la pancreatite. Il sintomo principale nella diagnosi differenziale è il dolore. La differenziazione con l'ulcera peptica è aiutata dall'assenza di dolori tardivi e "affamati" nell'esofagite, nonché dai dati ottenuti dall'endoscopia dell'esofago e dello stomaco. Il dolore coronarico, a differenza dell'esofagite, è caratterizzato da una connessione con lo stress fisico ed emotivo, l'effetto dei nitrati, i segni di ischemia sull'ECG, compresi quelli secondo l'ergometria della bicicletta. I dati ecografici degli organi addominali aiutano a escludere la patologia della cistifellea e del pancreas come causa della sindrome del dolore. Trattamento. La terapia dell'esofagite da reflusso comprende il trattamento delle malattie che l'hanno causata e la nomina di una terapia antireflusso. Si consiglia ai pazienti di evitare di sollevare pesi, piegarsi. È necessario assumere la posizione corretta durante il riposo e il sonno (la testiera è rialzata di 15-20 cm, con un angolo di 30-50). Si consiglia di normalizzare il peso corporeo, mangiare in modo frazionato (l'ultimo pasto - 3 ore prima di coricarsi). Alcol e cibi piccanti sono esclusi dalla dieta. Assegna adsorbenti e farmaci alcalinizzanti che hanno un effetto protettivo sulla mucosa. Queste sostanze includono Venter, che viene somministrato per via orale 1 g (preferibilmente sotto forma di sospensione) 30-40 minuti prima dei pasti 3 volte al giorno e la 4a volta - a stomaco vuoto prima di coricarsi. Il corso del trattamento è di 8-10 settimane. Almagel, phosphalugel, maalox, gastal hanno un effetto simile. Questi farmaci vengono utilizzati nel periodo interdigestivo (1/2-2 ore dopo i pasti e durante la notte) fino alla completa remissione. Phosphalugel e Maalox sono prescritti 1-2 pacchetti 2-3 volte al giorno, gastal - 2-3 compresse al giorno. Non è consigliabile utilizzare la soda di tè, una miscela di Bourget, argilla bianca a causa dell'insufficiente efficienza. Ad azione avvolgente e astringente ha nitrato di bismuto 1 g 3-4 volte al giorno. È stata notata un'elevata attività antireflusso di un nuovo antiacido, il topalkan. Acque minerali - "Borjomi", "Essentuki No. 4", "Jermuk", "Smirnovskaya" hanno un effetto alcalinizzante. Per ridurre la secrezione gastrica acida, vengono prescritti bloccanti dei recettori H2 dell'istamina (cimetidina, ranitidina, famotidina), inibitori della Ka-K-ATPasi (omeprazolo), un bloccante selettivo dei recettori M-colinergici delle cellule parietali e il suo analogo buscopan. Previsione e prevenzione. La prognosi per la vita e il lavoro è favorevole. In un corso complicato, la prognosi è determinata dalla tempestività e dalla qualità delle cure mediche. Ai pazienti con decorso grave viene assegnato un gruppo di disabilità. I pazienti con esofagite da reflusso cronico devono essere sotto la supervisione di un gastroenterologo. Almeno 2 volte l'anno sono indicati studi endoscopici e morfologici a causa della possibilità di malignità. 38. Ulcera peptica dell'esofago L'ulcera peptica dell'esofago è una malattia acuta o cronica caratterizzata dall'ulcerazione della mucosa dell'esofago distale sotto l'influenza del succo gastrico attivo. Eziologia e patogenesi. Le ulcere peptiche croniche dell'esofago sono complicazioni dell'esofagite da reflusso e dell'ernia iatale. La loro insorgenza è facilitata dall'esofago corto interno, metaplasia focale della mucosa, eterotopia della mucosa gastrica nell'esofago, malattia da reflusso con insufficienza cardiaca, malattie accompagnate da vomito frequente (sindrome post-vagotomia, sindrome dell'ansa afferente, alcolismo cronico). Quadro clinico. I sintomi dell'ulcera peptica dell'esofago assomigliano al quadro clinico dell'esofagite peptica: si verificano bruciore di stomaco persistente, peggioramento dopo aver mangiato, quando si piega il corpo, in posizione sdraiata, rigurgito, dolore durante la deglutizione e passaggio alterato del cibo solido. I sintomi clinici della perforazione sono indistinguibili dai sintomi della lesione meccanica acuta penetrante e non penetrante da corpi estranei. Circa il 14% delle ulcere esofagee penetra nei tessuti circostanti. Diagnosi e diagnosi differenziale. Sulla base dei sintomi clinici, è estremamente difficile sospettare un'ulcera peptica. La diagnosi viene verificata nel corso della ricerca strumentale e di laboratorio. L'esame radiografico ed endoscopico più informativo. Le informazioni più affidabili nella verifica dell'ulcera peptica dell'esofago sono fornite dall'endoscopia e dalla biopsia multipla dai bordi dell'ulcera. Quando si fa avanzare l'endoscopio all'ulcera peptica, vengono rilevati segni di esofagite di stadio I-IV, disfunzione motoria dell'esofago, edema perifocale e iperemia della mucosa. È necessario differenziare le ulcere peptiche dell'esofago con ulcerazioni di natura specifica (con tubercolosi, sifilide). In queste situazioni, i test sierologici specifici, i risultati degli studi istologici e batteriologici aiutano significativamente. La combinazione della patologia dell'esofago con danni ai polmoni e ad altri organi rende necessario esaminare in modo mirato il paziente in relazione a un processo specifico. Trattamento. Il trattamento include la nomina di una dieta: si raccomanda il risparmio di cibo meccanicamente e chimicamente, che viene assunto in piccole porzioni 5-6 volte al giorno. Per prevenire il reflusso del contenuto dallo stomaco nell'esofago, la posizione del paziente a letto dovrebbe essere con una testiera rialzata. I medicinali vengono presi sdraiati. Assegnare la monoterapia con un farmaco di uno dei seguenti gruppi farmacologici: antisecretori, inclusi antiacidi e adsorbenti, stimolanti della funzione di evacuazione motoria dello stomaco (procinetica), farmaci - simulatori di muco. La terapia viene eseguita per molto tempo - 1,5-3 mesi. Indicazioni per il trattamento chirurgico - mancanza di guarigione entro 6-9 mesi, decorso complicato (perforazione, penetrazione, stenosi, sanguinamento). Previsione e prevenzione. La prognosi per la vita e il lavoro è favorevole. 39. Eziologia, patogenesi, quadro clinico della gastrite cronica La gastrite cronica è una malattia clinicamente caratterizzata da dispepsia gastrica e morfologicamente - da cambiamenti infiammatori e degenerativi nella mucosa gastrica, processi di rinnovamento cellulare alterati e un aumento del numero di plasmacellule e linfociti nella membrana stessa della mucosa. Eziologia e patogenesi. Allo stato attuale di sviluppo della gastroenterologia, è stato stabilito che la comparsa della gastrite cronica è favorita dall'espansione microbica dell'Helicobacter pylori (HP), che causa gastrite antrale nel 95% dei casi e pangastrite nel 56% dei casi. I fattori eziologici della gastrite cronica possono essere attribuiti con un alto grado di certezza a fattori di rischio (alimentazione squilibrata irregolare, fumo, assunzione di alcol, ipersecrezione di acido cloridrico e pepsina). Il ruolo principale nello sviluppo della malattia appartiene anche ai meccanismi autoimmuni, accompagnati dall'accumulo di anticorpi contro le cellule parietali della mucosa gastrica, dall'ereditarietà aggravata e dall'uso di farmaci che hanno un effetto dannoso sulla mucosa gastrica. Classificazione. Nel 1990, al IX Congresso Internazionale dei Gastroenterologi in Australia, è stata adottata una nuova sistematizzazione della gastrite cronica, chiamata sistema di Sydney. Basi istologiche di classificazione. 1. Eziologia: gastrite cronica associata a HP, gastrite autoimmune, idiopatica, acuta da farmaci. 2. Topografia: antrale, fondo, pangastrite. 3. Morfologia: forme acute, croniche, speciali. Base di classificazione endoscopica: 1) gastrite dell'antro dello stomaco; 2) gastrite del corpo dello stomaco; 3) pangastrite; 4) alterazioni della mucosa gastrica: edema, eritema, vulnerabilità della mucosa, essudato, erosioni piatte, erosioni elevate, iperplasia delle pieghe, atrofia delle pieghe, visibilità del pattern vascolare, emorragie sopramucose. quadro clinico. La gastrite cronica è una delle malattie più comuni nella clinica delle malattie interne. La sua frequenza tra gli abitanti del globo varia dal 28 al 75%. La gastrite cronica si manifesta più spesso con sintomi di dispepsia gastrica e dolore nella regione epigastrica. Raramente è asintomatico. Un posto altrettanto importante nel quadro clinico della gastrite cronica è la sindrome dispeptica: nausea, eruttazione (acido, amaro, marcio), bruciore di stomaco, stitichezza o diarrea, feci instabili. Con la gastrite antrale isolata, i disturbi di bruciore di stomaco e stitichezza, derivanti dall'ipersecrezione di acido cloridrico e pepsina, diventano fondamentali. 40. Diagnosi e trattamento della gastrite cronica Diagnostica. La gastrite cronica scorre a lungo, con un aumento dei sintomi nel tempo. Le esacerbazioni sono provocate da violazioni alimentari. Il quadro fisico della gastrite cronica è piuttosto scarso. Nell'80-90% dei pazienti durante un'esacerbazione della malattia, uno studio oggettivo determina solo il dolore locale nella regione epigastrica. Quando la gastrite cronica è combinata con duodenite, colecistite o pancreatite, è possibile determinare la localizzazione del dolore che non è tipica della gastrite, ma caratteristica della patologia di un altro organo. È più probabile che un esame radiografico escluda altre malattie dello stomaco (ulcera, cancro), aiuti nella diagnosi della malattia di Menetrier piuttosto che confermare la diagnosi di gastrite cronica. A causa della scarsità delle manifestazioni cliniche della malattia, nonché della non specificità dei test di laboratorio, la diagnosi di gastrite cronica si basa sui risultati di studi endoscopici e morfologici. L'endoscopia rivela cambiamenti nella gravità della mucosa gastrica di varia gravità: edema, eritema, vulnerabilità della mucosa, essudato, erosioni piatte, erosioni in rilievo, iperplasia o atrofia delle pieghe, visibilità del pattern vascolare, emorragie sottomucose. Le manifestazioni cliniche caratteristiche della gastrite si osservano anche in altre malattie dell'apparato digerente, pertanto, nel processo di diagnosi, sono necessari l'ecografia della cavità addominale, un approfondito esame endoscopico e morfologico degli organi digestivi. Trattamento. I pazienti con gastrite necessitano di misure mediche generali: alimentazione regolare ed equilibrata, normalizzazione del regime di lavoro e riposo, livellamento di situazioni stressanti del piano domestico e industriale. La terapia farmacologica è indicata solo in presenza di manifestazioni cliniche di gastrite cronica. I pazienti con gastrite associata ad HP vengono trattati secondo il programma per l'ulcera peptica (vedi lezione successiva). Le persone con gastrite autoimmune necessitano di vitamina B12 (500 mcg una volta al giorno per via sottocutanea per 1 giorni, seguiti da cicli ripetuti di trattamento), acido folico (30 mg al giorno), acido ascorbico (fino a 5 g al giorno). Se necessario, viene eseguita la terapia sostitutiva con preparati enzimatici (mezim-forte, festal, enzistal, creon, pancitrato, acidin-pepsina). La sindrome del dolore viene solitamente interrotta dalla nomina di antiacidi (maalox, almagel, gastal) o bloccanti del recettore dell'istamina H (ranitidina, famotidina) a dosi terapeutiche medie. Con forme speciali di gastrite, è necessario il trattamento della malattia sottostante. Previsione e prevenzione. La prognosi per la vita e il lavoro è favorevole. La prevenzione della gastrite si riduce a un'alimentazione razionale, al rispetto del regime di lavoro e di riposo, limitando l'assunzione di FANS. 41. Eziologia dell'ulcera gastrica L'ulcera peptica (ulcera peptica) è una malattia cronica recidivante, manifestata clinicamente da una patologia funzionale della zona gastroduodenale e morfologicamente - da una violazione dell'integrità dei suoi strati mucosi e sottomucosi, e quindi l'ulcera guarisce sempre con la formazione di una cicatrice. Eziologia. Il principale fattore eziologico dell'ulcera peptica è l'espansione microbica di HP sulla superficie dell'epitelio dello stomaco. Il significato dell'aggressività batterica nell'eziologia della malattia è stato studiato dal 1983, quando J. Warren e B. Marshall hanno riportato la scoperta di un gran numero di batteri S-spirale sulla superficie dell'epitelio dell'antro dello stomaco. Gli elicobatteri sono in grado di esistere in un ambiente acido grazie alla produzione dell'enzima ureasi, che converte l'urea (dal flusso sanguigno) in ammoniaca e anidride carbonica. I prodotti dell'idrolisi enzimatica neutralizzano l'acido cloridrico e creano le condizioni per modificare il pH dell'ambiente attorno a ciascuna cellula batterica, fornendo così condizioni favorevoli per l'attività vitale dei microrganismi. Non meno importanti nello sviluppo dell'ulcera peptica sono gli effetti neuropsichici, la predisposizione ereditaria, gli agenti infettivi, gli errori alimentari e l'assunzione di determinati farmaci e le cattive abitudini. I fattori ereditari sono popolari tra i ricercatori: l'inerzia dei principali processi nervosi, le proprietà specifiche del gruppo del sangue, le caratteristiche immunologiche e biochimiche, la sindrome del carico ereditario. Nell'insorgenza dell'ulcera peptica, un'importanza essenziale è stata attribuita alle violazioni alimentari. Tuttavia, gli studi clinici e sperimentali condotti negli ultimi due decenni nella maggior parte dei casi non hanno rivelato l'effetto dannoso dei prodotti alimentari sulla mucosa gastroduodenale. La prevalenza dell'ulcera peptica tra contingenti significativi di persone con abitudini alimentari diverse testimonia anche la principale importanza dei fattori nutrizionali. Disturbi del ritmo e della regolarità dell'alimentazione, lunghe pause tra i pasti, alimentazione prematura sono essenziali per l'insorgenza dell'ulcera peptica. I ricercatori hanno espresso opinioni relativamente contrastanti sul ruolo dell'alcol nell'ulceragenesi. È noto che l'alcol provoca cambiamenti atrofici nella mucosa gastrica. Queste osservazioni sono in conflitto con il concetto generale di formazione dell'ulcera. Il ruolo degli effetti medicinali nell'ulceragenesi è oggetto di studio attivo. I risultati degli studi pubblicati in letteratura e i nostri dati indicano che i farmaci antinfiammatori non steroidei e gli ormoni glucocorticoidi hanno le proprietà ulcerogeniche più pronunciate. 42. Diagnosi di ulcera gastrica Diagnostica. Nel decorso semplice dell'ulcera peptica, non ci sono cambiamenti nell'analisi del sangue generale, sono possibili una certa diminuzione della VES, una leggera eritrocitosi. Con l'aggiunta di complicazioni, l'anemia appare negli esami del sangue, leucocitosi - quando il peritoneo è coinvolto nel processo patologico. Non ci sono cambiamenti nell'analisi generale delle urine. Il metodo tradizionale di ricerca nella patologia dello stomaco è la determinazione dell'acidità del contenuto gastrico. Sono possibili vari indicatori: elevati e normali, in alcuni casi persino ridotti. Un'ulcera duodenale si verifica con un'elevata acidità del succo gastrico. Nell'esame a raggi X, un'ulcera peptica è una "nicchia" - un deposito di sospensione di bario. La gastroduodenoscopia con biopsia è il metodo più affidabile per diagnosticare l'ulcera peptica. Consente di valutare la natura dei cambiamenti della mucosa ai margini dell'ulcera, nella zona periulcera e garantisce l'accuratezza della diagnosi a livello morfologico. Studi endoscopici e morfologici hanno dimostrato che la maggior parte delle ulcere gastriche si trova nell'area della curvatura minore e dell'antro, molto meno spesso - sulla curvatura maggiore e nell'area del canale pilorico. Il 90% delle ulcere duodenali si trova nella regione bulbare. Uno studio morfologico di un campione bioptico ottenuto dal fondo e dai bordi dell'ulcera rivela detriti cellulari sotto forma di un accumulo di muco con una miscela di leucociti in decomposizione, eritrociti e cellule epiteliali desquamate con fibre di collagene situate al di sotto. 43. Trattamento dell'ulcera gastrica Trattamento. La terapia razionale per l'ulcera peptica dovrebbe includere un regime, un'alimentazione appropriata, trattamento farmacologico, psicoterapia, trattamenti fisici e termali. Durante il periodo di esacerbazione dell'ulcera peptica, è necessario osservare rigorosamente la frammentazione nella nutrizione (da 4 a 6 volte al giorno con una piccola quantità di ogni porzione di cibo assunta a determinate ore). I prodotti alimentari dovrebbero avere buone proprietà tampone e contenere una quantità sufficiente di proteine (120-140 g). La psicoterapia è essenziale per fermare o ridurre le reazioni psiconevrotiche derivanti dalla sindrome del dolore persistente e dalla sua aspettativa. I medicinali usati per il trattamento dell'ulcera peptica sono divisi in 5 gruppi: 1) farmaci che agiscono sul fattore acido-peptico (antiacidi e bloccanti H2 dell'istamina, altri agenti antisecretori); 2) farmaci che migliorano la barriera mucosa gastrica; 3) farmaci che aumentano la sintesi delle prostaglandine endogene; 4) agenti antibatterici e antisettici; 5) farmaci che normalizzano i disturbi dell'evacuazione motoria dello stomaco e del duodeno. Antiacidi: 1) solubile (assorbibile) - bicarbonato di sodio, carbonato di calcio (gesso) e ossido di magnesio (magnesia bruciata); 2) insolubile (non assorbibile): trisilicato di magnesio e idrossido di alluminio. Diversi schemi di terapia combinata (a due, tre, quattro componenti). Terapia a due componenti: amoxicillina 1000 mg 2 volte al giorno per 2 settimane; omeprazolo 40 mg due volte al giorno. Lo schema a tre componenti include la preparazione di bismuto colloidale 2 mg 120 volte al giorno; tetraciclina 4 mg 250 volte al giorno; metronidazolo 4 mg 250 volte al giorno. Il ciclo di terapia è di 4 giorni. Il regime a quattro componenti prevede omeprazolo 20 mg 2 volte al giorno dal 1° al 10° giorno; denol 120 mg 4 volte al giorno dal 4° al 10° giorno; tetraciclina 500 mg 4 volte al giorno dal 4° al 10° giorno; metronidazolo 500 mg 3 volte al giorno dal 4° al 10° giorno. Il più efficace è un regime di trattamento a quattro componenti per le ulcere gastriche e duodenali. 6 settimane dopo la sua attuazione, si osserva la guarigione del difetto peptico nel 93-96% dei pazienti. Dopo la cicatrizzazione di un'ulcera peptica dello stomaco e del duodeno, vengono tradizionalmente utilizzati due tipi di trattamento. 1. La terapia di mantenimento continua viene eseguita con farmaci antisecretori a metà della dose giornaliera per un periodo fino a un anno. 2. La terapia "on demand", prevede l'uso di uno degli agenti antisecretori a metà della dose giornaliera per due settimane quando compaiono i sintomi dell'ulcera peptica. 44. Enterite cronica. Eziologia, patogenesi, classificazione L'enterite cronica è una malattia dell'intestino tenue, caratterizzata da una violazione delle sue funzioni (digestione e assorbimento) sullo sfondo di cambiamenti distrofici e disrigenerativi, culminanti nello sviluppo di infiammazione, atrofia e sclerosi della mucosa dell'intestino tenue. Eziologia e patogenesi. Questa è una malattia polieziologica che può essere l'esito di un'infiammazione acuta dell'intestino tenue o di un processo cronico primario. Negli ultimi anni, Yersinia, Helicobacteria, Proteus, Pseudomonas aeruginosa, rotavirus, numerosi rappresentanti di protozoi ed elminti (giardia, ascaris, tenie, opistorchia, cryptosporidium) hanno avuto grande importanza come fattore eziologico nell'enterite cronica. Di grande importanza nell'insorgenza di enterite cronica sono i fattori alimentari: eccesso di cibo, cibo secco, cibi squilibrati, prevalentemente carboidrati, abuso di spezie. L'enterite è causata da radiazioni ionizzanti, esposizione a sostanze tossiche e farmaci. Tra i comuni meccanismi patogenetici delle malattie croniche dell'intestino tenue, ci sono cambiamenti nella microflora intestinale sullo sfondo di una diminuzione dell'immunità locale e generale. I cambiamenti nello stato immunitario - una diminuzione del contenuto di lgA secretorie, un aumento del livello di lgE, una diminuzione della trasformazione blastica dei linfociti e l'inibizione della migrazione dei leucociti - portano alla colonizzazione dell'intestino tenue da parte dei rappresentanti della microflora opportunistica e di un diminuzione della normale flora anaerobica. Morfologicamente, l'enterite cronica si manifesta con cambiamenti infiammatori e disrigenerativi nella mucosa dell'intestino tenue. Se il processo progredisce, si osservano atrofia e sclerosi. Classificazione (Zlatkina AR, Frolkis AV, 1985). 1. Eziologia: infezioni intestinali, invasioni elmintiche, fattori alimentari, fisici e chimici, malattie dello stomaco, pancreas, vie biliari. 2. Fasi della malattia: esacerbazione; remissione. 3. Grado di gravità: lieve; moderare; pesante. 4. Flusso: monotono; ricorrente; continuamente ricorrente; latente. 5. Carattere dei cambiamenti morfologici: eunità senza atrofia; jeunitis con moderata atrofia parziale dei villi; jeunitis con parziale atrofia dei villi; jeunitis con atrofia totale dei villi. 6. La natura dei disturbi funzionali: disturbi della digestione della membrana (carenza di disaccaridasi), malassorbimento di acqua, elettroliti, oligoelementi, vitamine, proteine, grassi, carboidrati. 7. Complicanze: solarite, mesadenite aspecifica. 45. Quadro clinico e diagnosi di enterite cronica quadro clinico. Il quadro clinico dell'enterite cronica è costituito da sindromi enteriche locali e generali. Il primo è dovuto a una violazione dei processi di digestione parietale (membrana) e della cavità (maldigestione). I pazienti lamentano flatulenza, dolore nella zona paraombelicale, gonfiore a forma di berretto, forte brontolio, diarrea, costipazione meno frequente. La palpazione rivela dolore nel mesogastrio, così come a sinistra e sopra l'ombelico (sintomo positivo di Porges), rumore di schizzi nella regione del cieco (sintomo di Obraztsov). Le feci acquisiscono un aspetto argilloso, è caratteristica la polifecalia. La sindrome enterale generale è associata a un ridotto assorbimento degli ingredienti alimentari (malassorbimento), con conseguenti disturbi di tutti i tipi di metabolismo, cambiamenti nell'omeostasi. Caratterizzato da molteplici disordini metabolici, principalmente proteici, che si manifesta con una progressiva perdita di peso corporeo. I cambiamenti nel metabolismo dei carboidrati sono meno pronunciati, che si manifestano con gonfiore, brontolio nell'addome e aumento della diarrea durante l'assunzione di latticini. In larga misura, la carenza di peso corporeo nei pazienti è dovuta non solo alle proteine, ma anche allo squilibrio lipidico. I cambiamenti nel metabolismo dei lipidi sono strettamente correlati ai disordini metabolici delle vitamine e dei minerali liposolubili (calcio, magnesio, fosforo). I segni caratteristici della carenza di calcio sono un sintomo positivo del rollio muscolare, convulsioni, fratture ossee "immotivate" ricorrenti, osteoporosi, osteomalacia. Diagnosi e diagnosi differenziale. Un esame del sangue generale rivela anemia micro e macrocitica, un aumento della VES e, nei casi più gravi, linfo- ed eosinopenia. Se la malattia è di origine parassitaria, nel sangue si possono osservare linfocitosi ed eosinofilia. L'esame scatologico rivela un tipo intestinale di steatorrea da acidi grassi e saponi, creatorea, amilorrea. Il contenuto di enterochinasi e fosfatasi alcalina nelle feci aumenta. La massa giornaliera di feci aumenta in modo significativo. Un esame del sangue biochimico rivela ipoproteinemia, ipoalbuminemia, ipoglobulinemia, ipocalcemia, diminuzione dei livelli di magnesio, fosforo e altri microelementi, disturbi nel metabolismo degli elettroliti sotto forma di diminuzione dei livelli di sodio e potassio. Il quadro morfologico di una forma lieve di enterite cronica è caratterizzato da ispessimento dei villi, loro deformazione, diminuzione della profondità dei recessi, diminuzione del tono della muscolatura liscia, edema subepiteliale, alterazioni degenerative della superficie dell'epitelio , assottigliamento del bordo a spazzola delle cellule, diminuzione del numero di cellule caliciformi nella regione dei villi, aumento del numero di cripte e infiltrazione del proprio strato mucosa con elementi linfoplasmocitici, diminuzione delle cellule di Paneth in l'area del fondo delle cripte. 46. Trattamento, prognosi di enterite cronica Trattamento. Il trattamento dell'enterite cronica dovrebbe essere completo, compresi gli agenti che influenzano i fattori eziologici, i meccanismi patogenetici, nonché i sintomi locali e generali della malattia. La base è l'alimentazione dietetica, che aiuta a ridurre l'aumento della pressione osmotica nella cavità intestinale, riduce la secrezione e normalizza il passaggio del contenuto intestinale. La terapia farmacologica deve essere etiotropica, patogenetica e sintomatica. Trattamento etiotropico: per la disbiosi di grado II-IV vengono prescritti farmaci antibatterici: metronidazolo (0,5 g 3 volte al giorno), clindamicina (0,5 g 4 volte al giorno), cefalexina (0,5 g 2 volte al giorno), biseptolo (). 0,48 g 2 volte al giorno), sulgin (1 g 3-4 volte al giorno), furazolidone (0,1 g 4 volte al giorno). Dopo aver usato farmaci antibatterici, vengono prescritti eubiotici: bifidumbacterin o bificol 5 dosi 3 volte al giorno 30 minuti prima dei pasti, colibacterin o lactobacterin 3 dosi 3 volte al giorno prima dei pasti, hilak-forte 40 gocce 3 volte al giorno prima dei pasti. Il trattamento con preparati batterici viene effettuato a lungo: 3 cicli di 3 mesi ogni anno. Per la disbatteriosi da stafilococco viene prescritto il batteriofago antistafilococco (20 ml 3 volte al giorno per 15-20 giorni), per la disbatteriosi del proteo - batteriofago coliproteo per via orale, 20 ml 3 volte al giorno, il corso del trattamento è di 2-3 settimane. Per migliorare il processo di digestione si raccomandano gli enzimi: pancreatina, panzinorm forte, festal, digestal, pankurmen, mezim forte, trienzyme, le cui dosi sono selezionate individualmente (da 1 compressa 3 volte al giorno a 3-4 compresse 4 volte al giorno ) e che vengono prescritti direttamente prima o durante i pasti per 2-3 mesi. Se necessario, la terapia enzimatica sostitutiva viene proseguita per un periodo più lungo. Per correggere i disturbi idrici ed elettrolitici, la somministrazione endovenosa di panangin 20-30 ml, gluconato di calcio 10% 10-20 ml in 200-400 ml di soluzione isotonica o soluzione di glucosio, soluzioni poliioniche "Disol", "Trisol", "Quartasol" sono indicato. Le soluzioni elettrolitiche vengono somministrate per via endovenosa per 10-20 giorni sotto il controllo dello stato acido-base e del livello degli elettroliti nel sangue. Previsione e prevenzione. La prognosi per la vita e la capacità lavorativa nella maggior parte dei casi è favorevole. I segni prognosticamente sfavorevoli sono un decorso continuamente recidivante della malattia, una forte perdita di peso significativa, l'anemia, una sindrome da disturbi endocrini (diminuzione della libido, dismenorrea, infertilità). La prevenzione dell'enterite cronica consiste nel trattamento tempestivo delle infezioni intestinali acute e delle malattie concomitanti della zona gastroduodenale, nel rispetto della dieta, nella somministrazione profilattica di preparati batterici durante i raggi X e la radioterapia. 47. Eziologia, patogenesi, quadro clinico del morbo di Crohn Il morbo di Crohn è una malattia intestinale cronica con manifestazioni sistemiche; la cui base morfologica è l'infiammazione autoimmune granulomatosa del tratto gastrointestinale. Eziologia e patogenesi. L'eziologia e la patogenesi della malattia non sono ben comprese. I più popolari sono i concetti infettivi e immunitari dell'inizio della malattia. Negli ultimi anni sono stati segnalati il ruolo eziologico dei microrganismi del genere Yersinia. Tuttavia, è difficile stabilire se questi agenti microbici siano agenti patogeni o commensali. Allo stesso tempo, i cambiamenti nella microflora intestinale svolgono un ruolo importante nella patogenesi della malattia. Tipicamente, una diminuzione dei batteri di tipo bifidum con un contemporaneo aumento degli enterobatteri con segni di patogenicità. I meccanismi autoimmuni svolgono un ruolo nello sviluppo della malattia. Nella malattia di Crohn, gli autoanticorpi (lgC, lgM) compaiono contro i tessuti intestinali. Classificazione. Classificazione (FI Komarov, A. I. Kazanov, 1992). 1. Decorso: acuto; cronico. 2. Caratteristiche del processo: lesione all'interno dell'intestino tenue; lesione all'interno della regione ileocecale; lesione all'interno del colon. 3. Complicazioni: restringimento dell'intestino; dilatazione tossica del colon; fistole; amiloidosi; nefrolitiasi, colelitiasi; Anemia da carenza di vitamina B12. quadro clinico. Il quadro clinico della malattia di Crohn è caratterizzato da una notevole diversità, determinata dalla localizzazione e dall'estensione del processo patologico nell'intestino, dalla forma della malattia e dall'aggiunta di complicanze. Uno studio obiettivo presta attenzione al pallore della pelle, che è correlato alla gravità dell'anemia, al gonfiore delle gambe dovuto all'assorbimento ridotto e al metabolismo delle proteine. Alla palpazione dell'addome si notano flatulenza e brontolio. Durante l'esame obiettivo del paziente, vengono determinati il pallore della pelle, la condizione del subfebrile, la carenza di peso corporeo, la palpazione rivela le anse intestinali spasmodiche, il dolore nella zona paraombelicale, nella regione iliaca destra. Nella malattia di Crohn si notano segni extraintestinali della malattia: stomatite aftosa, flemmone e fistole del cavo orale, artrite, simile all'artrite reumatoide in clinica, con sintomi caratteristici di lesioni simmetriche delle piccole articolazioni, rigidità mattutina. Cambiamenti tipici negli occhi: irite, iridociclite, maculopatia. La pelle può sviluppare eritema nodoso e pioderma gangrenoso. La diarrea è caratterizzata da un aumento della frequenza delle feci fino a 10 volte al giorno o più, materia polifecale. Il volume delle feci è determinato dalla localizzazione anatomica del processo. La perdita di peso è nota in tutti i pazienti. 48. Diagnosi del morbo di Crohn Diagnosi e diagnosi differenziale. In un esame del sangue clinico durante un'esacerbazione, vengono rilevati leucocitosi, anemia e un aumento della VES. I cambiamenti nell'analisi generale delle urine appaiono in forma grave, caratterizzata dall'aggiunta di amiloidosi renale (proteinuria). Un esame del sangue biochimico rivela ipoproteinemia, ipoalbuminemia, aumento delle a-globuline, diminuzione del contenuto di ferro, vitamina B12, acido folico, zinco, magnesio e potassio. I dati dell'esame scatologico consentono di valutare indirettamente il livello della lesione. Nel coprogramma con localizzazione del processo nell'intestino tenue si trovano materia polifecale, steatorrea, creatorea; con colon - una miscela di muco, leucociti, eritrociti. La diagnostica a raggi X consente di stabilire la localizzazione e la prevalenza del processo patologico nell'intestino. Le aree dell'intestino interessato si alternano ad aree dell'intestino immodificato. Le anse alterate si irrigidiscono, il quadro è a mosaico con piccoli difetti di riempimento e con la penetrazione del contrasto oltre la parete intestinale sotto forma di tasche. L'intestino nella zona interessata acquisisce il carattere di finemente orlato, con la formazione di pseudodiverticoli. La capacità contrattile della parete intestinale si riduce o si perde completamente, l'evacuazione del bario rallenta. Si osserva un restringimento irregolare del lume intestinale, di conseguenza, diventa così stretto da assumere la forma di un pizzo. Sopra la zona di restringimento, l'intestino si espande. La diagnosi endoscopica è di importanza decisiva nella verifica della diagnosi. Per il morbo di Crohn, il più caratteristico è il cambiamento nell'antro dello stomaco e nella sezione iniziale del duodeno. Endoscopicamente, è possibile rilevare un restringimento circolare dell'antro, simile a una stenosi tumorale. Il periodo iniziale della malattia di Crohn è caratterizzato da scarsi dati endoscopici: una mucosa opaca, contro la quale sono visibili erosioni di tipo afte, circondata da granulazioni biancastre. Il pattern vascolare è assente o levigato. Nel lume dell'intestino e sulle sue pareti viene determinato il muco purulento. Nella remissione clinica, i cambiamenti descritti possono scomparire completamente. Con il progredire della malattia, la mucosa si ispessisce in modo non uniforme, assume un colore biancastro e si notano grandi fessure superficiali o profonde. Il lume intestinale si restringe, rendendo difficile l'avanzamento del colonscopio. La colonscopia consente di eseguire una biopsia mirata della mucosa in qualsiasi parte del colon e nell'ileo terminale. Nella malattia di Crohn, il processo patologico inizia nello strato sottomucoso, quindi la biopsia deve essere eseguita in modo tale che una parte dello strato sottomucoso entri nel materiale bioptico. In connessione con quanto sopra, nel 54% dei casi non viene rilevato il substrato morfologico della malattia. 49. Trattamento del morbo di Crohn Trattamento. Viene prescritta una dieta meccanicamente e chimicamente parsimoniosa con un alto contenuto di proteine, vitamine, microelementi, ad eccezione del latte se è intollerante, e la restrizione delle fibre vegetali grossolane. Viene mostrato l'uso di idrolizzati enterali liquidi. Salazopreparati e corticosteroidi costituiscono la base della terapia farmacologica patogenetica. La dose giornaliera di farmaci è di 3-6 g Con la localizzazione del processo patologico nell'intestino crasso, l'attività della sulfasalazina supera l'attività del prednisolone. In assenza dell'effetto dell'uso della sulfasalazina, con lesioni prevalentemente dell'intestino tenue e segni pronunciati di infiammazione immunitaria, nonché in presenza di manifestazioni sistemiche della malattia, è indicato l'uso di corticosteroidi. L'effetto del loro uso si nota nelle prime 8 settimane dall'inizio del trattamento. Il prednisolone è prescritto secondo il seguente schema: al culmine di un'esacerbazione, 60 mg al giorno, quindi la dose viene gradualmente ridotta e entro la 6-10a settimana viene regolata su una dose di mantenimento di 5-10 mg al giorno. Al raggiungimento della remissione clinica, il farmaco viene gradualmente cancellato. Se la remissione non viene raggiunta, il trattamento con prednisolone viene continuato in regime ambulatoriale fino a 52 settimane. Nel decorso grave della malattia, in caso di complicanze sotto forma di fistole rettovaginali, cutanee-enterali, entero-intestinali, la nomina di 6-mercaptopurina per via orale a 0,05 g 2-3 volte al giorno è indicata per 10 giorni corsi con un intervallo di 3 giorni fino alla remissione clinica. Successivamente, passano all'assunzione di dosi di mantenimento del farmaco durante l'anno. La dose di 6-mercaptopurina in questo caso è di 75 mg al giorno. L'effetto del trattamento con immunosoppressori può essere determinato non prima di 3-4 mesi. Il metronidazolo ha trovato un uso diffuso nel trattamento della malattia di Crohn, le cui principali indicazioni sono le fistole e le fessure perianali, la mancanza di effetto dei farmaci salazal e dei glucocorticoidi, nonché le ricadute della malattia dopo proctectomia. Il farmaco viene prescritto in una dose di 500-1000 mg al giorno. La durata del corso continuo non deve superare le 4 settimane. La terapia sintomatica per la malattia di Crohn si riduce alla prescrizione di brevi cicli (2-3 giorni) di farmaci antidiarroici (imodium, loperamide). Le dosi sono selezionate individualmente in base all'effetto clinico. I farmaci antidiarroici non dovrebbero essere prescritti per un lungo periodo (più di 5 giorni). A causa della presenza della sindrome da malassorbimento nella malattia di Crohn, i preparati enzimatici che non contengono acidi biliari (pancreatina, mezim-forte, solisim, somilasi) vengono utilizzati in una dose da 2 a 6 compresse ad ogni pasto. Secondo le indicazioni, l'anemia e l'ipoalbuminemia si correggono prescrivendo integratori di ferro (per via parenterale) e somministrando alvesina, idrolizzatori proteici, aminopeptide, aminocrovina. I multivitaminici sono prescritti in pillole e gli elementi essenziali in capsule. Il trattamento della disbiosi viene effettuato secondo le regole generali. 50. Classificazione della colite ulcerosa aspecifica La colite ulcerosa aspecifica è una malattia infiammatoria che colpisce la mucosa del colon con alterazioni ulcerative-distruttive, che ha un decorso cronico recidivante, spesso accompagnato dallo sviluppo di complicazioni potenzialmente letali. Classificazione (Yu. V. Baltaitis et al., 1986). Caratteristica clinica. 1. Forma clinica: 1) acuto; 2) cronico. 2. Corrente: 1) in rapido progresso; 2) continuamente recidivante; 3) ricorrente; 4) latente. 3. Grado di attività: 1) esacerbazione; 2) esacerbazione in dissolvenza; 3) remissione. 4. Gravità: 1) luce; 2) moderato; 3) pesante. Caratteristica anatomica. 1. Caratteristica macroscopica: 1) proctite: 2) proctosigmoidite; 3) lesione subtotale; 4) sconfitta totale. 2. Caratteristica microscopica: 1) la predominanza di processi distruttivi-infiammatori; 2) riduzione dei processi infiammatori con elementi di riparazione; 3) conseguenze del processo infiammatorio Complicazioni. 1. Locale: 1) sanguinamento intestinale; 2) perforazione del colon; 3) restringimento del colon; 4) pseudopoliposi; 5) infezione intestinale secondaria; 6) scomparsa della mucosa; 7) dilatazione tossica del colon; 8) malignità. 2. Generale: 1) ipocorticismo funzionale; 2) sepsi; 3) manifestazioni sistemiche - artrite, sacroileite, lesioni cutanee, irite, amiloidosi, flebite, colangite sclerosante, distrofia epatica. 51. Quadro clinico della colite ulcerosa quadro clinico. La clinica della colite ulcerosa è polimorfa e dipende dalla gravità del decorso e dalla gravità del processo. Il decorso del processo infiammatorio, considerato più spesso cronico, assume in alcuni casi un carattere acuto. Anche l'estensione della lesione del colon può variare. La colite ulcerosa è caratterizzata da 3 sintomi principali: il rilascio di sangue scarlatto durante i movimenti intestinali, funzionalità intestinale compromessa e dolore addominale. La disfunzione intestinale si manifesta sotto forma di disturbi di feci instabili ripetute, che è il risultato di un ampio danno alla mucosa e di una diminuzione dell'assorbimento di acqua e sali. Molto spesso, la diarrea si verifica con una grave colite ulcerosa. Tuttavia, la diarrea non è un indicatore affidabile della gravità del processo. La gravità della diarrea in combinazione con la presenza di sangue rosso nelle feci è importante. In un numero significativo di pazienti con colite ulcerosa, sangue e muco si trovano periodicamente sulla superficie delle feci formate, che è spesso erroneamente considerata una manifestazione di emorroidi. Il decorso lieve della colite ulcerosa non specifica è caratterizzato da una condizione soddisfacente dei pazienti. Il dolore addominale è moderato e di breve durata. La sedia è decorata, accelerata, fino a 2-3 volte al giorno. Nelle feci si trovano sangue e muco. Il processo è localizzato all'interno del retto e del colon sigmoideo. Il decorso clinico è ricorrente. L'effetto del trattamento con salazopreparati è soddisfacente. Le ricadute si verificano non più di 2 volte l'anno. Le remissioni possono essere lunghe (più di 2-3 anni). Il decorso moderato della malattia viene diagnosticato se il paziente ha la diarrea. La sedia è frequente (fino a 6-8 volte al giorno), in ciascuna porzione è visibile una miscela di sangue e muco. I dolori crampi all'addome sono più intensi. Ci sono febbre intermittente con aumento della temperatura corporea fino a 38 C, intensa debolezza generale. Si possono anche notare manifestazioni extraintestinali della malattia (artrite, uveite, eritema nodoso). Il corso è continuamente ricorrente, l'effetto dei salazopreparati è instabile, gli ormoni vengono prescritti durante le esacerbazioni. La forma grave della malattia è caratterizzata da un esordio acuto. Una lesione totale dell'intestino crasso si sviluppa rapidamente con la diffusione del processo patologico in profondità nella parete intestinale. Le condizioni del paziente peggiorano drasticamente. La clinica è caratterizzata da un esordio improvviso, febbre alta, diarrea profusa fino a 24 volte al giorno, sanguinamento intestinale abbondante e un rapido aumento della disidratazione. Appare tachicardia, diminuzione della pressione sanguigna, aumento delle manifestazioni extraintestinali di colite ulcerosa aspecifica. Il trattamento conservativo non è sempre efficace e spesso è necessario un intervento chirurgico d'urgenza. 52. Diagnosi di colite ulcerosa aspecifica Diagnosi e diagnosi differenziale. Negli esami del sangue clinici con una forma lieve della malattia, una leggera leucocitosi neutrofila, un aumento della VES e l'emocromo non vengono modificati. All'aumentare della gravità del decorso e della durata dell'esacerbazione, si verifica un'anemia di genesi mista (carente di B12 e carente di ferro) e la VES aumenta. Nell'analisi biochimica del sangue nelle forme moderate e gravi si notano disproteinemia, ipoalbuminemia, ipergammaglobulinemia, squilibrio elettrolitico e stato acido-base. Nell'analisi generale delle urine, i cambiamenti compaiono solo quando si verificano complicazioni sotto forma di sindrome nefrosica sullo sfondo dell'amiloidosi, quando si notano cambiamenti caratteristici nei test delle urine - proteinuria, sedimento urinario "morto", c'è anche un aumento del sangue e il livello di creatinina, urea. Il ruolo principale nella diagnosi è acquisito dall'esame endoscopico con biopsia mirata, poiché nella colite ulcerosa aspecifica è colpita principalmente la mucosa del colon. Il retto è sempre coinvolto nel processo patologico, cioè durante l'endoscopia vengono rilevati cambiamenti erosivi e ulcerativi immediatamente dietro lo sfintere anale durante la sigmoidoscopia. Nella colite ulcerosa, non è sempre possibile superare la flessura rettosigmoidea a causa di un forte spasmo. Un tentativo di tenere il tubo del proctoscopio è accompagnato da un forte dolore. In questa situazione, il proctoscopio deve essere inserito a una profondità non superiore a 12-15 cm. L'immagine endoscopica dipende dalla forma della malattia. Con una forma lieve, sono visibili una membrana mucosa opaca edematosa, spessi strati biancastri di muco sulle pareti dell'intestino e un leggero sanguinamento da contatto. Il pattern vascolare dello strato sottomucoso non è determinato visivamente. Con un decorso moderato della malattia, si rilevano iperemia ed edema della mucosa, gravi emorragie da contatto, emorragie, erosioni e ulcere di forma irregolare, spessi strati di muco sulle pareti dell'intestino. In un decorso grave della malattia, la membrana mucosa del colon viene distrutta in misura considerevole. Si trovano una superficie interna granulare sanguinante, estese aree di ulcerazione con depositi fibrinosi, pseudopolipi di varie dimensioni e forme, pus e sangue nel lume intestinale. Le controindicazioni per la colonscopia e la sigmoidoscopia sono forme gravi di colite ulcerosa nella fase acuta della malattia. In presenza di un'epidemia di infezioni intestinali, la diagnosi è facilmente stabilita. Ma anche nel caso di morbilità sporadica nelle infezioni intestinali acute, la sindrome della colite scorre senza ricadute, mentre la colite ulcerosa ha un decorso recidivante. I metodi più accurati per identificare l'infezione intestinale acuta includono batteriologico e sierologico. 53. Trattamento della colite ulcerosa aspecifica Trattamento. L'assenza di un singolo fattore eziologico e la complessità della patogenesi della colite ulcerosa aspecifica rendono difficile il trattamento di questa malattia. Vengono utilizzati farmaci antinfiammatori e antibatterici: salazopiridazina, sulfasalazina, salazodimetossina, salofalk. La sulfasalazina ingerita, con la partecipazione della microflora intestinale, si scompone in acido 5-aminosalicilico e sulfapiridina. La sulfapiridina non assorbita inibisce la crescita della microflora anaerobica nell'intestino, inclusi clostridi e batterioidi. E grazie all'acido 5-amino-salicilico, il farmaco non solo provoca cambiamenti nella microflora intestinale, ma modula anche le risposte immunitarie, blocca i mediatori del processo infiammatorio. Il farmaco viene prescritto alla dose di 2-6 g al giorno per l'intero periodo di infiammazione attiva. Quando la sindrome della colite scompare, la dose di sulfasalazina viene ridotta gradualmente, portandola a una dose di mantenimento (una media di 1-1,5 compresse al giorno). Nella sindrome diarroica grave in individui con malattia da lieve a moderata, è indicata la nomina di sandostatina, che inibisce la sintesi di ormoni gastrointestinali e ammine biogene (peptide intestinale vasoattivo, gastrina, serotonina), la cui produzione è fortemente aumentata nella colite ulcerosa e Morbo di Crohn. E anche il farmaco riduce la secrezione e migliora l'assorbimento nell'intestino, inibisce il flusso sanguigno viscerale e riduce la motilità. Quando si utilizza la sandostatina (entro 7 giorni alla dose di 0,1 mg 2 volte, per via sottocutanea), la diarrea diminuisce, il tenesmo praticamente scompare e l'escrezione di sangue con le feci diminuisce. In una forma grave di colite ulcerosa aspecifica, il trattamento viene effettuato sullo sfondo della nutrizione parenterale. Il contenuto proteico in queste preparazioni dovrebbe essere di circa 1,5-2,0 g/kg di peso corporeo. I corticosteroidi, che vengono somministrati per via parenterale, sono un trattamento patogenetico per una forma grave della malattia: durante il primo giorno, il prednisone viene somministrato per via endovenosa a intervalli di 12 ore (90-120 mg o più), nei successivi 5 giorni - per via intramuscolare, riducendo gradualmente la dose. Con un effetto positivo, passano ai farmaci per via orale (prednisolone 40 mg al giorno). Nella forma moderata del decorso dell'ulcera ulcerosa non specifica, è necessaria una dieta rigorosa con una restrizione di fibre, latticini e un alto contenuto proteico. Il prednisolone viene somministrato per via orale ad una dose iniziale di 20-40 mg al giorno. Il trattamento può essere integrato con sulfasalazina e suoi analoghi, che vengono assunti per via orale o somministrati in microclisteri e supposte nel retto. La dose iniziale di sulfasalazina è di 1 g al giorno, quindi viene aumentata a 4-6 g. Come metodo ausiliario di trattamento, possono essere utilizzati decotti di erbe con effetti antinfiammatori ed emostatici (radice di bruciacchia, foglia di ortica, lichene, pigne di ontano grigio, radice di liquirizia), la fitoterapia spesso consente di ridurre la dose di salazopreparati, prolungare remissione. 54. Quadro clinico della gromerulonefrite acuta La glomerulonefrite acuta (AGN) è una malattia renale diffusa acuta di natura infettiva-allergica, localizzata nei glomeruli. L'AGN può essere una malattia indipendente (primaria) o essere secondaria come parte di un'altra malattia, complicando il quadro clinico e la diagnosi di quest'ultima. L'AGN di solito colpisce uomini giovani e di mezza età. quadro clinico. Il quadro clinico della malattia è costituito dalle seguenti sindromi. sindrome urinaria. 1. Proteinuria dovuta al passaggio di molecole proteiche attraverso gli spazi della parete capillare del glomerulo, formati durante la deposizione di immunocomplessi su di essi. La proteinuria è di natura selettiva, in cui prevalentemente le albumine passano attraverso il "filtro" glomerulare. 2. Ematuria dovuta al coinvolgimento nel processo patologico del mesangio capillare e del tessuto interstiziale. Gli eritrociti penetrano attraverso le più piccole rotture della membrana basale, cambiando la loro forma. 3. Cilindruria - escrezione urinaria di cellule cilindriche dei tubuli. Durante i processi distrofici nei tubuli delle cellule disintegrate dell'epitelio renale, si formano cilindri granulari, costituiti da una massa granulare densa; i cilindri cerosi hanno contorni netti e una struttura omogenea; i calchi ialini sono formazioni proteiche. La sindrome ipertensiva si osserva a causa di: 1) ritenzione di sodio e acqua; 2) attivazione dei sistemi renina-angiotensina-aldosterone e simpatico surrenale; 3) diminuzione della funzione del sistema depressore dei reni. La sindrome dell'edema è associata ai seguenti fattori: 1) una diminuzione della filtrazione glomerulare dovuta alla loro sconfitta; 2) una diminuzione della carica di filtrazione del sodio e un aumento del suo riassorbimento; 3) ritenzione idrica dovuta alla ritenzione di sodio nel corpo; 4) un aumento delle BCC; 5) iperaldosteronismo secondario; 6) un aumento della secrezione di ADH e un aumento della sensibilità del nefrone distale ad esso, con conseguente ritenzione di liquidi; 7) un aumento della permeabilità delle pareti capillari e il rilascio di plasma nei tessuti; 8) una diminuzione della pressione oncotica plasmatica con proteinuria massiva. 55. Diagnosi di gromerulonefrite acuta Diagnostica. Nel 100% dei casi, agli esami delle urine viene diagnosticata proteinuria di varia gravità, cilindruria e, soprattutto per la diagnosi, ematuria di varia gravità - dalla microematuria (fino a 10 eritrociti per campo visivo) alla macroematuria (sebbene piuttosto rara). Tuttavia, se si sospetta l'AGN, è necessario eseguire una serie di test delle urine ripetuti o eseguire un test di Nechiporenko (determinazione del numero di elementi formati in 1 μl), poiché gli eritrociti potrebbero non essere rilevati in una singola porzione di urina. Nello studio del sangue vengono rilevati indicatori di fase acuta (aumento del contenuto di fibrinogeno e a2-globulina, proteina C-reattiva, accelerazione della VES), il numero di leucociti cambia poco, moderata anemia. Con un decorso semplice di AGN, il contenuto di sostanze azotate (creatinina, indican, urea) nel sangue non cambia. Nella fase iniziale della malattia si osserva un cambiamento nel test di Reberg: una diminuzione della filtrazione glomerulare e un aumento del riassorbimento tubulare, che si normalizza man mano che si riprende. Un esame radiografico in pazienti con grave ipertensione arteriosa può mostrare un moderato aumento del ventricolo sinistro, che assume le stesse dimensioni del paziente che si riprende. Esistono 3 varianti cliniche di AGN. 1. Variante monosintomatica: disturbi minori, assenza di edema e ipertensione arteriosa, c'è solo sindrome urinaria; la variante più comune del decorso della malattia (86% dei casi). 2. Variante nefrosica: edema, oliguria sono pronunciati, è possibile aumentare la pressione sanguigna a numeri relativamente bassi, viene rilevato nell'8% dei pazienti. 3. Versione estesa: ipertensione arteriosa, che raggiunge numeri elevati (180/100 mm Hg), edema moderatamente pronunciato, insufficienza circolatoria, si verifica nel 6% dei casi. 56. Trattamento della gromerulonefrite acuta Trattamento. Il trattamento per l'AGN è complesso e comprende le seguenti attività. 1. Modalità. Se si sospetta AGN o immediatamente dopo che è stata stabilita la diagnosi, il paziente deve essere immediatamente ricoverato in ospedale. Il rigoroso riposo a letto deve essere osservato per circa 2-4 settimane fino all'eliminazione dell'edema e alla normalizzazione della pressione sanguigna. Stare a letto fornisce un riscaldamento uniforme del corpo, che porta ad una diminuzione del vasospasmo (quindi, ad una diminuzione della pressione sanguigna) e ad un aumento della filtrazione glomerulare e della diuresi. Dopo la dimissione dall'ospedale, il trattamento domiciliare è indicato per un massimo di 4 mesi dalla data di insorgenza della malattia, che è la migliore prevenzione del passaggio dell'AGN allo stadio cronico. 2. Dieta. A seconda della gravità dei sintomi clinici, è molto importante limitare i liquidi e il cloruro di sodio. Con una forma espansa e nefrosica, si consiglia un digiuno completo per 1-2 giorni con assunzione di liquidi in quantità pari alla diuresi. Il 2-3° giorno viene mostrato il consumo di alimenti ricchi di sali di potassio (porridge di riso, patate). La quantità totale di acqua bevuta al giorno dovrebbe essere uguale al volume di urina escreto nel giorno precedente più 300-500 ml. Dopo 3-4 giorni, il paziente viene trasferito a una dieta con restrizione proteica (fino a 60 g al giorno) e la quantità totale di sale non supera i 3-5 g / giorno. Tale dieta è raccomandata fino alla scomparsa di tutti i sintomi extrarenali e un netto miglioramento del sedimento urinario. 3. La terapia farmacologica comprende principalmente la terapia antibiotica, che, tuttavia, dovrebbe essere eseguita solo se la natura infettiva dell'AGN è accertata in modo affidabile (l'agente patogeno è stato isolato e non sono trascorse più di 3 settimane dall'inizio della malattia). Solitamente prescritto penicillina o suoi analoghi semisintetici in dosaggi convenzionali. Anche la presenza di focolai evidenti di infezione cronica (tonsillite, sinusite, ecc.) è un'indicazione diretta per la terapia antibiotica. I diuretici nel trattamento dell'AGN sono indicati solo con ritenzione di liquidi, aumento della pressione sanguigna e comparsa di insufficienza cardiaca. La furosemide più efficace (40-80 mg), utilizzata fino all'eliminazione di edemi e ipertensione. Non è necessaria una prescrizione a lungo termine di questi farmaci, sono sufficienti 3-4 dosi. In assenza di edema, ma ipertensione persistente o con insufficiente effetto antipertensivo dei saluretici, vengono prescritti farmaci antipertensivi (clophelin, dopegyt) con una durata di somministrazione che dipende dalla persistenza dell'ipertensione arteriosa. Con proteinuria prolungata, l'indometacina o il voltaren vengono prescritti a 75-150 mg al giorno (in assenza di ipertensione e oliguria). La prognosi è favorevole, tuttavia, con forme prolungate, c'è la possibilità che il processo diventi cronico. La prevenzione dell'AGN si riduce al trattamento efficace dell'infezione focale, all'indurimento razionale. Al fine di rilevare tempestivamente l'insorgenza della malattia dopo la vaccinazione, trasferita la SARS in tutti i pazienti, è necessario esaminare le urine.
▪ Teoria del governo e dei diritti. Note di lettura ▪ Storia della psicologia. Note di lettura
Pelle artificiale per l'emulazione del tocco
15.04.2024 Lettiera per gatti Petgugu Global
15.04.2024 L'attrattiva degli uomini premurosi
14.04.2024
▪ Robot insetti con motori a ioni ▪ Spermatozoo artificiale creato ▪ Nuovo multimetro digitale FLUKE 87V ▪ Batteria ad acqua per veicoli elettrici
▪ sezione del sito Grande Enciclopedia per bambini e adulti. Selezione dell'articolo ▪ articolo In parole povere, ma usando un eufemismo. Espressione popolare ▪ articolo Quali uccelli trascorrono la maggior parte della loro vita in volo? Risposta dettagliata ▪ articolo Motore antigoccia. Trasporto personale ▪ articolo Cubo e due fazzoletti. Messa a fuoco segreta
Homepage | Biblioteca | Articoli | Mappa del sito | Recensioni del sito www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese





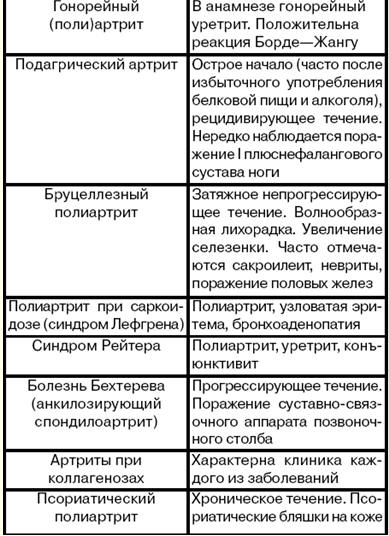
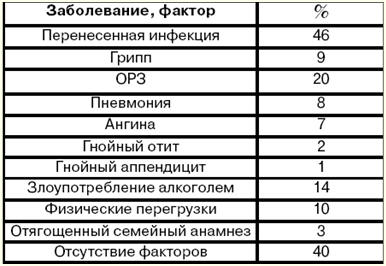
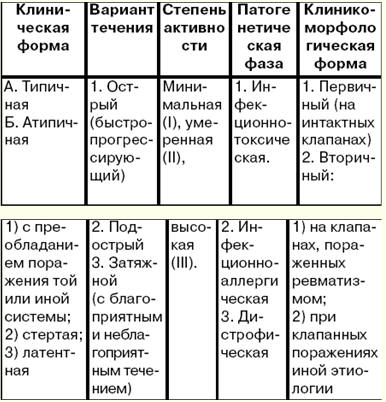
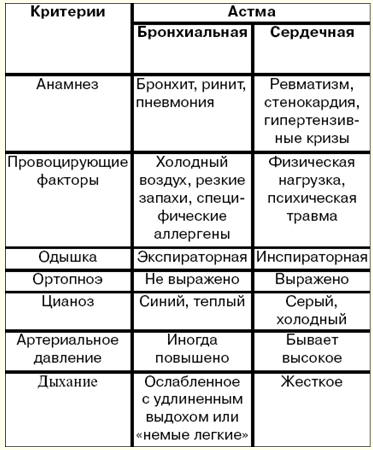

 Vedi altri articoli sezione
Vedi altri articoli sezione 