
|
|
Appunti delle lezioni, cheat sheet
Anestesiologia e rianimazione. Cheat sheet: in breve, il più importante
Elenco / Appunti delle lezioni, cheat sheet Sommario
1. Il concetto di rianimazione La rianimazione è una branca della medicina clinica che studia i problemi di rivitalizzazione del corpo, sviluppando principi per la prevenzione delle condizioni terminali, metodi di rianimazione e terapia intensiva. I metodi pratici per rivitalizzare il corpo sono accomunati dal concetto di "rianimazione". La rianimazione (dal latino "revival" o "animazione") è un sistema di misure volte a ripristinare le funzioni vitali del corpo gravemente alterate o perse e rimuoverlo da uno stato terminale e dalla morte clinica. Misure efficaci di rianimazione sono il massaggio cardiaco indiretto e la ventilazione artificiale dei polmoni. Se sono inefficaci entro 30 minuti, viene accertata la morte biologica. La terapia intensiva è un insieme di misure utilizzate per trattare condizioni gravi e pericolose per la vita e prevede l'uso di un'ampia gamma di misure terapeutiche, secondo le indicazioni, comprese le infusioni endovenose, la ventilazione meccanica prolungata, il pacing elettrico, i metodi di dialisi, ecc. Uno stato critico è l'impossibilità di mantenere l'integrità delle funzioni corporee a seguito di una disfunzione acuta di un organo o sistema, che richiede la sostituzione di farmaci o hardware-strumentali. Lo stato terminale è uno stato di confine tra la vita e la morte, un'estinzione reversibile delle funzioni corporee, comprese le fasi di preagonia, agonia e morte clinica. La morte clinica è una condizione terminale in cui non c'è circolazione sanguigna e respirazione, l'attività della corteccia cerebrale si interrompe, ma i processi metabolici sono preservati. Con la morte clinica, rimane la possibilità di una rianimazione efficace. La durata della morte clinica va da 5 a 6 minuti. La morte biologica è una cessazione irreversibile dei processi fisiologici negli organi e nei tessuti, in cui la rianimazione è impossibile. È stabilito da una combinazione di una serie di segni: assenza di movimenti spontanei, contrazioni del cuore e del polso nelle grandi arterie, respirazione, reazioni a stimoli dolorosi, riflesso corneale, massima dilatazione della pupilla e assenza della loro reazione alla luce. Segni affidabili dell'inizio della morte sono una diminuzione della temperatura corporea a 20 C, la comparsa di macchie da cadavere e rigor mortis muscolare. 2. Manipolazioni di base in terapia intensiva Puntura percutanea e cateterizzazione della vena principale (succlavia). Indicazioni: grandi volumi di terapia infusionale-trasfusionale, nutrizione parenterale, terapia di disintossicazione, terapia antibiotica endovenosa, sondaggio e contrasto del cuore, misurazione della CVP, impianto di un pacemaker, impossibilità di cateterizzazione delle vene periferiche. Controindicazioni: violazione del sistema di coagulazione del sangue, processo infiammatorio e purulento nel sito di puntura e cateterizzazione, trauma nella clavicola, sindrome della vena cava superiore, sindrome di Paget-Schretter. Strumentazione e accessori per puntura e cateterizzazione: ago da puntura, un set di cateteri in plastica, un set di conduttori, una siringa da 10 ml per iniezioni intramuscolari, forbici, un porta aghi, un ago chirurgico e una legatura di seta, un cerotto adesivo. Tecnica: la cateterizzazione viene eseguita nel rispetto delle regole di asepsi e antisepsi, trattamento delle mani dell'operatore, campo operatorio e avvolgimento con materiale sterile. La posizione del paziente è orizzontale sulla schiena con le braccia portate al corpo e il bavero della testa nella direzione opposta. Viene utilizzata l'anestesia locale: soluzione di novocaina allo 0,5-1%. La puntura viene eseguita meglio a destra, poiché quando si perfora la vena succlavia sinistra c'è il rischio di danneggiare il dotto linfatico toracico. Punto di puntura - sul bordo del terzo interno e medio della clavicola 2 cm sotto di essa. L'ago viene fatto passare lentamente con un angolo di 45 alla clavicola e 30-40 alla superficie del torace tra la clavicola e la 15a costola in direzione del bordo superiore dell'articolazione sternoclavicolare. Quando si passa l'ago, il pistone della siringa viene periodicamente serrato per determinare se entra nella vena e la novocaina viene iniettata lungo l'ago. Quando si perfora una vena, a volte c'è una sensazione di fallimento. Dopo essere entrati nella vena, la siringa viene scollegata dall'ago e la cannula viene chiusa con un dito. Quindi un conduttore viene inserito attraverso l'ago per una lunghezza di 20-6 cm e l'ago viene rimosso. Un catetere del diametro appropriato viene fatto passare attraverso il conduttore e, insieme al conduttore, viene inserito nella vena di 8-2 cm, dopodiché il conduttore viene accuratamente rimosso. Per controllare la posizione corretta del catetere, viene attaccata una siringa e vi vengono aspirati 3-3 ml di sangue, dopodiché viene posizionato un tappo o viene avviata la terapia per infusione. Il catetere viene fissato alla pelle con una legatura di seta. Per fare questo, viene praticata una manica di cerotto adesivo sul catetere a 5-XNUMX mm dalla pelle, su cui è legata la seta, quindi passata attraverso le orecchie del catetere e legata di nuovo. Dopo aver fissato il catetere, il sito di puntura viene chiuso con un adesivo asettico. Complicanze: puntura dell'arteria succlavia, embolia gassosa, puntura della cavità pleurica, danno al plesso brachiale, danno al dotto linfatico toracico, danno alla trachea, al gozzo e alla tiroide, suppurazione nel sito della puntura. 3. Tracheostomia. Conicostomia Tracheotomia Indicazioni: ostruzione della laringe e della trachea superiore per ostruzione da tumore o corpo estraneo, paralisi e spasmo delle corde vocali, grave gonfiore della laringe, distress respiratorio acuto, aspirazione del vomito, prevenzione dell'asfissia in gravi lesioni toraciche. Strumenti: 2 bisturi, 2 pinzette anatomiche e chirurgiche, diverse pinze emostatiche, un elevatore, una sonda scanalata, 2 uncini affilati smussati e 1 a dente singolo, dilatatore Trousseau o Deschamps, aghi chirurgici con porta aghi. Tecnica. Il paziente giace sulla schiena, un rullo sotto le spalle, la testa è gettata all'indietro. Se il paziente è in stato di asfissia, il rullo viene posizionato solo all'ultimo momento, prima di aprire la trachea. L'anestesia per infiltrazione locale viene eseguita con una soluzione allo 0,5-1% di novocaina con l'aggiunta di adrenalina. Nell'asfissia acuta è possibile operare senza anestesia. Punti di identificazione: l'angolo della cartilagine tiroidea e il tubercolo dell'arco della cartilagine cricoidea. Un'incisione della pelle, del tessuto sottocutaneo e della fascia superficiale viene praticata dal bordo inferiore della cartilagine tiroidea all'incisura giugulare rigorosamente lungo la linea mediana del collo. La vena mediana del collo viene retratta o legata, trovando una linea bianca, lungo la quale i muscoli vengono spinti in modo smussato e l'istmo della tiroide è esposto. I bordi dell'incisione vengono allontanati con un dilatatore Trousseau, si applicano legature sul bordo della ferita e si inserisce con cura la cannula tracheostomica, assicurandosi che la sua estremità entri nel lume della trachea. La ferita chirurgica viene suturata. Il tubo viene fissato al collo del paziente con una stecca di garza, precedentemente legata alla protezione del tubo. Inserire la camera d'aria nella camera d'aria. Conicostomia Il paziente viene posto sulla schiena con un rullo trasversale a livello delle scapole. La testa del paziente è inclinata all'indietro. La laringe è fissata con le dita sulle superfici laterali della cartilagine tiroidea e si sente lo spazio tra la tiroide e la cartilagine cricoidea, dove si trova il legamento a forma di cono. In anestesia locale per infiltrazione con bisturi appuntito, viene praticata un'incisione cutanea trasversale lunga circa 2 cm, il legamento conico viene palpato e sezionato o perforato. L'eventuale cannula tracheostomica di diametro adeguato viene inserita nel foro ricavato e fissata con una fascia di garza attorno al collo. In assenza di cannula, può essere sostituita da un pezzo di tubo di gomma o plastica di diametro e lunghezza adeguati. Per evitare che questo tubo scivoli nella trachea, la sua estremità esterna viene forata trasversalmente a una distanza di 2 cm dal bordo e fissata con una striscia di garza. Il conicotomo è una cannula per tracheostomia in metallo di piccolo diametro con un mandrino perforante al suo interno. Dopo la dissezione della pelle sul legamento a forma di cono, viene perforato con un conicotomo, il mandrino viene rimosso e la cannula viene posizionata in una posizione che garantisca il libero flusso d'aria nella trachea e fissata. 4. Intubazione tracheale Indicazioni: restringimento della laringe, respirazione patologica, insufficienza respiratoria acuta, coma II e III grado, alto rischio di aspirazione durante interventi chirurgici sugli organi del torace e della cavità addominale, testa e collo, nelle malattie della faringe, della laringe e della trachea (infiammazione acuta, cancro, tubercolosi e così via). Un laringoscopio viene utilizzato per l'intubazione. È composto da un manico e una lama. Le lame curve più utilizzate, in quanto più fisiologiche. Le lame dritte sono utilizzate con un collo lungo. La preparazione per l'intubazione comprende il controllo dell'attrezzatura e il corretto posizionamento del paziente. Il tubo endotracheale deve essere controllato. Il bracciale viene testato gonfiandolo con una siringa da 10 ml. Controllare il contatto della lama con l'impugnatura del laringoscopio e la lampadina. È necessario assicurarsi che l'aspirazione sia pronta in caso di espettorato improvviso, sanguinamento o vomito. Il successo dell'intubazione dipende dalla posizione corretta del paziente. La testa del paziente dovrebbe essere a livello del processo xifoideo dell'intubatore. Un moderato sollevamento della testa con estensione simultanea dell'articolazione atlanto-occipitale crea una posizione migliore per l'intubazione. La preparazione per l'intubazione include anche la pre-ossigenazione obbligatoria. Il laringoscopio viene tenuto nella mano non dominante (per la maggior parte delle persone, questa è la sinistra) e la bocca del paziente viene spalancata con l'altra mano. La lama viene inserita lungo il lato destro dell'orofaringe, evitando danni ai denti. La lingua è spostata a sinistra e la lama è sollevata fino all'arco della faringe. La punta di una lama curva viene inserita nella vallecula (una fossa situata sulla superficie anteriore dell'epiglottide), mentre la punta di una lama dritta dovrebbe sollevare direttamente l'epiglottide. L'impugnatura del laringoscopio viene spinta in alto e in avanti perpendicolarmente alla mandibola fino a quando non si vedono le corde vocali. La dipendenza dai denti dovrebbe essere evitata. Il tubo endotracheale viene prelevato con la mano destra e fatto passare attraverso la glottide aperta sotto controllo visivo. Il bracciale deve essere posizionato nella trachea superiore, ma sotto la laringe. Il laringoscopio viene rimosso dalla bocca, sempre per evitare danni ai denti. Immediatamente dopo l'intubazione, l'auscultazione viene eseguita sui polmoni su entrambi i lati (poiché è possibile far passare un tubo in un bronco) e nell'epigastrio (per escludere l'intubazione esofagea). Se il tubo è nella trachea, viene fissato in posizione con nastri e il bracciale viene gonfiato. La cuffia deve essere posizionata al di sopra del livello della cartilagine cricoidea, poiché una lunga permanenza nella laringe può portare a raucedine nel periodo postoperatorio. Complicanze: intubazione dell'esofago, bronco, localizzazione della cuffia nella laringe, danno ai denti, lussazione della mascella inferiore, laringospasmo, disturbi dei riflessi (ipertensione, tachicardia, aumento della pressione intracranica), trauma delle vie respiratorie, infiammazione, ecc. 5. Puntura e cateterizzazione dello spazio epidurale Indicazioni: sindrome del dolore grave, interventi chirurgici, analgesia postoperatoria. Il livello di impostazione del blocco epidurale dipende da quale organo deve essere anestetizzato. Livelli della colonna vertebrale e "organi bersaglio" in anestesia epidurale
Strumentazione: aghi per anestesia, un ago speciale per la perforazione dello spazio epidurale, una siringa per campioni, un catetere, un tappo, sfere filtranti, tovaglioli, nastro adesivo e guanti sterili. La posizione del paziente è seduto o sdraiato su un fianco. In questo caso, le ginocchia e il mento dovrebbero essere avvicinati il più possibile al petto. Pertanto, viene creata la massima flessione della colonna vertebrale, alla quale aumenta l'angolo tra i processi spinosi delle vertebre adiacenti e viene facilitato l'approccio al legamento giallo. In condizioni asettiche e in anestesia locale con una soluzione allo 0,5% di novocaina, viene eseguita una puntura dello spazio epidurale. L'ago viene iniettato rigorosamente perpendicolarmente, ma con l'osteocondrosi è possibile un angolo di inclinazione o durante la puntura nella regione medio-toracica. Quando l'ago entra nello spessore dei legamenti, il mandrino viene rimosso da esso e viene attaccata una siringa con liquido. L'ulteriore avanzamento dell'ago viene effettuato lentamente e senza intoppi premendo sullo stantuffo della siringa. A causa della notevole resistenza dei legamenti, il liquido non può lasciare la siringa. La siringa è scollegata e il catetere è inserito a 5-7 cm, non dovrebbe esserci resistenza. L'ago viene rimosso e il filo guida viene fissato alla schiena con cerotto adesivo, portandolo sulla superficie anteriore del torace. La spina con il filtro è fissata al conduttore. Viene iniettato un anestetico. Successivamente, viene determinato il livello di anestesia cutanea. Complicanze: disturbi respiratori ed emodinamici, intossicazione, danno alla dura madre, complicanze neurologiche, peridurite. 6. Violazioni affilate di coscienza La coscienza è la più alta forma di riflessione della realtà, che è un insieme di processi mentali che consentono a una persona di navigare nel mondo che lo circonda, il tempo, la propria personalità, che assicura il suo comportamento. La compromissione della coscienza è il nome generico per i disturbi dell'attività integrale del cervello, espressi in una violazione della capacità di percepire, comprendere e rispondere adeguatamente all'ambiente, navigarlo, ricordare gli eventi attuali, stabilire un contatto vocale ed eseguire espedienti arbitrari atti comportamentali. Esistono varie opzioni per l'oppressione della coscienza (stupore, stupore, coma di varie profondità), nonché per la confusione acuta (stato delirante o encefalopatia metabolica). Il grado di alterazione della coscienza varia da lieve confusione al coma e non ci sono chiare transizioni tra questi stati. In pratica, il grado di alterazione della coscienza è determinato dalla reazione del paziente agli stimoli. Lo stupore è una forma di coscienza alterata, caratterizzata da letargia, rallentamento e difficoltà nel corso dei processi mentali, rapido esaurimento dell'attenzione, aumento della soglia per la percezione degli stimoli esterni, ma pur mantenendo un contatto verbale limitato. Lo stupore si basa su una violazione dell'attenzione, ovvero la capacità di selezionare le informazioni necessarie e coordinare le risposte in modo tale che la sequenza logica di pensieri e azioni non venga violata. Le cause più comuni di stupore sono disordini metabolici e tossici, ma a volte si osserva anche con lesioni focali della corteccia, in particolare il lobo parietale destro. In tali pazienti, è possibile ottenere una risposta monosillabica o l'attuazione delle istruzioni più semplici solo dopo un appello persistente ad esso o una stimolazione aggiuntiva. Con un'ulteriore oppressione della coscienza, la possibilità di contatto vocale viene persa e si sviluppa il sopor. Il sopor è uno stato di profonda depressione della coscienza con la perdita della possibilità di contatto con il paziente, ma il mantenimento di reazioni protettive coordinate e l'apertura degli occhi del paziente in risposta al dolore, al suono o ad altri stimoli. Il paziente non può essere completamente svegliato anche con l'aiuto di stimoli dolorosi, giace con gli occhi chiusi. La reazione alle istruzioni verbali è debole o completamente assente, è impossibile ottenere una parola o un suono di risposta dal paziente. Con un'ulteriore oppressione della coscienza, si sviluppa il coma. Il coma è uno stato inconscio caratterizzato da insensibilità agli stimoli esterni. Questo è uno stato di depressione pericolosa per la vita delle funzioni del sistema nervoso centrale e disturbi della regolazione delle funzioni vitali. Il coma può essere causato da diversi disturbi metabolici e danni strutturali. 7. Esame di un paziente in coma Il piano di esame del paziente è il seguente. 1. Valutazione dello stato funzionale dell'apparato respiratorio e cardiovascolare. 2. Esami clinici generali, tenendo conto dei dati di laboratorio, che consentono di valutare la patologia extracranica. 3. Esame neurologico. Studi di laboratorio: analisi del sangue clinica generale (segni di un'infezione batterica o virale); analisi del sangue biochimiche: glucosio, fattori della coagulazione (tempo di coagulazione, protrombina, fibrinogeno, APTT, antitrombina III, test di paracoagulazione, conta piastrinica), urea, creatinina, bilirubina, ALT, AST, osmolarità, elettroliti (K, Na, Mg, Ca) ; screening tossicologico di sangue, urina, contenuto gastrico. Studi strumentali: radiografia del cranio e del rachide cervicale. La consultazione di un neuropatologo (neurochirurgo) determina l'ulteriore direzione della ricerca diagnostica: risonanza magnetica o computerizzata; EEG; dopplerografia ad ultrasuoni. La puntura lombare con analisi del liquido cerebrospinale è obbligatoria dopo: 1) consultazione di un oftalmologo ed esclusione dei segni di aumento della pressione intracranica - edema ed elevazione dei dischi ottici; 2) esclusione dei segni di ernia cerebrale. Si distinguono le seguenti localizzazioni dell'ernia cerebrale. Ernia diencefalica, che si verifica quando la localizzazione sopratentoriale mediale è danneggiata e consiste nello spostamento del diencefalo attraverso l'incavo del tenone cerebellare. Questo processo chiama: 1) respirazione di Cheyne-Stokes; 2) costrizione delle pupille pur mantenendo la loro reazione alla luce; 3) paralisi dello sguardo in alto; 4) cambiamenti nello stato mentale. L'ernia delle parti mediali del lobo temporale, che si manifesta quando è interessata la localizzazione sovratentoriale laterale, consiste nello spostamento delle parti mediali del lobo temporale attraverso l'incavo del tenone cerebellare. La pressione risultante sulle strutture del mesencefalo si manifesta con: 1) coscienza alterata; 2) una pupilla allargata e non reattiva sul lato dell'ernia, che è associata alla compressione del III nervo cranico; 3) emiparesi sul lato opposto. I movimenti dei bulbi oculari non sono sempre disturbati. Ernia delle tonsille del cervelletto, che è causata dalla pressione che spinge la parte inferiore del cervelletto attraverso il forame magno, che porta alla compressione del midollo allungato. Causa: 1) coscienza alterata; 2) violazioni del ritmo della respirazione o dell'apnea. 8. Trattamento del coma Il trattamento deve essere il più aggressivo possibile e mirato principalmente a garantire un'adeguata ossigenazione e stabilizzazione dell'emodinamica centrale. Se viene mantenuta la respirazione spontanea, si raccomanda l'insufflazione di ossigeno umidificato attraverso una maschera o un catetere nasale. In assenza di respirazione spontanea o in presenza di respirazione patologica si esegue l'intubazione tracheale ed il paziente viene trasferito in ventilazione polmonare artificiale. Con l'agitazione psicomotoria e la reazione alla ventilazione meccanica, è necessario l'uso di sedativi (benzodiazepine, butirrofenoni). La stabilizzazione dell'emodinamica centrale è la normalizzazione della pressione sanguigna. In uno stato ipertensivo, la pressione sanguigna deve essere ridotta, ma non più del 10% dell'originale all'ora. Un buon effetto è l'uso di nitroprussiato di sodio o solfato di magnesio. Con l'ipotensione vengono utilizzati dopamina, dopamina, dobutrex e farmaci ormonali. In assenza di dati anamnestici e di una diagnosi poco chiara, viene eseguita la terapia esjuvantibus (una risposta positiva all'esposizione al farmaco, da un lato, dà la chiave della diagnosi, dall'altro, aiuta a guadagnare tempo per evitare cambiamenti irreversibili) : 1) tiamina - 100 mg per via endovenosa, successivamente - 100 mg per via intramuscolare (soprattutto se c'è una storia di alcolismo, quando si determinano alte concentrazioni di etanolo nel sangue); 2) glucosio: una soluzione al 40% di 60 ml per via endovenosa (con un livello sconosciuto di glucosio nel plasma o a un livello inferiore a 3 mmol / l); 3) naloxone - 0,4-1,2 mg per via endovenosa, frazionata, ripetutamente, specialmente in presenza di "segni di oppiacei" (tracce di iniezioni endovenose, pupille strette, disturbi respiratori centrali); 4) anexat (flumazenil) - 0,2 mg per 30 secondi, nel minuto successivo, iniettare altri 0,3 mg, ogni minuto successivo - 0,5 mg fino a una dose totale di 3 mg. In assenza di un effetto, si può presumere che è improbabile che il coma sia causato da farmaci benzodiazepinici; 5) in caso di avvelenamento o sovradosaggio con un noto farmaco o sostanza, è necessario somministrare l'antidoto appropriato (se esiste la possibilità di terapia antidoto). Il trattamento viene effettuato: 1) controllo della sindrome convulsiva; 2) mantenimento della normotermia; 3) prevenzione di aspirazione di contenuti gastrici; 4) trattamento urologico; 5) diminuzione della pressione intracranica. 9. Rianimazione cardiopolmonare La rianimazione cardiopolmonare (RCP) è un complesso di misure chirurgiche e terapeutiche eseguite in assenza di lesioni potenzialmente letali e volte a ripristinare e supportare la funzione del sistema cardiorespiratorio. Indicazioni per la rianimazione cardiopolmonare: eseguita in pazienti privi di polso efficace sulle arterie carotidi o polso debole e filiforme, in stato di incoscienza e (o) in assenza di movimenti respiratori efficaci. I casi più comuni di arresto cardiaco primario e insufficienza respiratoria primaria. Controindicazioni: traumi incompatibili con la vita, stadi terminali di malattie incurabili e morte biologica. Principi di base Gli sforzi primari nella RCP sono volti a: 1) compressione toracica; 2) soffiare aria nei polmoni e ventilazione; 3) preparazione e somministrazione di farmaci; 4) installazione e manutenzione dell'accesso endovenoso; 5) attività specialistiche (defibrillazione, installazione di pacemaker, intubazione tracheale). Pertanto, per completare l'intero ambito delle attività, sono necessarie 4 persone e un team leader. Una persona dovrebbe essere responsabile della RCP. Questa persona dovrebbe integrare tutte le informazioni disponibili e dare priorità all'impatto. Deve monitorare il monitor ECG, l'uso di farmaci e garantire che le azioni degli altri membri del team siano corrette. Dovrebbe essere rimosso dall'esecuzione di procedure che sminuiscono il ruolo di leadership. Per più di 40 anni, l'alfabeto di rianimazione Safar è stato utilizzato per la RCP. In questo complesso si sostiene la sequenza delle azioni del rianimatore che, secondo il loro nome inglese, sono indicate dalle lettere corrispondenti. A - Vie aeree - garantendo la pervietà delle vie aeree. B - Respirazione - ventilazione polmonare artificiale (ALV) in modo accessibile, ad esempio durante la respirazione "bocca a bocca". C - Circolazione - garanzia dell'emocircolazione - massaggio cardiaco indiretto. D - Droghe - l'introduzione di farmaci. E - Elettrocardiografia - Registrazione ECG. F - Fibrilazione - condurre, se necessario, la defibrillazione elettrica (cardioversione). G - Gauging - valutazione dei risultati primari. H - Ipotermia - raffreddamento della testa. I - Terapia intensiva - terapia intensiva per sindromi post-rianimazione. 10. Garantire la pervietà delle vie respiratorie. IVL A - Vie aeree - Gestione delle vie aeree Il paziente viene posizionato orizzontalmente sulla schiena. La testa è gettata all'indietro il più possibile. Se un paziente con un tono muscolare ridotto giace sulla schiena, la sua lingua potrebbe affondare, come se si chiudesse la gola. Allo stesso tempo, l'epiglottide discende, bloccando ulteriormente le vie aeree. Appare: respiro sonoro, quindi violazioni del ritmo respiratorio fino al suo completo arresto. Tali fenomeni si sviluppano particolarmente rapidamente nei pazienti incoscienti. Per prevenire ed eliminare la retrazione della lingua, è necessario portare in avanti la mascella inferiore e contemporaneamente eseguire l'iperestensione dell'articolazione occipito-cervicale. Per fare ciò, con la pressione dei pollici sul mento, la mascella inferiore del paziente viene spostata verso il basso, quindi con le dita posizionate agli angoli della mascella, la spingono in avanti, integrando questa tecnica con una sovraestensione della testa posteriormente ( tripla tecnica Safari). Con la corretta e tempestiva conduzione di queste manipolazioni, la pervietà delle vie aeree a livello della faringe viene rapidamente ripristinata. La causa dell'ostruzione delle vie aeree possono essere corpi estranei. Vengono rapidamente rimossi con qualsiasi materiale improvvisato (tovagliolo). La testa del paziente deve essere girata di lato a causa del pericolo di aspirazione. Il ripristino della pervietà delle prime vie respiratorie è facilitato dall'uso di vari condotti d'aria. Il più conveniente è l'uso di un condotto dell'aria a forma di S. Per la sua introduzione, la bocca del paziente viene aperta con le dita incrociate II e I e il tubo viene fatto avanzare fino alla radice della lingua in modo che la sua apertura "scivoli" lungo il palato. È necessario prestare attenzione per garantire che il condotto dell'aria non si muova durante il trasporto. Se tutte le procedure descritte non sono efficaci, si può ipotizzare la presenza di otturazione delle vie aeree nelle sezioni sottostanti. In questi casi è necessaria la laringoscopia diretta e l'aspirazione attiva della secrezione patologica, seguita da intubazione tracheale per 10-15 secondi. Si consiglia di eseguire conicotomia e tracheostomia. B - Respirazione - ventilazione polmonare artificiale (ALV) in modo accessibile Il metodo più semplice ed efficace di respirazione artificiale durante la rianimazione è il metodo bocca a bocca. Dopo 2-3 insufflazioni dei polmoni, viene determinata la presenza di un impulso sull'arteria carotide, se non viene rilevato, si procede al ripristino artificiale della circolazione sanguigna. La ventilazione manuale viene utilizzata utilizzando una sacca di tipo Ambu autoespandibile. Quando si utilizza un ventilatore, la frequenza respiratoria è di 12-15 al minuto, il volume inspiratorio è di 0,5-1,0 litri. In un ospedale viene eseguita l'intubazione tracheale e il paziente viene trasferito a un ventilatore. 11. Massaggio cardiaco indiretto Circolazione C - garantire l'emocircolazione - compressioni toraciche Il massaggio cardiaco chiuso è il modo più semplice ed efficace di supporto circolatorio artificiale di emergenza. Il massaggio cardiaco chiuso deve essere avviato immediatamente, non appena viene posta la diagnosi di arresto circolatorio acuto, senza chiarirne cause e meccanismi. In caso di contrazioni cardiache inefficaci, non si deve attendere un arresto cardiaco completo o un ripristino indipendente di un'adeguata attività cardiaca. Regole di base per il massaggio cardiaco chiuso. 1. Il paziente deve essere in posizione orizzontale su una base solida (pavimento o lettino basso) per evitare la possibilità di spostamento del suo corpo sotto il rafforzamento delle mani massaggianti. 2. La zona di applicazione della forza delle mani del rianimatore si trova sul terzo inferiore dello sterno, rigorosamente lungo la linea mediana; il rianimatore può trovarsi su entrambi i lati del paziente. 3. Per il massaggio, un palmo viene posizionato sopra l'altro e viene applicata una pressione sullo sterno nell'area situata 3-4 dita trasversali sopra il punto di attacco allo sterno del processo xifoideo; le mani del massaggiatore, raddrizzate all'altezza delle articolazioni del gomito, sono posizionate in modo che solo il polso produca pressione. 4. La compressione del torace della vittima viene eseguita a causa della gravità del busto del medico. Lo spostamento dello sterno verso la colonna vertebrale (cioè la profondità della deflessione del torace) dovrebbe essere di 4-6 cm. 5. La durata di una compressione toracica è 0,5 s, l'intervallo tra le singole compressioni è 0,5-1 s. Tasso di massaggio - 60 movimenti di massaggio al minuto. A intervalli, le mani non vengono rimosse dallo sterno, le dita rimangono sollevate, le braccia sono completamente estese alle articolazioni del gomito. Quando la rianimazione viene eseguita da una persona, dopo due rapide iniezioni di aria nei polmoni del paziente, vengono eseguite 15 compressioni toraciche, ovvero il rapporto "ventilazione: massaggio" è 2: 15. Se 2 persone sono coinvolte nella rianimazione, allora questo rapporto è 1: 5, cioè ci sono 5 compressioni toraciche per respiro. Un prerequisito per il massaggio cardiaco è il monitoraggio costante della sua efficacia. I criteri per l'efficacia del massaggio dovrebbero essere considerati come segue. 1. Cambiamento del colore della pelle: diventa meno pallida, grigia, cianotica. 2. Costrizione delle pupille, se dilatate, con apparenza di reazione alla luce. 3. La comparsa di un impulso cardiaco sulle arterie carotidee e femorali e talvolta sull'arteria radiale. 4. Determinazione della pressione sanguigna a livello di 60-70 mm Hg. Arte. se misurato alla spalla. 5. A volte la comparsa di movimenti respiratori indipendenti. 12. L'introduzione dei farmaci. Registrazione ECG D - Droghe - l'introduzione di farmaci. In caso di interruzione acuta della circolazione sanguigna, l'introduzione di agenti che stimolano l'attività cardiaca dovrebbe iniziare il prima possibile, se necessario, ripetuta durante la rianimazione. Dopo l'inizio del massaggio cardiaco, iniettare 0,5-1 ml di adrenalina il prima possibile (per via endovenosa o intratracheale). Le sue iniezioni ripetute sono possibili dopo 2-5 minuti (fino a 5-6 ml in totale). Con l'asistolia, l'adrenalina tonifica il miocardio e aiuta a "avviare" il cuore, con la fibrillazione ventricolare contribuisce al passaggio dalla fibrillazione a onde piccole a quelle a onde grandi, che facilita notevolmente la defibrillazione. L'adrenalina facilita il flusso sanguigno coronarico e aumenta la contrattilità del muscolo cardiaco. Al posto dell'adrenalina, può essere utilizzata l'isodrina, che è 3 volte più efficace dell'adrenalina in termini di efficacia dell'effetto sul miocardio. La dose iniziale è di 1-2 ml per iniezione endovenosa e i successivi 1-2 ml in 250 ml di una soluzione di glucosio al 5%. In condizioni di alterata circolazione sanguigna, l'acidosi metabolica aumenta progressivamente, pertanto, subito dopo l'infusione di adrenalina, viene somministrata per via endovenosa una soluzione al 4-5% di bicarbonato di sodio alla velocità di 3 ml / kg del peso corporeo del paziente. Nel processo di morte, il tono del sistema nervoso parasimpatico aumenta in modo significativo, il cervello è esaurito, quindi vengono utilizzati gli M-colinolitici. Con asistolia e bradicardia, l'atropina viene somministrata per via endovenosa in una soluzione allo 0,1% - 0,5-1 ml, fino a una dose massima di 3-4 ml. Per aumentare il tono miocardico e ridurre l'effetto dell'iperkaliemia, si raccomanda la somministrazione endovenosa di 5 ml di una soluzione al 10% di cloruro di calcio. Adrenalina, atropina e cloruro di calcio possono essere somministrati insieme nella stessa siringa. Con tachicardia grave e soprattutto con lo sviluppo di fibrillazione, è indicato l'uso di lidocaina alla dose di 60-80 mg, ma poiché è a breve durata d'azione, viene infusa ad una velocità di 2 mg / min. È inoltre indicato l'uso di glucocorticoidi, che, aumentando la sensibilità delle strutture miocardiche adrenoreattive alle catecolamine e normalizzando la permeabilità delle membrane cellulari, contribuiscono al ripristino di un'adeguata attività cardiaca. E - Elettrocardiografia - Registrazione ECG Con l'aiuto di uno studio ECG, viene determinata la natura della violazione dell'attività cardiaca. Molto spesso può essere asistolia - completa cessazione delle contrazioni cardiache, fibrillazione - contrazione caotica non coordinata delle fibre miocardiche con una frequenza di 400-500 battiti / min, in cui la gittata cardiaca praticamente si interrompe. Inizialmente si nota una fibrillazione a onde grandi, che, entro 1-2 minuti, passa in fibrillazione a onde piccole, seguita da asistolia. La presenza di qualsiasi ritmo sull'ECG è migliore della completa assenza di attività elettrica del miocardio. Pertanto, il compito chiave della RCP è stimolare l'attività elettrica del miocardio e successivamente modificarla in un ritmo efficace (presenza di un impulso). 13. Defibrillazione elettrica F - Fibrilazione - condurre, se necessario, defibrillazione elettrica (cardioversione) La fibrillazione cardiaca può essere eliminata mediante l'uso della defibrillazione elettrica. È necessario applicare saldamente gli elettrodi al torace (in posizione anterolaterale, un elettrodo si trova nella regione dell'apice del cuore, il secondo nella regione succlavia a destra dello sterno), che aumenta la forza del scarica e, di conseguenza, l'efficacia della defibrillazione. In un certo numero di pazienti, la posizione anteroposteriore (apice del cuore - spazio interscapolare) degli elettrodi è più efficace. Non applicare elettrodi sulle sovrapposizioni del monitor ECG. Va notato che la defibrillazione elettrica è efficace solo quando sull'ECG vengono registrate oscillazioni a onde grandi con un'ampiezza compresa tra 0,5 e 1 mV o più. Questo tipo di fibrillazione miocardica indica la sicurezza delle sue risorse energetiche e la possibilità di ripristinare un'adeguata attività cardiaca. Se le oscillazioni sono basse, aritmiche e polimorfiche, che si osservano nell'ipossia miocardica grave, la possibilità di ripristinare l'attività cardiaca dopo la defibrillazione è minima. In questo caso, con l'aiuto del massaggio cardiaco, della ventilazione meccanica, della somministrazione endovenosa di adrenalina, atropina, cloruro di calcio, è necessario ottenere il trasferimento della fibrillazione alle onde grandi e solo dopo deve essere eseguita la defibrillazione. Il primo tentativo di defibrillazione viene effettuato con una scarica di 200 J, con i successivi tentativi la carica sale a 360 J. Gli elettrodi devono essere inumiditi e premuti saldamente sulla superficie del torace. Gli errori più comuni durante la defibrillazione, che causano l'inefficacia di quest'ultima, includono quanto segue. 1. Lunghe interruzioni del massaggio cardiaco o completa assenza di rianimazione durante la preparazione del defibrillatore per la dimissione. 2. Pressatura allentata o inumidimento insufficiente degli elettrodi. 3. Applicazione di una scarica sullo sfondo della fibrillazione a onde basse senza adottare misure che aumentino le risorse energetiche del miocardio. 4. Applicare una scarica di tensione bassa o eccessivamente alta. Va notato che la defibrillazione elettrica del cuore è un metodo efficace per correggere tali aritmie cardiache come tachicardia ventricolare parossistica, flutter atriale, tachicardia nodale e sopraventricolare, fibrillazione atriale. L'indicazione per la defibrillazione elettrica, nella fase preospedaliera, è il più delle volte la tachicardia ventricolare parossistica. Una caratteristica della defibrillazione in queste condizioni è la presenza di coscienza nel paziente e la necessità di eliminare la reazione al dolore quando si applica una scarica elettrica. 14. Terapia intensiva delle sindromi post-rianimazione I-Terapia intensiva - terapia intensiva per sindromi post-rianimazione 1. Correzione del CBS e dell'equilibrio idroelettrolitico. Spesso dopo la RCP si sviluppano alcalosi metabolica, ipokaliemia, ipocloremia e altri disturbi elettrolitici. C'è uno spostamento del pH in un ambiente acido o alcalino. La chiave per la correzione del pH è un'adeguata ventilazione. L'uso del bicarbonato deve essere effettuato sotto il controllo della composizione gassosa del sangue. Di norma, non è necessaria l'introduzione di HCO3 con un rapido ripristino della circolazione sanguigna e della respirazione. Con un cuore funzionante, un livello di pH di ~ 7,15 è adeguato per il funzionamento del sistema cardiovascolare. 2. Normalizzazione del sistema di difesa antiossidante. La terapia intensiva comprende un complesso di farmaci antiossidanti con azione multidirezionale: mafusol, unitiol, vitamina C, multibiont, tocoferolo, probucol, ecc. 3. L'uso di antiossidanti aiuta a ridurre l'intensità dei processi metabolici e, di conseguenza, a ridurre il fabbisogno di ossigeno ed energia, nonché il massimo utilizzo della ridotta quantità di ossigeno disponibile durante l'ipossia. Ciò si ottiene attraverso l'uso di farmaci di protezione neurovegetativa e antiipoxants (seduxen, droperidolo, bloccanti gangliari, mexamina, idrossibutirrato di sodio, citocromo, gutimina, ecc.). 4. Un aumento delle risorse energetiche è fornito dalla somministrazione endovenosa di soluzioni concentrate di glucosio con insulina e i principali coenzimi coinvolti nell'utilizzo dell'energia (vitamina B6, cocarbossilasi, ATP, riboxina, ecc.). 5. La stimolazione della sintesi di proteine e acidi nucleici - substrati assolutamente necessari per il normale funzionamento delle cellule, la sintesi di enzimi, immunoglobuline e altri, viene effettuata mediante l'uso di ormoni anabolici (retabolil, nerabolil, insulina, retinolo ), acido folico, nonché l'introduzione di soluzioni di amminoacidi. 6. L'attivazione del metabolismo aerobico si ottiene introducendo una quantità sufficiente di substrati di ossidazione (glucosio), nonché utilizzando l'ossigenazione iperbolica (HBO): questo metodo garantisce la fornitura della quantità richiesta di ossigeno anche in condizioni di forti violazioni della sua erogazione . 7. Miglioramento dei processi redox (acido succinico, riboxin, tocoferolo, ecc.). 8. La terapia disintossicante attiva contribuisce alla normalizzazione dei processi metabolici. Per questo vengono utilizzati vari metodi di terapia infusionale (gelatinolo, albumina, plasma), diuresi forzata, ecc.. Nei casi più gravi vengono utilizzati metodi di disintossicazione extracorporea (emoassorbimento, emodialisi, plasmaferesi). 9. Eliminazione delle violazioni dei processi di microcircolazione. Per questo viene eseguita la terapia con eparina. 15. Laringospasmo Il laringospasmo è la chiusura delle corde vocali vere e false. In entrambi i casi vengono necessariamente utilizzati agenti di controllo (eufillin). Se ciò non aiuta, è necessario introdurre miorilassanti a breve durata d'azione, intubare e trasferire il paziente in ventilazione meccanica. I miorilassanti causano insufficienza respiratoria nel periodo postoperatorio se non viene eseguita una decurarizzazione sufficiente. Di solito è prodotto da farmaci anticolinesterasici (prozerin). Al momento dell'estubazione, è necessario assicurarsi che la forza e il tono muscolare siano stati ripristinati (chiedere di alzare una mano, stringere una mano, alzare la testa). Con fratture multiple delle costole, parte del torace affonda durante l'inalazione, si sviluppa la cosiddetta respirazione paradossale, quindi è necessario ripristinare la struttura del torace. Per questo paziente è necessario intubare, dopo aver introdotto i miorilassanti, con ulteriore trasferimento alla ventilazione meccanica (fino al ripristino dell'integrità del torace). Quanto segue porta ad una diminuzione del parenchima polmonare funzionante: atelettasia, collasso polmonare, polmonite, conseguenze di un intervento chirurgico, pneumo-, emo-, piotorace. Differenze tra atelettasia e collasso: l'atelettasia è un'ostruzione in uno stato raddrizzato. Questa condizione è caratterizzata dalla presenza di un polmone non ventilato attraverso il quale passa metà del sangue circolante, quest'ultimo non ossigenato. Di conseguenza, si sviluppa insufficienza respiratoria acuta. Quando il polmone collassa, viene compresso da aria o fluido nella cavità pleurica. Allo stesso tempo, la circolazione sanguigna nel polmone compresso diminuisce drasticamente e aumenta la circolazione sanguigna nel polmone sano. Pertanto, il collasso non è una complicazione così pericolosa in termini di sviluppo di insufficienza respiratoria acuta come l'atelettasia. Prima dell'intervento chirurgico, deve essere valutata la funzione del polmone intatto (spirografia separata). Secondo lo stadio di sviluppo, l'insufficienza respiratoria acuta è suddivisa in: 1) disfunzione; 2) insufficienza; 3) fallimento della funzione protesica. Secondo il tasso di sviluppo, l'insufficienza respiratoria acuta è suddivisa in: 1) fulmineo (si sviluppa entro un minuto); 2) acuto (si sviluppa entro poche ore); 3) subacuto (si sviluppa entro pochi giorni); 4) cronico (dura per anni). I principali elementi della terapia intensiva per l'insufficienza respiratoria acuta: ossigenoterapia, posizione di drenaggio del paziente, fibrobroncoscopia, tracheostomia, intubazione e ventilazione meccanica, broncodilatazione, terapia ormonale, HBO. 16. Embolia polmonare L'embolia polmonare (EP) è un blocco del tronco principale o medio, piccoli tronchi vascolari dell'arteria polmonare, che porta ad un aumento della pressione nella circolazione polmonare, insufficienza ventricolare destra. Classificazione clinica di PE Forma: pesante, media e leggera. A valle: fulminante, acuto, ricorrente. Secondo il livello di danno all'arteria polmonare: tronco o rami principali, rami lobari (segmentali), rami piccoli. Il decorso clinico dell'EP è abbastanza variabile. I sintomi più comuni sono l'insorgenza improvvisa di dispnea (RR varia da 30 a più di 50 al minuto), respiro rapido, pallore, più spesso cianosi, gonfiore delle vene giugulari, tachicardia, ipotensione arteriosa (fino a shock), retrosternale dolore, tosse ed emottisi. L'auscultazione determina spesso il rafforzamento dell'II tono sull'arteria polmonare. Segni radiografici: aumento delle dimensioni dell'arteria polmonare prossimale, esaurimento del pattern periferico e aumento della cupola del diaframma. L'ECG può rivelare un sovraccarico dei reparti giusti (cuore polmonare): 1) la comparsa di onde Q con un aumento simultaneo dell'ampiezza delle onde R e S (sindrome QS); 2) rotazione del cuore attorno all'asse longitudinale con il ventricolo destro in avanti (spostamento della zona di transizione verso il torace sinistro conduce); 3) sopraslivellamento del tratto ST con onda negativa nelle derivazioni III, aUR, V1-V3; 4) la comparsa o l'aumento del grado di blocco della gamba destra del fascio di His; 5) dente P "polmonare" a punta alta con una deviazione del suo asse elettrico a destra; 6) tachicardia sinusale o forma tachisistolica di fibrillazione atriale. L'ecocardiografia consente di rilevare il cuore polmonare acuto, determinare la gravità dell'ipertensione nella circolazione polmonare, valutare lo stato strutturale e funzionale del ventricolo destro, rilevare il tromboembolismo nelle cavità cardiache e nelle principali arterie polmonari, visualizzare un forame ovale aperto, che può interessare la gravità dei disturbi emodinamici ed essere causa di embolia paradossale. Tuttavia, un risultato ecocardiografico negativo non esclude in alcun modo la diagnosi di embolia polmonare. Il metodo diagnostico più informativo è l'angiografia dell'arteria polmonare. trattamento 1. Terapia anticoagulante. 2. Terapia trombolitica. 3. Trattamento chirurgico. 17. Trattamento di emergenza dello stato asmatico Ossigenoterapia. L'ossigeno inumidito viene inalato2attraverso cateteri nasali o attraverso una maschera alla velocità di 1-2 l / min. L'adrenalina stimolaα1-,β., - e β2-recettori adrenergici, dilata i bronchi e riduce la resistenza delle vie aeree. L'eufillina inibisce la fosfodiesterasi, che contribuisce all'accumulo di AMP ciclico e alla rimozione del broncospasmo. Quando si prescrive l'aminofillina, devono essere prese in considerazione le controindicazioni, che includono fumo e infanzia, insufficienza cardiaca e sindrome coronarica acuta, malattie croniche dei polmoni, del fegato e dei reni. Con AS, la dose di carico di aminofillina è di 3-6 mg/kg, viene somministrata per via endovenosa in 20 minuti. Quindi eseguire l'infusione a goccia di mantenimento del farmaco. L'effetto della terapia con corticosteroidi è associato alla soppressione dell'infiammazione delle vie aeree e ad una maggiore sensibilità agli agenti β-adrenergici. Più grave è l'AS, maggiore è l'indicazione per una terapia corticosteroidea immediata. Inizialmente deve essere somministrata una dose elevata di corticosteroidi. Se la terapia è inefficace, la dose viene aumentata. Almeno ogni 6 ore, vengono somministrate dosi equivalenti appropriate di questi farmaci. Alla maggior parte dei pazienti viene mostrata una terapia inalatoria con b - adrenomimetici; (fenoterolo, alupent, salbutamolo). Le eccezioni sono casi di overdose di simpaticomimetici. Se la terapia in corso non dà effetto, è indicata la somministrazione endovenosa di agonisti β-adrenergici, come l'isoproterenolo, diluito in soluzione di glucosio al 5%. Le controindicazioni sono malattie cardiache (cardiosclerosi coronarica, infarto del miocardio), tachicardia grave e sintomi di tachifilassi, vecchiaia. La velocità di somministrazione dell'isoproterenolo è di 0,1 μg/kg per 1 minuto fino all'inizio della tachicardia (FC 130 per 1 minuto o più). La terapia infusionale è la componente più importante del trattamento dell'AS, volta a reintegrare la carenza di liquidi ed eliminare l'ipovolemia, il volume totale della terapia infusionale è di 3-5 litri al giorno. L'idratazione viene effettuata introducendo soluzioni contenenti una quantità sufficiente di acqua libera (soluzioni di glucosio), nonché soluzioni elettrolitiche ipo e isotoniche contenenti sodio e cloro. Indicatori di un'adeguata idratazione sono la cessazione della sete, la lingua bagnata, il ripristino della normale diuresi, una migliore evacuazione dell'espettorato e una diminuzione dell'ematocrito a 0,30-0,40. L'anestesia con alotano può essere utilizzata nel trattamento di un grave attacco d'asma che non è suscettibile di terapia convenzionale. Ventilazione artificiale dei polmoni. Le indicazioni per il trasferimento di pazienti con SA alla ventilazione meccanica dovrebbero essere molto rigide, poiché in questo stato provoca spesso complicazioni ed è caratterizzato da un'elevata mortalità. Allo stesso tempo, la ventilazione meccanica, se effettuata secondo rigorose indicazioni, è l'unico metodo in grado di prevenire l'ulteriore progressione dell'ipossia e dell'ipercapnia. 18. Infarto del miocardio L'infarto miocardico è una discrepanza tra la richiesta di ossigeno del miocardio e la sua erogazione, con conseguente necrosi limitata del muscolo cardiaco. La causa più comune è un trombo, meno spesso un embolo, meno spesso uno spasmo delle arterie coronarie. La trombosi è più spesso osservata sullo sfondo del danno aterosclerotico alle arterie coronarie. Classicamente, l'infarto del miocardio inizia con un dolore crescente dietro lo sterno, che in natura brucia e preme. Caratterizzato da un'ampia irradiazione del dolore alle braccia (più spesso a sinistra), schiena, addome, testa, sotto la scapola sinistra, nella mascella inferiore sinistra, ecc. I pazienti sono irrequieti, ansiosi, a volte notano una sensazione di paura di morte. Ci sono segni di insufficienza cardiaca e vascolare: estremità fredde, sudore umido, ecc. La sindrome del dolore è prolungata e non viene alleviata dalla nitroglicerina per 30 minuti o più. Ci sono vari disturbi del ritmo cardiaco, un calo della pressione sanguigna o il suo aumento. I pazienti notano soggettivamente la sensazione di mancanza d'aria. I segni di cui sopra sono tipici del periodo I - doloroso o ischemico, la cui durata varia da alcune ore a 2 giorni. Obiettivamente, un aumento della pressione sanguigna (quindi una diminuzione); aumento della frequenza cardiaca o disturbi del ritmo; all'auscultazione si sente un tono IV anormale; i suoni del cuore sono smorzati; sull'accento dell'aorta II tono; non ci sono praticamente cambiamenti biochimici nel sangue, segni caratteristici sull'ECG. Il secondo periodo è acuto (febbrile, infiammatorio), caratterizzato dal verificarsi di necrosi del muscolo cardiaco nel sito di ischemia. Il dolore di solito scompare. La durata del periodo acuto è fino a 2 settimane. Il benessere del paziente migliora gradualmente, ma persistono debolezza generale, malessere e tachicardia. I suoni cardiaci sono ovattati. L'aumento della temperatura corporea causato dal processo infiammatorio nel miocardio, solitamente piccolo, fino a 38°C, compare solitamente il 3° giorno della malattia. Entro la fine della prima settimana, la temperatura ritorna solitamente alla normalità. Il terzo periodo (periodo subacuto o cicatriziale) dura 4-6 settimane. Caratteristica è la normalizzazione dei parametri del sangue (enzimi), la temperatura corporea si normalizza, tutti gli altri segni di un processo acuto scompaiono: l'ECG cambia, una cicatrice del tessuto connettivo si sviluppa nel sito di necrosi. Il quarto periodo (periodo di riabilitazione, recupero) dura da 6 mesi a 1 anno. Non ci sono segni clinici. Durante questo periodo, si verifica l'ipertrofia compensatoria delle fibre muscolari miocardiche intatte e si sviluppano altri meccanismi compensatori. C'è un graduale ripristino della funzione miocardica. Ma l'onda Q patologica persiste sull'ECG. Il trattamento ha lo scopo di prevenire le complicanze, limitare la zona dell'infarto, alleviare il dolore e correggere l'ipossia. 19. Shock cardiogeno Lo shock cardiogeno è un disturbo circolatorio critico con ipotensione arteriosa e segni di deterioramento acuto della circolazione sanguigna negli organi e nei tessuti. Il principale segno diagnostico è una significativa diminuzione della pressione arteriosa sistolica, che è inferiore a 90 mm Hg. Arte. La differenza tra pressione sistolica e diastolica (pressione del polso) è di 20 mm Hg. Arte. o diventando ancora più piccolo. Inoltre, si sta sviluppando una clinica di un forte deterioramento della perfusione di organi e tessuti: 1) alterazione della coscienza da lieve letargia a psicosi o coma, possono comparire sintomi neurologici focali; 2) diuresi inferiore a 20 ml/h. Sintomi di deterioramento della circolazione periferica: pelle pallida cianotica, marmorizzata, mattone, umida; vene periferiche collassate, una forte diminuzione della temperatura della pelle delle mani e dei piedi; diminuzione del flusso sanguigno. Il valore del CVP può essere diverso. Gli indicatori normali di CVP sono 5-8 cm di acqua. Arte.; indicatore sotto i 5 cm di acqua. Arte. indica ipovolemia e bassa pressione sanguigna e oltre 8 cm di acqua. Arte. indica insufficienza ventricolare destra. trattamento È indicata l'ossigenoterapia con ossigeno umidificato attraverso una maschera o cateteri nasali. Anticoagulanti dolorosamente somministrati alla dose di 10 UI, seguiti da infusomat per via endovenosa 000 UI all'ora. È necessario somministrare analgesici: morfina 1000% 1 ml per via sottocutanea o endovenosa in bolo; analgin 1,0% 50 ml per via intramuscolare, endovenosa. Tonici vascolari: Cordiamin 1-4 ml per via endovenosa; mezaton 1% 1,0 g per via sottocutanea, endovenosa, in soluzione fisiologica; noradrenalina 0,2% 1,0 g per via endovenosa. Il vero shock cardiogeno viene trattato come segue. Per aumentare l'attività contrattile del miocardio si utilizza: strofantina 0,05% 0,5-0,75 g per via endovenosa lentamente per soluzione isotonica 20,0, korglucon 0,01 g per via endovenosa, anche in una soluzione isotonica o in una miscela polarizzante, glucagone 2-4 mg per via endovenosa gocciolare su una soluzione polarizzante. Normalizzazione della pressione sanguigna: noradrenalina 0,2% 2-4 ml per 1 litro di soluzione di glucosio al 5% o soluzione isotonica. La pressione arteriosa è mantenuta a 100 mm Hg. Art., mezaton 1% 1,0 g per via endovenosa; cordiammina 2-4 ml, dopamina 200 mg in 400 ml di reopoliglucina o glucosio al 5%. Con un effetto instabile dei suddetti farmaci, vengono utilizzati idrocortisone 200 mg, prednisolone 90-120 mg. Normalizzazione delle proprietà reologiche del sangue. Eliminazione dell'ipovolemia, poiché vi è sudorazione della parte liquida del sangue: reopoliglyukin, polyglukin - in un volume fino a 100 ml a una velocità di 50,0 ml al minuto. Correzione dell'equilibrio acido-base (lotta contro l'acidosi): bicarbonato di sodio dal 5% a 200,0 ml. Reintroduzione di antidolorifici. Ripristino dei disturbi del ritmo e della conduzione. 20. Crisi ipertensiva Una crisi ipertensiva è un improvviso aumento della pressione sanguigna a un livello che di solito non è caratteristico di questo paziente, che porta a disturbi circolatori regionali acuti e danni agli organi bersaglio (cuore, cervello, reni, intestino). I fattori esterni che provocano una crisi possono essere: 1) stress psico-emotivo; 2) influenze meteorologiche; 3) consumo eccessivo di sale da cucina. I sintomi clinici di una crisi si manifestano con il rumore nelle orecchie, mosche lampeggianti davanti agli occhi, mal di testa scoppiato nella regione occipitale, aggravato da chinarsi, sforzarsi, tossere, nausea, vomito, disturbi del ritmo cardiaco. Durante una crisi, si verificano pericolose violazioni della circolazione coronarica cerebrale, meno spesso renale e addominale, che porta a ictus, infarto del miocardio e altre gravi complicazioni. L'ECG rivela l'ipertrofia ventricolare sinistra. La radiografia del torace mostra un cuore ingrossato, deformità aortica sotto forma del numero "3", usura delle costole a causa dell'aumento del flusso sanguigno collaterale attraverso le arterie intercostali. L'aortografia conferma la diagnosi. La forma neurovegetativa della crisi è caratterizzata da un esordio improvviso, eccitazione, iperemia e umidità della pelle, tachicardia, minzione abbondante e frequente, aumento predominante della pressione sistolica con aumento dell'ampiezza del polso. Tali crisi sono altrimenti chiamate crisi surrenali o di tipo I. Le crisi di tipo I di solito hanno un decorso relativamente benigno, sebbene possano portare ad aritmie parossistiche o angina pectoris e, nei casi più gravi, a infarto del miocardio. Con la forma salina della crisi, la condizione peggiora gradualmente, si notano sonnolenza, debolezza, letargia, disorientamento, pallore e gonfiore del viso e gonfiore. La pressione sistolica e diastolica aumenta in modo uniforme o con una predominanza di quest'ultima e una diminuzione della pressione del polso. Tali crisi sono chiamate crisi di tipo II. Le crisi di tipo II, di regola, sono gravi e possono essere complicate da infarto del miocardio, ictus, insufficienza ventricolare sinistra acuta. È necessario evidenziare le crisi ipertensive che si sviluppano a seguito di una brusca cessazione della terapia antiipertensiva permanente, in particolare l'assunzione di b-bloccanti, nifedipina, simpaticolitici e soprattutto clonidina. Il trattamento di una crisi ipertensiva consiste in un urgente abbassamento della pressione sanguigna a un livello normale, necessario per prevenire o limitare i danni agli organi bersaglio nell'ipertensione, per prevenire complicazioni fino alla morte nei casi più gravi o disabilità permanente nello sviluppo dell'ictus , infarto miocardico. 21. Aritmia. Parossismo di fibrillazione atriale Un'aritmia è un ritmo cardiaco diverso dal seno. Classificazione delle aritmie 1. Violazione della formazione degli impulsi: 1) nel nodo del seno: a) tachicardia sinusale; b) bradicardia sinusale; c) aritmia sinusale; d) sindrome del seno malato (SSS); 2) aritmie ectopiche: a) extrasistolia; b) tachicardia parossistica; c) fibrillazione atriale e flutter; d) sfarfallio e sfarfallio dei ventricoli. 2. Violazione della conduzione degli impulsi: 1) percorsi aggiuntivi (pacchetti Kent); 2) blocco cardiaco: a) atriale (intra-atriale); b) atrioventricolare; c) intraventricolare. Meccanismi delle aritmie Una diminuzione del potenziale di riposo, la soglia di eccitabilità si verifica solo sulla base di una carenza di potassio cellulare, il rapporto "plasma - cellula" (normalmente 80 meq di potassio sono nella cellula e 5 meq nel plasma). Asimmetria del focus elettrofisiologico-metabolico del miocardio a causa di ischemia, infiammazione, riperfusione durante la trombolisi. Debolezza elettrofisiologica del pacemaker superiore. Vie di conduzione accessorie congenite. La tachicardia parossistica sopraventricolare è un attacco improvviso di battito cardiaco con una frequenza di 150-250 battiti al minuto. Ci sono 3 forme: 1) atriale; 2) nodale; 3) ventricolare. L'eziologia della tachicardia parossistica sopraventricolare è più spesso associata ad un aumento dell'attività del sistema nervoso simpatico. Si manifesta clinicamente con un improvviso attacco del battito cardiaco, i vasi del collo pulsano, l'attività cardiaca passa a un ritmo diverso. La durata dell'attacco va da alcuni minuti a diversi giorni. Il numero di battiti cardiaci nella forma ventricolare è solitamente compreso tra 150 e 180 battiti al minuto, con le forme sopraventricolari - 180-240 battiti al minuto. Durante un attacco, un ritmo a pendolo è caratteristico dell'auscultazione, non c'è differenza tra I e II tono. Aumenta la richiesta di ossigeno del miocardio e può provocare un attacco di insufficienza coronarica acuta. Segni ECG 1. I complessi QRS non vengono modificati. 2. Nella forma sopraventricolare, l'onda P si fonde con T. 22. Extrasistolia ventricolare. Disturbo della conduzione AV L'extrasistole ventricolare è il verificarsi di un complesso QRS straordinariamente ampio e deformato, uno spostamento ST e T discordante, una pausa compensatoria completa (l'intervallo tra l'onda P pre e post extrasistolica è pari al doppio del normale intervallo RR). Il farmaco di scelta è la lidocaina, che viene somministrata secondo lo schema di cui sopra. Forse l'uso di cordarone alla dose di 300-450 mg per via endovenosa. Violazione della conduzione AV con sviluppo di sincope (sindrome di Morgagni-Adams-Stokes) Quando la conduzione è disturbata, si verificano vari tipi di blocchi cardiaci, c'è un rallentamento o una completa cessazione della conduzione dell'impulso attraverso il sistema di conduzione del cuore. Il blocco senoauricolare è caratterizzato da disfunzione dei linfociti T e ridotta conduzione degli impulsi dal nodo seno-atriale agli atri. Ci sono 3 gradi. I grado - rallentando l'impulso. Sull'ECG - prolungamento dell'intervallo PQ per più di 0,20 s. Prolasso del complesso QRS. L'intervallo RR è stabile. II grado - perdita di parte degli impulsi, conduzione incompleta. Mobitz tipo I - man mano che gli impulsi vengono eseguiti, l'intervallo PQ si allunga gradualmente fino alla completa perdita dell'onda del polso. QRS non viene modificato. Nel sito del prolasso QRS, la distanza maggiore è RR. Prognosticamente, questo tipo è relativamente favorevole. Mobitz tipo II con un intervallo PQ costante e un complesso QRS invariato. Allo stesso tempo, non tutti gli impulsi raggiungono i ventricoli - in alcuni casi viene eseguito ogni secondo impulso, in altri - ogni terzo, ecc., cioè c'è un prolasso periodico del complesso QRS 3: 2, 4: 3 , 5: 6, ecc. d. III grado - blocco completo della conduzione. Allo stesso tempo, la conduzione degli impulsi ai ventricoli viene completamente interrotta e nei ventricoli nasce un focus eterotopico del ritmo idioventricolare e più basso è l'automatismo, più difficile è la clinica. Si osserva una dissociazione completa: il ritmo atriale è vicino al normale e i ventricoli hanno una frequenza propria - 40 battiti al minuto o meno. Quest'ultimo dipende dal livello di danno: se il nodo AV soffre, 40-50 per 1 minuto, se la gamba del fascio di His - 20 battiti per 1 minuto o meno. Il livello di danno è indicato anche dal grado di deformazione del complesso QRS. I suoni del cuore sono indeboliti, periodicamente c'è un "cannone" I tono, quando la sistole degli atri e dei ventricoli quasi coincide nel tempo. Può essere III tono aggiuntivo. Alla base del cuore possono comparire soffi di eiezione sistolica. Spesso si riscontra una pulsazione delle vene associata alla contrazione atriale, particolarmente distinta dal tono cannone di Strazhesko. clinica Fallimento del cuore, se cade un impulso. Vertigini se cadono diversi impulsi. Sindrome di Morgagni-Adams-Stokes (perdita di coscienza), se cadono 6-8 complessi. trattamento Per ripristinare un ritmo adeguato, l'atropina viene somministrata alla dose da 0,5-1 mg a 3 mg. Ogni 3 minuti, 1 mg per una dose totale di 0,4 mg/kg. Calcio antagonisti - isoptina 0,04 mg/kg. Con la frequente perdita di coscienza, il paziente viene trasferito alla terapia elettropulsante permanente. Ma più spesso il ritmo deve essere eseguito "on demand". 23. Cause di insufficienza renale acuta L'insufficienza renale acuta (ARF) è una complicazione di una serie di malattie renali ed extrarenali caratterizzate da un forte deterioramento o cessazione della funzione renale e manifestata dal seguente complesso sintomatologico: oligoanuria, azotemia, iperidratazione, alterata CBS e bilancio idrico ed elettrolitico. Le forme di OOP includono: 1) prerenale (emodinamico); 2) renale (parenchimale); 3) postrenale (ostruttivo); 4) areale. Ragioni per lo sviluppo dell'insufficienza renale acuta prerenale. 1. Diminuzione della gittata cardiaca (shock cardiogeno, aritmia parossistica, tamponamento cardiaco, embolia polmonare, insufficienza cardiaca congestizia). 2. Diminuzione del tono vascolare (sepsi, shock tossico-infettivo, shock anafilattico, sovradosaggio di farmaci antipertensivi). 3. Diminuzione del volume intravascolare efficace (perdita di sangue, perdita di plasma, disidratazione - perdita del 7-10% del peso corporeo). 4. Violazione dell'emodinamica intrarenale (assunzione di FANS, ACE-inibitori, farmaci radiopachi, sandimmune). 5. Avvelenamento idrico - iperidratazione (produzione incontrollata di ADH nei tumori maligni, malattie infiammatorie del sistema nervoso centrale, sovradosaggio di farmaci - farmaci, barbiturici, farmaci antidiabetici sulfanilamide, indometacina, amitriptilina, ciclofosfamide). Ragioni per lo sviluppo dell'insufficienza renale acuta renale. 1. Ischemia del rene. 2. Danno nefrotossico dovuto all'esposizione a: 1) farmaci (aminoglicosidi, FANS, farmaci radiopachi, ecc.; 2) nefrotossine industriali (sali di metalli pesanti); 3) nefrotossine domestiche (glicole etilenico, alcol metilico, dicloroetano, tetracloruro di carbonio). 3. Ostruzione intratubulare da pigmenti: 1) emoglobina; 2) urati; 3) mioglobina; 4) processi infiammatori; 5) papillite necrotica (diabete mellito, analgesico, nefropatia alcolica); 6) patologia vascolare. Ragioni per lo sviluppo dell'insufficienza renale acuta postrenale. 1. Patologia degli ureteri: 1) ostruzione; 2) compressione. 2. Patologia della vescica. 3. Stenosi uretrale. 24. Clinica e trattamento dell'insufficienza renale acuta Ci sono cinque fasi nel decorso clinico dell'insufficienza renale acuta. Lo stadio I dell'insufficienza renale acuta è iniziale, dura dal momento in cui si manifesta il fattore eziologico fino alla comparsa dei primi segni. In questa fase, le tattiche terapeutiche mirano ad eliminare o mitigare l'impatto del fattore eziologico: terapia anti-shock, reintegrare il BCC, combattere l'insufficienza cardiaca, terapia alcalinizzante per l'emolisi intravascolare, combattere il dolore, trattare condizioni settiche, ecc. Insieme a eziologico terapia, lo spasmo dei vasi renali viene eliminato sotto il controllo della diuresi oraria. Quanto prima si inizia la stimolazione della diuresi, tanto più favorevole è la prognosi. Lo stadio II dell'insufficienza renale acuta, o oligoanurica, è caratterizzato dalla disfunzione del 70% dei nefroni. Una produzione di urina inferiore a 500 ml al giorno indica lo sviluppo di oliguria e una diminuzione a 50 ml al giorno o inferiore indica anuria. Oltre alla ridotta capacità dei reni di espellere l'acqua, ne risentono anche le funzioni di concentrazione e di escrezione di azoto. La quantità di elettroliti e azoto nelle urine diminuisce drasticamente. In questa fase si verificano i cambiamenti più pronunciati nell'emostasi. Il trattamento deve essere mirato alla costanza dell'ambiente interno in modo da concedere tempo e opportunità alla rigenerazione dell'epitelio renale. Uno stato di iperidratazione si sviluppa a causa della perdita di elettroliti durante il vomito e la diarrea. Pertanto, è necessario stimolare la diuresi, ma solo sotto il controllo del CVP. Migliora il flusso sanguigno renale. Poiché è necessario effettuare uno stretto controllo della diuresi, viene eseguita la cateterizzazione vescicale. La violazione della funzione di eliminazione dell'azoto dei reni porta all'azotemia, pertanto, per massimizzare la prevenzione della disgregazione proteica nel corpo, è necessario introdurre una quantità sufficiente di carboidrati. Se il decorso è grave e non trattabile, vengono eseguite sessioni di emodialisi. Se il fattore eziologico viene rimosso, dopo 5-7 giorni di trattamento, la diuresi inizia ad aumentare. La durata massima di questa fase è fino a 2 settimane. III stadio di insufficienza renale acuta - poliurico precoce. È caratterizzato da un progressivo aumento della diuresi (di 200-300 ml al giorno) fino a 3 litri. Le funzioni di escrezione e concentrazione di azoto dei reni non si sono ancora completamente riprese, ma la concentrazione di potassio, magnesio e fosfati si sta gradualmente normalizzando. La terapia intensiva nella fase poliurica precoce dovrebbe comprendere le stesse misure della precedente, fatta eccezione per la stimolazione della diuresi. Spesso è necessaria l'emodialisi. C'è un alto rischio di disidratazione. IV stadio di insufficienza renale acuta - poliuria tardiva. L'aumento giornaliero delle urine raggiunge 500-1000 ml e la diuresi può raggiungere 8-10 litri al giorno o più. Nei reni, i processi di scambio ionico iniziano a riprendersi. Le perdite di potassio, magnesio, fosforo e altri elettroliti aumentano drasticamente, i pazienti sono a rischio di disidratazione e demineralizzazione. Pertanto, in questa fase gli elettroliti e il fluido vengono somministrati per via endovenosa. Fase V OPN, o fase di recupero. Viene ripristinata la funzione di concentrazione dei reni. La diuresi inizia a diminuire gradualmente fino alla normalità (2-3 litri al giorno) e la densità delle urine aumenta (1008-1028). 25. Insufficienza epatica acuta L'insufficienza epatica acuta è un complesso di sintomi caratterizzato da una violazione di una o più funzioni epatiche a causa di un danno acuto o cronico al suo parenchima. Le manifestazioni cliniche di ARF sono le seguenti. 1. La coagulopatia è causata da una carenza di fattori della coagulazione e da un aumento dell'attività fibrinolitica. Predispone al sanguinamento spontaneo dalle mucose: si possono osservare emorragie gastrointestinali, uterine, nasali. Sono possibili emorragie cerebrali. Per valutare lo stato del sistema emostatico, viene determinato il tempo di protrombina. 2. L'ipoglicemia è caratterizzata da un livello elevato di insulina nel plasma, dovuto a una diminuzione della sua captazione da parte del fegato. Porta a un rapido deterioramento dello stato neurologico e alla morte dei pazienti. 3. Violazioni dell'equilibrio idroelettrolitico e acido-base. L'insufficienza renale acuta allo stadio terminale è caratterizzata da iponatriemia, ipofosfatemia, ipocalcemia e ipomagnesiemia. Il cambiamento nello stato acido-base non ha una direzione univoca. L'alcalosi respiratoria associata alla stimolazione del centro respiratorio con sostanze tossiche può essere sostituita dall'acidosi respiratoria a causa dell'aumento della pressione intracranica e della soppressione dell'attività respiratoria. Nello sviluppo del coma epatico come decorso grave della malattia, si distinguono gli stadi del precoma, del coma minaccioso e del coma vero e proprio. Sono presenti anche coma epatocellulare (endogeno), risultante da necrosi massiva del parenchima, porto-cavale (bypass, shunt, esogeno), a causa di una significativa esclusione del fegato dai processi metabolici per la presenza di pronunciate anastomosi porto-cavali, e coma misto, che si verificano principalmente nella cirrosi epatica. Nel periodo precomatoso si sviluppano anoressia progressiva, nausea, diminuzione delle dimensioni del fegato, aumento dell'ittero, iperbilirubinemia e aumento del contenuto di acidi biliari nel sangue. In futuro, aumentano i disturbi neuropsichici, il rallentamento del pensiero, la depressione e talvolta l'euforia. Caratterizzato da instabilità dell'umore, irritabilità, la memoria è disturbata, il sonno è disturbato. I riflessi tendinei sono aumentati, è caratteristico un piccolo tremore degli arti. Si sviluppa l'azotemia. Con una terapia tempestiva, i pazienti possono uscire da questo stato, ma più spesso con gravi cambiamenti irreversibili nel fegato, si verifica il coma. Durante il periodo di coma è possibile l'eccitazione, che viene poi sostituita dalla depressione (stupore) e da un progressivo deterioramento della coscienza fino alla sua completa perdita. Si sviluppano fenomeni meningei, riflessi patologici, irrequietezza motoria, convulsioni. La respirazione è disturbata (come Kussmaul, Cheyne-Stokes); il polso è piccolo, aritmico; c'è l'ipotermia. Il viso del paziente è smunto, le estremità sono fredde, un caratteristico odore dolciastro del fegato proviene dalla bocca e dalla pelle, i fenomeni emorragici si intensificano (emorragie cutanee, sanguinamento dal naso, gengive, vene varicose dell'esofago, ecc.). 26. Trattamento dell'insufficienza epatica acuta Il tempestivo supporto inotropo è una componente essenziale della terapia intensiva. Prevenzione delle complicanze infettive - nomina di antibiotici cefalosporinici in combinazione con farmaci antimicotici (amfotericina-B). Epatoprotettori e farmaci stabilizzanti di membrana: prednisolone fino a 300 mg, vitamina C 500 mg, troxevasina 5 ml, sodio etamsilato 750 mg, Essentiale 30 ml, tocoferolo 4 ml per via intramuscolare, citomak 35 mg, cocarbossilasi 300 mg, acido nicotinico 30-40 mg, com-plamin 900 mg, sirepar 5-10 ml, acido glutammico 1% 400 ml, vikasol 10 ml per via endovenosa, vitamine del gruppo B. Inibitori della proteasi, che comprendono corticali 100mila unità, trasylol 400mila unità, antagonosan, go-dox. Stimolazione della diuresi: reogluman 400 ml, mannitolo, lasix fino a 200 mg per via endovenosa, eufillina 240 mg. Per correggere la coagulopatia, viene utilizzata la somministrazione endovenosa di vitamina K (10 mg al giorno per 3 giorni). L'effetto si verifica dopo 3 ore In questo caso, l'eliminazione dell'ipoprotrombinemia è associata a un ridotto assorbimento della vitamina K, derivante da una carenza di acidi biliari. In caso di sanguinamento o di sospette procedure invasive (cateterizzazione vascolare, dialisi peritoneale), la massa piastrinica o il plasma fresco congelato vengono somministrati per via endovenosa. L'edema cerebrale è una causa comune di morte. Il mannitolo viene somministrato alla velocità di 1 g/kg di peso corporeo. Nei pazienti con insufficienza renale, il mannitolo viene prescritto in combinazione con l'ultrafiltrazione per evitare iperosmolarità e iperidratazione. Con lo sviluppo del coma epatico, viene prescritto cloruro di potassio (soluzione allo 0,4-0,5% in una soluzione di glucosio al 5% con un volume di 500 ml per via endovenosa) o soluzione di bicarbonato di sodio (con acidosi metabolica); I pazienti respirano ossigeno umidificato attraverso un catetere nasale. Con una diminuzione della pressione arteriosa e venosa, la poliglucina e l'albumina vengono somministrate per via endovenosa. In presenza di emorragie massicce, vengono prese misure appropriate per fermarli, viene trasfuso sangue di un gruppo e vengono somministrati farmaci che contengono fattori di coagulazione del sangue. Con segni significativi di coagulazione intravascolare disseminata, l'eparina viene somministrata per via endovenosa alla dose di 10-000 UI in bolo. In caso di insufficienza renale, vengono eseguite l'emodialisi peritoneale e la plasmaferesi, che danno un buon risultato, ma l'introduzione dell'eparina è controindicata prima di queste manipolazioni. Per fermare l'agitazione psicomotoria e le convulsioni, vengono prescritti diprazina, aloperidolo, sodio ossibutirrato. Nei casi più gravi, ricorrere all'intubazione e alla ventilazione meccanica. È importante ricordare che esiste un alto rischio di sanguinamento, quindi tutte le manipolazioni devono essere eseguite con estrema cautela. Quando si rimuove il paziente dal coma, il passo successivo è condurre una terapia intensiva per la malattia sottostante. 27. Shock Lo shock è una forma di uno stato critico del corpo, manifestato da disfunzioni multiple d'organo, che si sviluppa a cascata sulla base di una crisi circolatoria generalizzata e, di regola, termina con la morte senza trattamento. Un fattore shock è qualsiasi effetto sul corpo che supera i meccanismi adattivi in termini di forza. In stato di shock, le funzioni della respirazione, del sistema cardiovascolare e dei reni cambiano, i processi di microcircolazione di organi e tessuti e i processi metabolici sono disturbati. Lo shock è una malattia di natura polietiologica. A seconda dell'eziologia dell'occorrenza, i tipi di shock possono essere diversi. 1. Shock traumatico: 1) con lesioni meccaniche - fratture ossee, ferite, compressione dei tessuti molli, ecc.; 2) con ustioni (ustioni termiche e chimiche); 3) sotto l'influenza della bassa temperatura - shock da freddo; 4) in caso di lesioni elettriche - scossa elettrica. 2. Shock emorragico o ipovolemico: 1) si sviluppa a causa di sanguinamento, perdita di sangue acuta; 2) a seguito di una grave violazione del bilancio idrico, si verifica la disidratazione del corpo. 3. Shock settico (batterico-tossico) (processi purulenti generalizzati causati da microflora gram-negativa o gram-positiva). 4. Shock anafilattico. 5. Shock cardiogeno (infarto del miocardio, insufficienza cardiaca acuta). Considerato nella sezione condizioni di emergenza in cardiologia. In tutti i tipi di shock, il principale meccanismo di sviluppo è la vasodilatazione e, di conseguenza, aumenta la capacità del letto vascolare, l'ipovolemia - il volume del sangue circolante (BCC) diminuisce, poiché ci sono vari fattori: perdita di sangue, ridistribuzione di fluido tra il sangue e i tessuti o una mancata corrispondenza del volume sanguigno normale che aumenta la capacità vascolare. La conseguente discrepanza tra il BCC e la capacità del letto vascolare è alla base della diminuzione della gittata cardiaca e dei disturbi del microcircolo. Quest'ultimo porta a seri cambiamenti nel corpo, poiché è qui che si svolge la funzione principale della circolazione sanguigna: lo scambio di sostanze e ossigeno tra la cellula e il sangue. Si verifica un ispessimento del sangue, un aumento della sua viscosità e una microtrombosi intracapillare. Successivamente, le funzioni cellulari vengono interrotte fino alla loro morte. Nei tessuti, i processi anaerobici iniziano a prevalere su quelli aerobici, il che porta allo sviluppo dell'acidosi metabolica. L'accumulo di prodotti metabolici, principalmente acido lattico, aumenta l'acidosi. 28. Shock anafilattico Lo shock anafilattico è un complesso di varie reazioni allergiche di tipo immediato, che raggiungono un grado estremo di gravità. Esistono le seguenti forme di shock anafilattico: 1) forma cardiovascolare, in cui si sviluppa un'insufficienza circolatoria acuta, manifestata da tachicardia, spesso con disturbi del ritmo cardiaco, fibrillazione ventricolare e atriale e diminuzione della pressione sanguigna; 2) forma respiratoria, accompagnata da insufficienza respiratoria acuta: mancanza di respiro, cianosi, stridore, respiro gorgogliante, rantoli umidi nei polmoni. Ciò è dovuto a una violazione della circolazione capillare, gonfiore del tessuto polmonare, laringe, epiglottide; 3) forma cerebrale dovuta a ipossia, alterata microcircolazione ed edema cerebrale. In base alla gravità del corso, si distinguono 4 gradi di shock anafilattico. I grado (lieve) è caratterizzato da prurito della pelle, comparsa di eruzioni cutanee, mal di testa, vertigini, sensazione di vampate alla testa. II grado (gravità moderata) - Ai sintomi precedentemente indicati si uniscono edema di Quincke, tachicardia, abbassamento della pressione arteriosa, aumento dell'indice di Algover. Il grado III (grave) si manifesta con perdita di coscienza, insufficienza respiratoria e cardiovascolare acuta (mancanza di respiro, cianosi, respiro stridore, polso piccolo e rapido, forte diminuzione della pressione sanguigna, alto indice di Algover). Il grado IV (estremamente grave) è accompagnato da perdita di coscienza, grave insufficienza cardiovascolare: il polso non è determinato, la pressione sanguigna è bassa. Trattamento 1. Infusione endovenosa di adrenalina fino alla stabilizzazione emodinamica. Puoi usare la dopmin 10-15 mcg / kg / min e con sintomi di broncospasmo e b - adrenomimetici: alupent, brikanil flebo per via endovenosa. 2. Terapia infusionale in un volume di 2500-3000 ml con l'inclusione di poliglucina e reopoliglucina, a meno che la reazione non sia causata da questi farmaci. Sodio bicarbonato 4% 400 ml, soluzioni di glucosio per ripristinare bcc ed emodinamica. 3. Stabilizzatori di membrana per via endovenosa: prednisolone fino a 600 mg, acido ascorbico 500 mg, troxevasina 5 ml, sodio etamsilato 750 mg, citocromo C 30 mg (sono indicate le dosi giornaliere). 4. Broncodilatatori: eufillin 240-480 mg, noshpa 2 ml, alupent (brikanil) 0,5 mg flebo. 5. Antistaminici: difenidramina 40 mg (suprastin 60 mg, tavegil 6 ml), cimetidina 200-400 mg per via endovenosa (sono indicate le dosi giornaliere). 6. Inibitori della proteasi: trasylol 400 mila U, contrical 100 mila U. 29. Shock traumatico Lo shock traumatico è una condizione patologica e critica del corpo che si è verificata in risposta a una lesione, in cui le funzioni dei sistemi e degli organi vitali sono compromesse e inibite. Durante lo shock da trauma si distinguono le fasi torpide ed erettile. Al momento del verificarsi, lo shock può essere primario (1-2 ore) e secondario (più di 2 ore dopo l'infortunio). Stadio erettile o fase dell'occorrenza. La coscienza rimane, il paziente è pallido, irrequieto, euforico, inadeguato, può urlare, correre da qualche parte, scappare, ecc. In questa fase viene rilasciata adrenalina, per cui la pressione e il polso possono rimanere normali per qualche tempo. La durata di questa fase va da alcuni minuti e ore a diversi giorni. Ma nella maggior parte dei casi è breve. La fase torpida sostituisce quella erettile, quando il paziente diventa letargico e adinamico, la pressione sanguigna diminuisce e compare la tachicardia. Le stime della gravità della lesione sono fornite nella tabella. Valutazione dell'entità della gravità della lesione
Dopo aver calcolato i punti, il numero risultante viene moltiplicato per un coefficiente (da 1,2 a 2,0). Trattamento. Le principali direzioni di trattamento. 1. Eliminazione dell'azione dell'agente traumatico. 2. Eliminazione dell'ipovolemia. 3. Eliminazione dell'ipossia. 30. Shock emorragico Lo shock emorragico è una condizione di insufficienza cardiovascolare acuta che si sviluppa dopo la perdita di una quantità significativa di sangue e porta ad una diminuzione della perfusione degli organi vitali. Eziologia: lesioni con danno ai grandi vasi, ulcere gastriche e duodenali acute, rottura di un aneurisma aortico, pancreatite emorragica, rottura della milza o del fegato, rottura del tubo o gravidanza extrauterina, presenza di lobuli placentari nell'utero, ecc. In base ai dati clinici e all'entità della carenza di volume del sangue, si distinguono i seguenti gradi di gravità. 1. Non espresso - non ci sono dati clinici, il livello di pressione sanguigna è normale. Il volume della perdita di sangue è fino al 10% (500 ml). 2. Debole - tachicardia minima, leggera diminuzione della pressione sanguigna, alcuni segni di vasocostrizione periferica (mani e piedi freddi). Il volume della perdita di sangue va dal 15 al 25% (750-1200 ml). 3. Moderato: tachicardia fino a 100-120 battiti al minuto, diminuzione della pressione del polso, pressione sistolica 1-90 mm Hg. Art., ansia, sudorazione, pallore, oliguria. Il volume della perdita di sangue va dal 100 al 25% (35-1250 ml). 4. Grave - tachicardia superiore a 120 battiti al minuto, pressione sistolica inferiore a 60 mm Hg. Art., spesso non determinato dal tonometro, stupore, pallore estremo, estremità fredde, anuria. Il volume della perdita di sangue è superiore al 35% (più di 1750 ml). Laboratorio nell'analisi del sangue generale, una diminuzione del livello di emoglobina, eritrociti ed ematocrito. L'ECG mostra cambiamenti aspecifici nel segmento ST e nell'onda T, che sono dovuti a una circolazione coronarica insufficiente. Il trattamento dello shock emorragico comprende l'arresto dell'emorragia, l'uso della terapia infusionale per ripristinare il BCC, l'uso di vasocostrittori o vasodilatatori, a seconda della situazione. La terapia infusionale prevede la somministrazione endovenosa di liquidi ed elettroliti in un volume di 4 litri (soluzione salina, glucosio, albumina, poliglucina). In caso di sanguinamento, è indicata la trasfusione di sangue e plasma di un singolo gruppo in un volume totale di almeno 4 dosi (1 dose è 250 ml). Viene mostrata l'introduzione di farmaci ormonali, come stabilizzatori di membrana (prednisolone 90-120 mg). A seconda dell'eziologia, viene eseguita una terapia specifica. 31. Shock settico Lo shock settico è la penetrazione di un agente infettivo dalla sua fonte originaria nel sistema sanguigno e la sua diffusione in tutto il corpo. Gli agenti causali possono essere: batteri stafilococco, streptococco, pneumococco, meningococco ed enterococco, nonché Escherichia, Salmonella e Pseudomonas aeruginosa, ecc. Lo shock settico è accompagnato da disfunzione dei sistemi polmonare, epatico e renale, violazione della coagulazione del sangue sistema, che porta alla comparsa della sindrome tromboemorragica (sindrome di Machabeli), che si sviluppa in tutti i casi di sepsi. Il decorso della sepsi è influenzato dal tipo di agente patogeno, questo è particolarmente importante con i moderni metodi di trattamento. I risultati di laboratorio indicano un'anemia progressiva (dovuta all'emolisi e all'inibizione dell'ematopoiesi). Leucocitosi fino a 12 χ 109/l, tuttavia, nei casi più gravi, quando si forma una forte depressione degli organi ematopoietici, si può anche osservare la leucopenia. Sintomi clinici di shock batterico: brividi, febbre alta, ipotensione, pelle calda e secca - dapprima e poi - fredda e umida, pallore, cianosi, disturbo dello stato mentale, vomito, diarrea, oliguria. Caratterizzato da neutrofilia con spostamento della formula dei leucociti a sinistra fino ai mielociti; La VES aumenta a 30-60 mm/h o più. Il livello di bilirubina nel sangue è aumentato (fino a 35-85 µmol/l), che si applica anche al contenuto di azoto residuo nel sangue. La coagulazione del sangue e l'indice di protrombina sono ridotti (fino al 50-70%), il contenuto di calcio e cloruri è ridotto. La proteina totale del sangue si riduce, il che si verifica a causa dell'albumina e il livello di globuline (alfa globuline e β - globuline) aumenta. Nelle urine, proteine, leucociti, eritrociti e cilindri. Il livello di cloruri nelle urine è ridotto e l'urea e l'acido urico sono elevati. Il trattamento è principalmente di natura eziologica, pertanto, prima di prescrivere una terapia antibatterica, è necessario determinare l'agente patogeno e la sua sensibilità agli antibiotici. Gli agenti antimicrobici devono essere utilizzati alle dosi massime. Per trattare lo shock settico è necessario utilizzare antibiotici che coprano l'intero spettro dei microrganismi gram-negativi. La più razionale è l'associazione di ceftazidima e impinem, che si sono rivelate efficaci contro Pseudomonas aeruginosa. Farmaci come la clindamicina, il metronidazolo, la ticarcillina o l'imipinem vengono utilizzati come farmaci di scelta quando si verifica un agente patogeno resistente. Se gli stafilococchi vengono coltivati dal sangue, è imperativo iniziare il trattamento con farmaci a base di penicillina. Il trattamento dell'ipotensione consiste nella prima fase del trattamento nell'adeguatezza del volume del fluido intravascolare. Utilizzare soluzioni cristalloidi (soluzione isotonica di cloruro di sodio, Ringerlattato) o colloidi (albumina, destrano, polivinilpirrolidone). Il vantaggio dei colloidi è che quando vengono introdotti, le pressioni di riempimento richieste vengono raggiunte più rapidamente e rimangono tali per lungo tempo. Se non vi è alcun effetto, vengono utilizzati il supporto inotropo e (o) i farmaci vasoattivi. 32. Avvelenamento da alcol metilico L'alcol metilico viene assorbito attraverso tutte le vie: respiratoria, digestiva e transdermica. La dose letale di metanolo se assunta per via orale varia da 40 a 250 ml, ma l'assunzione anche di 10-20 ml può causare cecità. L'avvelenamento si verifica anche dopo l'assunzione di varie miscele alcoliche contenenti dall'1,5 al 2,5% di metanolo. Una volta assorbito, il metanolo si distribuisce in tutti i tessuti grazie alla sua solubilità in acqua. La quantità maggiore si accumula nei reni e nel tratto gastrointestinale, la quantità minore nel cervello, nei muscoli e nel tessuto adiposo. Le lesioni patologiche comprendono edema cerebrale e danni alla natura inizialmente infiammatoria e successivamente distrofica delle cellule gangliari retiniche. In alcuni casi, oltre a danni al sistema nervoso, si riscontrano lesioni degenerative del fegato, dei reni, dei polmoni e del muscolo cardiaco. Nell'effetto tossico del metanolo si può distinguere l'azione a due fasi. Nel periodo iniziale (fase I), il metanolo agisce sull'organismo come molecola intera e ha un effetto prevalentemente narcotico, ma più debole di quello dell'alcol etilico. Successivamente (fase II) si manifesta l'effetto dannoso dei prodotti di ossidazione. Nel quadro clinico si distinguono i periodi: intossicazione, benessere latente o relativo (che dura da alcune ore a 1-2 giorni), le principali manifestazioni di intossicazione e, con esito favorevole, sviluppo inverso. In base alla gravità si distinguono lieve, moderata (o oftalmica) e grave (o generalizzata). Con un lieve avvelenamento, si notano affaticamento rapido, mal di testa, nausea e uno stato di leggera intossicazione, che si verificano dopo un periodo di latenza da 30 minuti a diverse ore. L'assorbimento simultaneo di alcol etilico e metilico aumenta il periodo di latenza e riduce la gravità dell'avvelenamento. Trattamento 1. Fermare l'ingresso di veleno nel corpo. Cessazione dell'uso del veleno, rimozione dall'atmosfera contaminata, rimozione del veleno dalla pelle. 2. Rimozione del veleno non assorbito (dal tratto gastrointestinale): 1) sondare la lavanda gastrica; 2) l'uso di adsorbenti o lassativi salini; 3) clistere purificante o sifone. 3. Rimozione del veleno assorbito: 1) forzare la diuresi; 2) metodi di disintossicazione extracorporea (emosorbimento, emodialisi, dialisi peritoneale, chirurgia sostitutiva del sangue). 4. Terapia antidotica, ovvero neutralizzazione del veleno dovuta alla neutralizzazione fisica o chimica, nonché competizione con il veleno per i punti di applicazione. 5. Mantenimento delle funzioni vitali del corpo. 6. Normalizzazione dell'acqua-elettrolita, stato acido-base del corpo. 7. Trattamento delle conseguenze e delle complicanze a lungo termine. 33. Avvelenamento da alcol etilico e glicole etilenico Quando si assumono dosi tossiche - agitazione, atassia, stupore, coma con inibizione dei riflessi, odore di alcol dalla bocca, rossore al viso, congiuntivite, "gioco" delle pupille, vomito, minzione involontaria, tachicardia, respirazione "rauca" , collasso, vomito con possibile aspirazione di emetico wt. trattamento Lavanda gastrica attraverso una sonda spessa, seguita dall'introduzione di un lassativo salino, clistere a sifone. Per via sottocutanea 1 ml di una soluzione allo 0,1% di atropina, 2 ml di cordiamina, 1 ml di una soluzione al 20% di caffeina, con collasso - per via intramuscolare 1 ml di una soluzione all'1% di mezaton. In assenza di riflessi faringei - intubazione tracheale e ventilazione meccanica. Forzare la diuresi con la somministrazione simultanea di una soluzione di bicarbonato di sodio al 4% in un volume calcolato secondo la formula di Astrup, soluzioni di glucosio ipertoniche (10 e 20%) con insulina, vitamine del gruppo B e C, cocarbossilasi, acido nicotinico. Con depressione respiratoria - lentamente per via endovenosa 3-5 ml di soluzione all'1,5% di etimizolo, 10 ml di soluzione al 2,4% di aminofillina, 1 ml di soluzione al 5% di efedrina, inalazione di ossigeno. Con aspirazione - broncoscopia di sanificazione di emergenza. Antibiotici parenterali. Avvelenamento da glicole etilenico (antigelo). La dose letale media è di circa 100 ml. Viene rapidamente assorbito nel tratto digerente e distribuito a tutti i tessuti, creando la massima concentrazione nel cervello. Il principale effetto tossico si osserva nel parenchima renale, dove si sviluppa la necrosi dell'epitelio tubulare, l'edema interstiziale e focolai di necrosi emorragica nello strato corticale. L'edema si trova nel cervello. Nella clinica dell'intossicazione si distinguono 3 periodi: 1) iniziale - che dura fino a 12 ore, predominano i sintomi del danno al SNC dovuti al tipo di intossicazione da alcol; 2) neurotossico - quando i sintomi del danno al SNC progrediscono e si uniscono disturbi del sistema respiratorio e cardiovascolare; 3) nefrotossico - il 2°-5° giorno, il danno renale predomina nel quadro clinico dell'intossicazione. trattamento Lavanda gastrica con acqua o soluzione di bicarbonato di sodio al 2%, seguita dall'introduzione di 30 g di solfato di magnesio in 200 ml di acqua. Dentro 200 ml di una soluzione al 30% di alcol etilico. 3-5 g di bicarbonato di sodio in 100 ml di acqua. Bevanda abbondante. Per via intramuscolare 1-2 ml di cordiammina, 1 ml di una soluzione di caffeina al 20%. Per via endovenosa 400 ml di soluzione di glucosio al 5% con 5 ml di soluzione di acido ascorbico al 5% e 8 UI di insulina, miscela di glucosone-vocaina, 400 ml di poliglucina, 400 ml di emodez, 80-120 g di furosemide, 60-100 mg di prednisolone. 34. Avvelenamento da dicloroetano Le principali vie di ingresso sono il tratto digerente, il tratto respiratorio e la pelle. La dose letale di DCE per l'uomo quando somministrata per via orale è di 10-20 ml. L'effetto tossico del DCE è dovuto all'effetto narcotico sul sistema nervoso centrale, al danno al fegato, ai reni, al tratto gastrointestinale e a un pronunciato effetto sul sistema cardiovascolare. Nel quadro clinico, i sintomi principali sono: encefalopatia tossica, gastrite e gastroenterite tossica acuta, respirazione esterna alterata, epatite tossica, funzionalità renale compromessa. Nelle prime ore dopo la somministrazione compaiono vertigini, atassia, agitazione psicomotoria, convulsioni toniche cloniche, depressione della coscienza, fino al coma. Uno dei primi segni di avvelenamento sono i disturbi gastrointestinali sotto forma di nausea, vomito ripetuto con una miscela di bile. La violazione della funzione della respirazione esterna si verifica spesso secondo il tipo di aspirazione ostruttiva ed è associata ad aumento della salivazione, broncorrea e aspirazione. Si nota l'inibizione della funzione del centro respiratorio, lo sviluppo dell'ipertono dei muscoli respiratori e la rigidità del torace. trattamento In caso di avvelenamento con vapori - rimozione della vittima dall'area interessata, con depressione respiratoria IVL. Se il veleno penetra all'interno - lavanda gastrica attraverso una sonda densa, seguita dall'introduzione di 3-4 cucchiai di carbone attivo in polvere in 200 ml di acqua e 150-200 ml di olio di vaselina, clistere a sifone. Per via endovenosa 20-40 ml di soluzione di tiosolfato di sodio al 30%, per via intramuscolare 5 ml di soluzione di unitiolo al 5%. per via endovenosa 400 ml di poliglucina, 400 ml di hemodez, 400 ml di soluzione di glucosio al 5%, 80-120 mg di furosemide (lasix), 6-8 ml di soluzione al 5% di acido ascorbico. Per via intramuscolare 2 ml di cordiammina, con collasso - 1 ml di una soluzione all'1% di mezaton, 1 ml di una soluzione al 20% di caffeina, 100-150 mg di prednisolone. Con un aumento dell'insufficienza epatico-renale, viene eseguita una terapia specifica. Bolo endovenoso 400 ml di poliglucina, 400 ml di hemodez, 400 ml di glucosio al 5%, 80-120 mg di furosemide, 6-8 ml di acido ascorbico al 5%, 100-150 mg di prednisolone, per collasso 1 ml di 1% mesatone. Per via intramuscolare 2-4 ml di bromuro di tiamina al 6% e 2-4 ml di piridossina al 5%. Per l'agitazione psicomotoria, 1 ml di soluzione di fenozepam al 3%. Inalazione di ossigeno, in caso di depressione respiratoria - ventilazione meccanica attraverso un tubo di respirazione. Durante il primo giorno, il metodo più efficace e parsimonioso è la dialisi peritoneale. La composizione della soluzione per dialisi standard comprende: cloruro di potassio 0,3 g, cloruro di sodio 8,3 g, cloruro di magnesio 0,1 g, cloruro di calcio 0,3 g, glucosio 6 g per 1 litro di acqua. Allo stesso tempo, nella cavità addominale del paziente vengono iniettati fino a 2 litri di soluzione elettrolitica con l'aggiunta di 500 mila unità di penicillina e 1000 unità di eparina. 35. Avvelenamento con veleno di funghi e veleno di serpente Dopo un periodo di latenza che dura da 1-2 a 36 ore, compaiono crampi addominali, salivazione, nausea, vomito indomabile, diarrea, disidratazione, collasso, delirio, allucinazioni, convulsioni. Il 2-3 ° giorno - i fenomeni di insufficienza renale-epatica con anuria, azotemia, ittero. In caso di avvelenamento grave con linee e spugnole, è possibile l'emolisi. trattamento Lavaggio gastrico attraverso un tubo spesso, seguito dall'introduzione di 3-4 cucchiai di carbone attivo in polvere in 200 ml di acqua e 30 g di solfato di magnesio (sodio) in 100 ml di acqua, clistere a sifone. Per via sottocutanea 1 ml di una soluzione allo 0,1% di atropina, 2 ml di cordiamina. Nell'avvelenamento da spugnole, l'atropina non è usata come antidoto. Per via endovenosa 400 ml di poliglucina, 400 ml di gemodez, 400 ml di soluzione di glucosio al 5% con 4-6 ml di soluzione di acido ascorbico al 5%, 80-120 mg di furosemide (lasix). Per via intramuscolare 1-2 ml di una soluzione al 6% di bromuro di tiamina e 2 ml di una soluzione al 5% di piridossina cloridrato (non iniettare in una siringa). Sollievo dalla sindrome del dolore per via intramuscolare con l'introduzione di 1 ml di una soluzione allo 0,2% di platifillina, 2 ml di una soluzione al 2% di papaverina. Con convulsioni, agitazione psicomotoria - per via intramuscolare 1-2 ml di una soluzione al 3% di fenozepam o una miscela litica (1-2 ml di una soluzione al 2,5% di clorpromazina, 1-2 ml di una soluzione all'1% di difenidramina, 5-10 ml 25 % di soluzione di solfato di magnesio) sotto il controllo della pressione sanguigna. Forzare la diuresi. Nei casi più gravi - emoassorbimento, emodialisi precoce. Terapia sintomatica. Avvelenamento da veleno di serpente Dolore e gonfiore a rapida diffusione nella sede del morso, sonnolenza, depressione respiratoria, collasso, emolisi intravascolare con emoglobinuria, gravi emorragie sottocutanee, a volte convulsioni. Possibile insufficienza renale. Con un morso di cobra, i cambiamenti locali sono meno pronunciati, predominano i disturbi bulbari (disturbi del linguaggio e della deglutizione, ptosi, paralisi dei muscoli motori) e la depressione respiratoria. trattamento Aspirare il sangue e la linfa dalla ferita (entro e non oltre 30-60 minuti dopo il morso) formati nel sito del morso utilizzando una ventosa. Risciacquare la ferita con una soluzione all'1% di permanganato di potassio. Iniezione nella ferita di 0,3-0,5 ml di una soluzione allo 0,1% di adrenalina. Se possibile, somministrazione urgente di siero antiserpente specifico mono o polivalente dopo somministrazione endovenosa preliminare di 100-150 ml di idrocortisone o 50-100 ml di prednisolone. In caso di morsi di cobra - siero Anticobra per via endovenosa alla dose di 300 ml in combinazione con 1 ml di una soluzione allo 0,05% di prozerin e somministrazione ripetuta ogni 30 minuti con 1 ml di una soluzione allo 0,1% di atropina. 36. Avvelenamento da acido e arsenico L'inalazione dei vapori provoca irritazione degli occhi e delle prime vie respiratorie (lacrimazione, naso che cola, tosse, respiro corto). Possibile arresto respiratorio riflesso. Dopo un periodo di latenza (da 2 a 24 ore), si forma polmonite tossica o edema polmonare tossico. A colpo in occhi, su pelle - ustioni chimiche. Se ingerito - un'ustione chimica della cavità orale, faringe, esofago, stomaco, possibile gonfiore della laringe con insufficienza respiratoria. Vomito ripetuto con sangue, irritazione peritoneale e occasionalmente perforazione dell'esofago o dello stomaco. Collasso, shock, sindrome emorragica. Possibile emolisi intravascolare, nefrosi emoglobinurica con insufficienza renale acuta (renale-epatica). La lavanda gastrica tubeless e il vomito artificiale sono pericolosi a causa della possibilità di bruciare nuovamente l'esofago e l'aspirazione acida. Non iniettare soluzioni saline lassative e alcaline. trattamento Lavaggio gastrico attraverso un tubo spesso con acqua fredda dopo un'iniezione endovenosa o intramuscolare preliminare di 1-2 ml di una soluzione al 2% di promedol. Dentro pezzi di ghiaccio, Almagel A 15-20 ml ogni ora. Per via endovenosa 800 ml di poliglucina, 400 ml di emodez, miscela di glucosone-vocaina (400 ml di soluzione di glucosio al 5% con 25 ml di soluzione di novocaina al 2%), 50-150 mg di prednisolone o 150-250 mg di idrocortisone, 10 mila unità di eparina, 80-120 mg di furosemide (Lasix). Il sollievo dal dolore si ottiene mediante iniezione endovenosa di 1-2 ml di soluzione di fentanil allo 0,005% e 2-4 ml di soluzione di droperidolo allo 0,25%, per dolore addominale persistente - iniezione intramuscolare di 1-2 ml di soluzione di platifillina allo 0,2%, 2 ml di 2 % soluzione di papaverina. Inalazione di ossigeno con agente antischiuma. Con crescente gonfiore della laringe - per via endovenosa 200-400 mg di prednisolone, 1-2 ml di una soluzione all'1% di difenidramina, 10-20 ml di una soluzione al 2,4% di aminofillina, 1-2 ml di una soluzione al 5% di efedrina . Se non vi è alcun effetto, tracheostomia, inalazione di ossigeno e, se indicato, ventilazione meccanica. Avvelenamento con arsenico e suoi composti: sapore metallico in bocca, dolore addominale, vomito, feci molli, grave disidratazione, convulsioni, tachicardia, diminuzione della pressione sanguigna, coma, insufficienza renale acuta. Nell'avvelenamento da idrogeno da arsenico si sviluppano emolisi intravascolare ed emoglobinuria. trattamento Lavaggio gastrico attraverso una sonda densa (2-3 volte al giorno) con l'introduzione all'inizio e alla fine del lavaggio 50 ml di una soluzione al 5% di unithiol, clisteri ripetuti a sifone con l'aggiunta di unithiol. Continuazione della terapia antidoto per via endovenosa o intramuscolare con l'introduzione di una soluzione al 5% di unithiol (fino a 300 ml al giorno), gocciolamento endovenoso di 20 ml di tetacina di calcio al 10% (ED1A) in 400 ml di una soluzione di glucosio al 5%. 37. Avvelenamento con alcali, atropina, cannabis avvelenamento da alcali Se ingerito, si sviluppa un'ustione chimica della mucosa della cavità orale, dell'esofago e dello stomaco. Dolore lungo l'esofago e nell'addome, vomito con una miscela di sangue, sanguinamento esofageo-gastrico. Possibile perforazione dell'esofago, stomaco con sviluppo di mediastinite, peritonite. Con un'ustione della laringe - raucedine della voce, afonia, difficoltà (stridore) di respirazione. Nei casi più gravi - shock da ustione, oliguria. Il contatto con la pelle provoca ustioni chimiche. Trattare come in avvelenamento da acido. Avvelenamento da atropina Secchezza delle fauci, raucedine, pelle secca e iperemica, pupille dilatate, mancanza di respiro, palpitazioni, tachicardia, sete, nausea, difficoltà a urinare. In grave avvelenamento - sono possibili agitazione psicomotoria, delirio, allucinazioni, convulsioni, disturbi del ritmo cardiaco, coma, collasso. trattamento Se necessario - lavanda gastrica attraverso una sonda densa, riccamente lubrificata con olio di vaselina, l'introduzione di 3-4 cucchiai. l. carbone attivo in polvere in 200 ml di acqua e 30 mg di solfato di magnesio in 100 ml di acqua. per via endovenosa 2-4 ml di soluzione di proserina allo 0,05%, 400-800 ml di soluzione di glucosio al 5%, 40-80 mg di furosemide (lasix). Bevanda abbondante. Sollievo dall'agitazione psicomotoria e dalle convulsioni per via intramuscolare somministrando 1-2 ml di una soluzione al 3% di fenozepam o una miscela litica (2 ml di una soluzione al 2,5% di aminazina, 2 ml di una soluzione all'1% di difenidramina e 10 ml di una soluzione al 25 % soluzione di solfato di magnesio ) o 1-2 g di cloralio idrato in un clistere con 1-2 g di amido per 25-50 ml di acqua, per via endovenosa 10-15 ml di una soluzione al 20% di idrossibutirrato di sodio, 2-4 ml di una soluzione allo 0,5% di seduxen. Con grave tachicardia, extrasistole - anaprilina per via endovenosa (1-2 ml di una soluzione allo 0,25%) o una compressa di anaprilina (40 mg) sotto la lingua. Con il collasso - per via endovenosa 1 ml di una soluzione all'1% di mezaton in 10 ml di una soluzione allo 0,9% di cloruro di sodio. Con una forte ipertermia - per via intramuscolare 2 ml di una soluzione al 50% di analgin, impacchi di ghiaccio su grandi vasi e testa, impacchi umidi. Avvelenamento da cannabis (hashish, marijuana, marijuana, piano) C'è euforia, agitazione psicomotoria, allucinazioni visive vivide, pupille dilatate, tinnito. Successivamente debolezza, letargia, depressione dell'umore, sonnolenza, bradicardia, ipotermia. trattamento In caso di avvelenamento orale - lavanda gastrica attraverso una sonda spessa, seguita dall'introduzione di 3-4 cucchiai. l. carbone attivo in polvere in 200 ml di acqua. Per via endovenosa 400-800 ml di una soluzione di glucosio al 5% con 5-10 ml di una soluzione al 5% di acido ascorbico e 8-16 unità di insulina, 40-80 mg di furosemide (lasix), per via intramuscolare 2 ml di una soluzione al 6% di bromuro di tiamina. 38. Avvelenamento con cocaina, dicaina, analgesici narcotici avvelenamento da cocaina Si manifesta clinicamente con agitazione generale, mal di testa, arrossamento del viso, pupille dilatate, tachicardia, aumento della respirazione, aumento della pressione sanguigna, allucinazioni. Nei casi più gravi - convulsioni, coma, paralisi respiratoria, collasso. Lavanda gastrica ripetuta attraverso una sonda spessa con una soluzione allo 0,1% di permanganato di potassio, seguita dall'introduzione di 3-4 cucchiai. l. carbone attivo in polvere in 200 ml di acqua e 30 g di solfato di magnesio in 100 ml di acqua. Per via endovenosa 400 ml di gemodez, 400 ml di soluzione di glucosio al 5% con 5-10 ml di soluzione di acido ascorbico al 5%, 40-80 mg di furosemide (lasix). Quando è eccitato - fissando la vittima, per via intramuscolare 1-2 ml di una soluzione al 3% di fenozepam o una miscela litica (1-2 ml di una soluzione al 2,5% di clorpromazina, 2 ml di una soluzione all'1% di difenidramina e 5-10 ml del 25% - una soluzione di solfato di magnesio) sotto il controllo della pressione sanguigna. Con le convulsioni, 1-2 g di cloralio idrato vengono somministrati in un clistere con 1-2 g di amido in 25-50 ml di acqua, lentamente per via endovenosa 15-20 ml di una soluzione di ossibutirrato di sodio al 20%, se non vi è alcun effetto, lentamente per via intramuscolare fino a 20 ml di soluzione al 2,5% di sodio tiopentale o esenale. Con lo sviluppo di un coma, un impacco di ghiaccio sulla testa, per via endovenosa 40 ml di una soluzione di glucosio al 40% con 4-6 ml di una soluzione al 5% di acido ascorbico e 8 unità di insulina, per via endovenosa lentamente o per via intramuscolare 2-4 ml di una soluzione al 6% di bromuro di tiamina e 2-4 ml di una soluzione al 5% di piridossina cloridrato, 80-120 mg di furosemide. Con grave depressione respiratoria, viene eseguita la ventilazione meccanica, per via endovenosa lentamente 2 ml di cordiamina, inalazione di ossigeno. Avvelenamento con analgesici narcotici (morfina, omnopon, droperidolo) Sonnolenza o perdita di coscienza, costrizione pupillare, ipertono muscolare (talvolta convulsioni), depressione respiratoria, bradicardia, collasso. La paralisi respiratoria è possibile con la conservazione della coscienza del paziente. Lavaggio gastrico attraverso una sonda spessa (mantenendo la coscienza), seguito dall'introduzione di 3-4 cucchiai. l. carbone attivo in polvere e 30 g di solfato di sodio, clistere a sifone. Per via endovenosa 400 ml di gemodez, 400 ml di poliglucina, 400 ml di soluzione di glucosio al 5%, 60-80 mg di furosemide (lasix). Per via sottocutanea 1-2 ml di una soluzione allo 0,1% di atropina, 1-2 ml di cordiamina, 1 ml di una soluzione al 20% di caffeina. Con lo sviluppo di un coma, un impacco di ghiaccio sulla testa, per via endovenosa 40 ml di una soluzione di glucosio al 40% con 5-10 ml di una soluzione al 5% di acido ascorbico e 8 unità di insulina, per via endovenosa lentamente o per via intramuscolare 2-4 ml di una soluzione al 6% di bromuro di tiamina e 2-4 ml di una soluzione al 5% di piridossina cloridrato, 80-120 mg di furosemide (lasix). Se necessario - cateterizzazione vescicale ed estrazione delle urine. Con depressione respiratoria - IVL, inalazione di ossigeno. Emoassorbimento (2-3 volte al giorno fino al ripristino della coscienza). 39. Dolore Il dolore è uno stato sensoriale ed emotivo spiacevole causato da effetti patologici reali o potenziali sui tessuti. Nel SNC, il dolore è condotto lungo due vie principali. Percorso specifico: le corna posteriori del midollo spinale, i nuclei specifici del talamo, la corteccia del giro centrale posteriore. Questo percorso è a basso neurone, veloce, conduce il dolore di soglia, emotivamente incolore, precisamente localizzato (dolore epicritico). Modo non specifico: le corna posteriori del midollo spinale, i nuclei non specifici del talamo, la corteccia dei lobi frontali e parietali in modo diffuso. Conduce dolore sottosoglia, emotivamente colorato, scarsamente localizzato. È lento, multineuronale, poiché forma numerose collaterali al midollo allungato, alla formazione reticolare, al sistema limbico e all'ippocampo. Gli impulsi del dolore sottosoglia subiscono la somma nel talamo. Gli impulsi condotti lungo la via del dolore aspecifico eccitano i centri emotivi del sistema limbico, i centri autonomici dell'ipotalamo e il midollo allungato. Pertanto, il dolore è accompagnato da paura, esperienze dolorose, aumento della respirazione, polso, aumento della pressione sanguigna, dilatazione della pupilla, disturbi dispeptici. L'azione del sistema nocicettivo del dolore è contrastata dal sistema antinocecettivo, i cui neuroni principali sono localizzati nella sostanza grigia periacqueduttale (l'acquedotto di Sylvius collega il III e il IV ventricolo). I loro assoni formano percorsi discendenti verso il midollo allungato e il midollo spinale e percorsi ascendenti verso la formazione reticolare, il talamo, l'ipotalamo, il sistema limbico, i gangli della base e la corteccia. I mediatori di questi neuroni sono i pentapeptidi: methenkephalin e leuenkephalin, che hanno rispettivamente metionina e leucina come amminoacidi terminali. Le encefaline eccitano i recettori degli oppiacei. Nelle sinapsi encefalinergiche, i recettori degli oppiacei si trovano sulla membrana postsinaptica, ma la stessa membrana è presinaptica per altre sinapsi. I recettori degli oppiacei sono associati all'adenilato ciclasi e ne causano l'inibizione interrompendo la sintesi di cAMP nei neuroni. Di conseguenza, l'ingresso del calcio e il rilascio di mediatori, inclusi i mediatori del dolore - diminuiscono i peptidi: sostanza P, colecistochinina, somatostatina, acido glutammico. I recettori degli oppiacei sono eccitati non solo dai mediatori - le encefaline, ma anche da altri componenti del sistema antinocecettivo - gli ormoni cerebrali (endorfine). Gli agonisti peptidici dei recettori degli oppiacei si formano durante la proteolisi delle sostanze peptidiche del cervello: proopiocortina, proencefaline A e B. Tutti questi peptidi si formano nell'ipotalamo. I recettori degli oppiacei eccitano i recettori in tutte le strutture cerebrali coinvolte nella conduzione e nella percezione del dolore, nella formazione di reazioni emotivamente colorate al dolore. Allo stesso tempo, il rilascio dei mediatori del dolore diminuisce e tutte le reazioni che accompagnano il dolore sono indebolite. 40. Farmaci analgesici L'analgesico (acido acetilsalicilico, paracetamolo, morfina) è un farmaco che riduce il dolore di varia origine. I farmaci che riducono il dolore provocato solo da un determinato fattore causale o eliminano una specifica sindrome del dolore, ad esempio antiacidi, ergotamina (emicrania), carbamazepina (nevralgia), nitroglicerina (angina pectoris), non appartengono agli analgesici classici. I corticosteroidi sopprimono la risposta infiammatoria e il dolore che ne deriva, ma nonostante il loro uso diffuso per questi scopi, non rappresentano nemmeno gli analgesici classici. Gli analgesici si classificano in narcotici, agendo sulle strutture del SNC e provocando sonnolenza, come gli oppioidi, e non narcotici, agendo principalmente sulle strutture periferiche, come il paracetamolo, l'acido acetilsalicilico. Ulteriori farmaci che migliorano l'effetto degli analgesici I farmaci di questo gruppo non sono analgesici di per sé, ma vengono utilizzati in combinazione con analgesici per il dolore, in quanto possono modificare l'atteggiamento nei confronti del dolore, la sua percezione e il livello di ansia, paura, depressione (gli antidepressivi triciclici possono anche causare una diminuzione della necessità di morfina in un paziente in stato terminale). Tali farmaci possono essere psicofarmaci, nonché quelli che influenzano i meccanismi del dolore, ad esempio eliminando lo spasmo dei muscoli lisci e striati. Gli analgesici narcotici sono farmaci erboristici e sintetici che riducono selettivamente la percezione del dolore, aumentano la tolleranza al dolore riducendo la colorazione emotiva del dolore e il suo accompagnamento vegetativo, provocano euforia e tossicodipendenza. Classificazione degli analgesici narcotici e dei loro antagonisti 1. Derivati piperidina-fenantrene: 1) morfina; 2) codeina (metilmorfina, 5-7 volte più debole della morfina come analgesico); 3) etilmorfina (dionina, uguale in forza alla morfina). 2. Derivati della fenilpiperidina: 1) promedol (3-4 volte più debole della morfina); 2) fentanil (100-400 volte più forte della morfina). 3. Derivati del difenilmetano: 1) piritrammide (dipidolor) - uguale alla morfina; 2) tramadolo (tramal) - leggermente inferiore alla morfina. 4. Agonisti-antagonisti: 1) agonisti del recettore degli oppiacei e antagonisti del recettore degli oppiacei - buprenorfina (norfina) (25-30 volte più forte della morfina); 2) agonisti dei recettori degli oppiacei e antagonisti dei recettori degli oppiacei - pentazocina (lexir) (2-3 volte più debole della morfina) e butorfanolo (moradolo) (uguale alla morfina). 41. Fasi dell'anestesia L'anestesia generale, o anestesia, è uno stato del corpo caratterizzato da un arresto temporaneo della coscienza di una persona, dalla sua sensibilità al dolore e dai suoi riflessi, nonché dal rilassamento dei muscoli dei muscoli scheletrici, causato dall'azione degli analgesici narcotici su il sistema nervoso centrale. A seconda delle vie di somministrazione di sostanze stupefacenti nel corpo, si distinguono l'anestesia per inalazione e non per inalazione. Ci sono 4 fasi dell'anestesia: 1) analgesia; 2) eccitazione; 3) stadio chirurgico, suddiviso in 4 livelli; 4) fase del risveglio. Fase di analgesia Il paziente è cosciente, ma si nota un po' di letargia, sonnecchia, risponde a domande a monosillabi. La sensibilità superficiale e al dolore è assente, ma per quanto riguarda la sensibilità tattile e termica, sono preservate. In questa fase vengono eseguiti interventi chirurgici a breve termine, come apertura di flemmone, ascessi, studi diagnostici, ecc. La fase è a breve termine, della durata di 3-4 minuti. Fase di eccitazione In questa fase, i centri della corteccia cerebrale sono inibiti e i centri sottocorticali in questo momento sono in uno stato di eccitazione. Allo stesso tempo, la coscienza del paziente è completamente assente, si nota un'eccitazione motoria e vocale pronunciata. I pazienti iniziano a urlare, tentano di alzarsi dal tavolo operatorio. Si nota iperemia della pelle, il polso diventa frequente, la pressione sanguigna sistolica aumenta. La pupilla dell'occhio si allarga, ma la reazione alla luce persiste, si nota la lacrimazione. Spesso c'è tosse, aumento della secrezione bronchiale, a volte vomito. L'intervento chirurgico sullo sfondo dell'eccitazione non può essere eseguito. Durante questo periodo, dovresti continuare a saturare il corpo con un narcotico per migliorare l'anestesia. La durata della fase dipende dalle condizioni generali del paziente e dall'esperienza dell'anestesista. In genere, la durata dell'eccitazione è di 7-15 minuti. Fase chirurgica Con l'inizio di questa fase dell'anestesia, il paziente si calma, la respirazione diventa calma e uniforme, la frequenza cardiaca e la pressione sanguigna si avvicinano alla normalità. Durante questo periodo, sono possibili interventi chirurgici. A seconda della profondità dell'anestesia, si distinguono 4 livelli e lo stadio III dell'anestesia. Primo livello: il paziente è calmo, il numero dei movimenti respiratori, il numero delle contrazioni cardiache e la pressione sanguigna si stanno avvicinando ai valori iniziali. La pupilla inizia gradualmente a restringersi, la sua reazione alla luce viene preservata. Secondo livello: il movimento dei bulbi oculari è interrotto, sono fissati in posizione centrale. Le pupille si dilatano e la loro reazione alla luce si indebolisce. Il tono muscolare è ridotto, il che consente operazioni addominali. Il terzo livello è caratterizzato come anestesia profonda. Allo stesso tempo, le pupille degli occhi si dilatano con una reazione a un forte stimolo luminoso. L'anestesia al quarto livello è pericolosa per la vita del paziente, poiché può verificarsi un arresto respiratorio e circolatorio. Fase di risveglio Non appena l'introduzione di stupefacenti si interrompe, la loro concentrazione nel sangue diminuisce e il paziente attraversa tutte le fasi dell'anestesia in ordine inverso, si verifica il risveglio. 42. Preparazione del paziente per l'anestesia L'anestesista assume un ruolo diretto e spesso principale nella preparazione del paziente all'anestesia e alla chirurgia. Momento d'obbligo è l'esame del paziente prima dell'intervento, ma allo stesso tempo è importante non solo la malattia di base, per la quale si vuole operare, ma anche la presenza di patologie concomitanti, che l'anestesista chiede in dettaglio. . È necessario sapere come è stato trattato il paziente per queste malattie, l'effetto del trattamento, la durata del trattamento, la presenza di reazioni allergiche, il tempo dell'ultima esacerbazione. Se il paziente subisce un intervento chirurgico in modo pianificato, se necessario, viene eseguita la correzione delle malattie concomitanti esistenti. L'igiene del cavo orale è importante in presenza di denti sciolti e cariati, poiché possono essere un'ulteriore e indesiderata fonte di infezione. L'anestesista scopre e valuta lo stato psiconevrologico del paziente. Quindi, ad esempio, nella schizofrenia, l'uso di droghe allucinogene (ketamina) è controindicato. La chirurgia durante il periodo di psicosi è controindicata. In presenza di un deficit neurologico, viene preliminarmente corretto. La storia allergica è di grande importanza per l'anestesista, per questo viene specificata l'intolleranza ai farmaci, oltre che agli alimenti, ai prodotti chimici per la casa, ecc. Se il paziente ha un'anemnesi allergica aggravata, nemmeno ai farmaci, durante l'anestesia può svilupparsi una reazione allergica fino allo shock anafilattico. Pertanto, gli agenti desensibilizzanti (difenidramina, suprastin) vengono introdotti nella premedicazione in grandi quantità. Un punto importante è la presenza di un paziente in passato operazioni e anestesia. Si scopre che cos'era l'anestesia e se ci sono state complicazioni. Si richiama l'attenzione sulla condizione somatica del paziente: la forma del viso, la forma e il tipo del torace, la struttura e la lunghezza del collo, la gravità del grasso sottocutaneo, la presenza di edema. Tutto ciò è necessario per scegliere il giusto metodo di anestesia e farmaci. La prima regola per preparare un paziente all'anestesia durante qualsiasi operazione e quando si utilizza qualsiasi anestesia è la pulizia del tratto gastrointestinale (lo stomaco viene lavato attraverso il tubo, vengono eseguiti clisteri purificanti). Per sopprimere la reazione psico-emotiva e sopprimere l'attività del nervo vago, prima dell'intervento chirurgico, al paziente vengono somministrati farmaci: la premedicazione. Di notte, il fenazepam viene prescritto per via intramuscolare. Ai pazienti con un sistema nervoso labile vengono prescritti tranquillanti (seduxen, relanium) il giorno prima dell'intervento chirurgico. 40 minuti prima dell'intervento, gli analgesici narcotici vengono iniettati per via intramuscolare o sottocutanea: 1 ml di una soluzione all'1-2% di promololo o 1 ml di pentozocina (lexir), 2 ml di fentanil o 1 ml di morfina all'1%. Per sopprimere la funzione del nervo vago e ridurre la salivazione, vengono somministrati 0,5 ml di una soluzione allo 0,1% di atropina. 43. Anestesia endovenosa e inalatoria I vantaggi dell'anestesia generale per via endovenosa sono la rapida introduzione del paziente in anestesia. Con questo tipo di anestesia, non c'è eccitazione e il paziente si addormenta rapidamente. Ma i narcotici utilizzati per la somministrazione endovenosa creano un'anestesia a breve termine, quindi non possono essere utilizzati nella loro forma pura come mononarcosi per operazioni a lungo termine. I barbiturici - sodio tiopentale ed esenale - sono in grado di indurre rapidamente il sonno narcotico, mentre non c'è stadio di eccitazione e il risveglio è veloce. I quadri clinici dell'anestesia condotta con sodio tiopentale ed esenale sono simili. Geksenal ha un effetto meno inibitorio sul centro respiratorio. Vengono utilizzate soluzioni appena preparate di derivati dell'acido barbiturico. In chirurgia, l'anestesia con barbiturici come mononarcosi viene utilizzata per operazioni a breve termine che non superano i 20 minuti di durata (ad esempio apertura di ascessi, flemmone, riduzione delle lussazioni, manipolazioni diagnostiche e riposizionamento di frammenti ossei). I derivati dell'acido barbiturico sono utilizzati anche per l'anestesia di induzione. L'idrossibutirrato di sodio viene somministrato per via endovenosa molto lentamente. Il farmaco crea un'anestesia superficiale, quindi viene spesso utilizzato in combinazione con altri narcotici, come i barbiturici - il propanidide. Viene spesso utilizzato per l'anestesia di induzione. La ketamina può essere utilizzata per la mononarcosi e per l'anestesia di induzione. Il farmaco provoca un sonno superficiale, stimola l'attività del sistema cardiovascolare (la pressione sanguigna aumenta, il polso accelera). L'anestesia per inalazione viene eseguita con l'aiuto di liquidi (volatili) facilmente evaporabili - etere, alotano, metossiflurano (pentran), tricloroetilene, cloroformio o sostanze stupefacenti gassose - protossido di azoto, ciclopropano. Con il metodo endotracheale dell'anestesia, la sostanza narcotica entra nel corpo dalla macchina per anestesia attraverso un tubo inserito nella trachea. Il vantaggio del metodo sta nel fatto che fornisce la pervietà libera delle vie respiratorie e può essere utilizzato in operazioni su collo, viso, testa, elimina la possibilità di aspirazione di vomito, sangue; riduce la quantità di droga utilizzata; migliora lo scambio di gas riducendo lo spazio "morto". L'anestesia endotracheale è indicata per interventi chirurgici importanti, viene utilizzata come anestesia multicomponente con miorilassanti (anestesia combinata). L'uso totale di diversi farmaci a piccole dosi riduce gli effetti tossici sul corpo di ciascuno di essi. La moderna anestesia mista viene utilizzata per fornire analgesia, spegnere la coscienza, rilassamento. L'analgesia e lo spegnimento della coscienza vengono effettuati utilizzando una o più sostanze stupefacenti, inalate o non. L'anestesia viene eseguita al primo livello della fase chirurgica. Il rilassamento muscolare, o rilassamento, si ottiene con la somministrazione frazionata di miorilassanti. 44. Fasi dell'anestesia Ci sono tre fasi dell'anestesia. 1. Introduzione all'anestesia. L'anestesia introduttiva può essere eseguita con qualsiasi sostanza narcotica, contro la quale si verifica un sonno anestetico piuttosto profondo senza fase di eccitazione. Vengono utilizzati principalmente barbiturici, fentanil in combinazione con sombrevin, macinato con sombrevin. Viene spesso utilizzato anche il tiopentale di sodio. I farmaci vengono utilizzati sotto forma di una soluzione all'1%, vengono somministrati per via endovenosa alla dose di 400-500 mg. Sullo sfondo dell'anestesia di induzione, vengono somministrati miorilassanti e viene eseguita l'intubazione tracheale. 2. Mantenimento dell'anestesia. Per mantenere l'anestesia generale, è possibile utilizzare qualsiasi narcotico in grado di proteggere il corpo da traumi chirurgici (alotano, ciclopropano, protossido di azoto con ossigeno), nonché neurolepta-nalgesia. L'anestesia viene mantenuta al primo e al secondo livello della fase chirurgica e per eliminare la tensione muscolare vengono somministrati miorilassanti, che causano mioplegia di tutti i gruppi muscolari scheletrici, compresi quelli respiratori. Pertanto, la condizione principale per il moderno metodo combinato di anestesia è la ventilazione meccanica, che viene eseguita spremendo ritmicamente una borsa o una pelliccia o utilizzando un apparato di respirazione artificiale. Recentemente, la neuroleptanalgesia più diffusa. Con questo metodo, per l'anestesia vengono utilizzati protossido di azoto con ossigeno, fentanil, droperidolo, miorilassanti. Anestesia introduttiva endovenosa. L'anestesia viene mantenuta mediante inalazione di protossido di azoto con ossigeno in un rapporto di 2: 1, somministrazione endovenosa frazionata di fentanil e droperidolo 1-2 ml ogni 15-20 minuti. Con l'aumento della frequenza cardiaca, viene somministrato il fentanil, con un aumento della pressione sanguigna - droperidolo. Questo tipo di anestesia è più sicuro per il paziente. Il fentanil migliora il sollievo dal dolore, il droperidolo sopprime le reazioni vegetative. 3. Ritiro dall'anestesia. Entro la fine dell'operazione, l'anestesista interrompe gradualmente la somministrazione di sostanze stupefacenti e miorilassanti. La coscienza ritorna al paziente, la respirazione indipendente e il tono muscolare vengono ripristinati. I criteri per valutare l'adeguatezza della respirazione spontanea sono indicatori di PO2, PCO2 e pH. Dopo il risveglio, il ripristino della respirazione spontanea e del tono muscolare scheletrico, l'anestesista può estubare il paziente e trasportarlo per un'ulteriore osservazione nella sala di risveglio. Durante l'anestesia generale, i principali parametri dell'emodinamica vengono costantemente determinati e valutati. Misurare la pressione sanguigna, la frequenza cardiaca ogni 10-15 minuti. Nelle persone con malattie del sistema cardiovascolare, così come durante le operazioni toraciche, è necessario monitorare costantemente la funzione del muscolo cardiaco. L'osservazione elettroencefalografica può essere utilizzata per determinare il livello di anestesia. Per controllare la ventilazione polmonare e i cambiamenti metabolici durante l'anestesia e l'intervento chirurgico, è necessario studiare lo stato acido-base (PO2, PCO2, pH, BE). 45. Complicazioni dell'anestesia Complicazioni durante l'anestesia possono verificarsi a causa di una tecnica di anestesia impropria o dell'effetto degli anestetici sugli organi vitali. Una di queste complicazioni è il vomito. All'inizio dell'introduzione dell'anestesia, il vomito può essere associato alla natura della malattia dominante (stenosi pilorica, ostruzione intestinale) o all'effetto diretto del farmaco sul centro del vomito. Sullo sfondo del vomito, l'aspirazione è pericolosa: l'ingresso del contenuto gastrico nella trachea e nei bronchi. I contenuti gastrici che hanno una reazione acida pronunciata, che cadono sulle corde vocali e poi penetrano nella trachea, possono portare a laringospasmo o broncospasmo, con conseguente insufficienza respiratoria con successiva ipossia - questa è la cosiddetta sindrome di Mendelssohn, accompagnata da cianosi, broncospasmo, tachicardia. Pericoloso può essere il rigurgito: lancio passivo del contenuto gastrico nella trachea e nei bronchi. Possono verificarsi complicazioni dell'apparato respiratorio a causa della ridotta pervietà delle vie aeree. Ciò potrebbe essere dovuto a difetti nella macchina per anestesia. Le complicanze dell'intubazione tracheale eseguita mediante laringoscopia diretta possono essere raggruppate come segue: 1) danno ai denti da parte della lama del laringoscopio; 2) danno alle corde vocali; 3) introduzione di un tubo endotracheale nell'esofago; 4) introduzione di un tubo endotracheale nel bronco destro; 5) uscita del tubo endotracheale dalla trachea o piegamento dello stesso. Disturbi del ritmo cardiaco (tachicardia ventricolare, extrasistole, fibrillazione ventricolare) possono verificarsi per una serie di motivi: 1) ipossia e ipercapnia derivanti da intubazione prolungata o ventilazione insufficiente durante l'anestesia; 2) sovradosaggio di sostanze stupefacenti - barbiturici, alotano; 3) l'uso dell'adrenalina sullo sfondo del fluorotano, che aumenta la sensibilità del fluorotano alle catecolamine. Danno ai nervi periferici Questa complicanza si verifica un giorno o più dopo l'anestesia. Molto spesso, i nervi degli arti superiori e inferiori e il plesso brachiale sono danneggiati. Questo è il risultato di una posizione errata del paziente sul tavolo operatorio (abduzione del braccio superiore a 90 dal corpo, braccio dietro la testa, fissaggio del braccio all'arco del tavolo operatorio, appoggio delle gambe sui supporti senza imbottitura). La corretta posizione del paziente sul lettino elimina la tensione dei tronchi nervosi. Il trattamento viene effettuato da un neuropatologo e un fisioterapista. 46. Anestesia locale Anestesia di superficie Questo tipo di anestesia viene effettuato per contatto della sostanza anestetica con l'uno o l'altro organo, la sua superficie. A tale scopo, una soluzione all'1-3% di cocaina, una soluzione allo 0,25-2% di dicaina, una soluzione all'1-2% di lidocaina, una soluzione all'1-5% di trimecaina e una soluzione allo 0,5-2% di piromecaina. La maggior parte degli anestetici locali si lega ai canali del sodio inattivati, impedendo la loro attivazione e l'ingresso del sodio nella cellula durante la depolarizzazione della membrana, ottenendo così un effetto analgesico. La tecnica dell'anestesia superficiale è semplice e consiste nel lubrificare, instillare una soluzione o spruzzarla utilizzando speciali pistole a spruzzo. L'inizio dell'azione dell'anestetico dipende dal pH, con un pH basso che richiede più tempo per avere effetto rispetto a un pH alto. La durata dell'azione dell'anestetico dipende dal grado del suo legame con le proteine. Questo tipo di anestesia viene utilizzato nelle manipolazioni diagnostiche e in oftalmologia, otorinolaringoiatria. Anestesia regionale L'anestesia regionale comprende plesso, conduzione, epidurale, paravertebrale e altri tipi di anestesia. A differenza dell'anestesia generale, l'anestesia regionale fornisce un'adeguata analgesia chirurgica a causa del blocco periferico degli impulsi del dolore pur mantenendo le normali funzioni vitali. L'anestesia regionale è tecnicamente difficile e richiede un'accurata conoscenza della posizione anatomica e topografica del plesso nervoso o conduttore nervoso, un chiaro orientamento nei punti di identificazione permanente (sporgenza ossea, arterie, muscoli), la capacità di valutare la resistenza dei tessuti e le sensazioni del paziente. Per disattivare la sensibilità al dolore, è sufficiente introdurre una soluzione all'1% di trimecaina (lidocaina) e per disattivare la sensibilità propriocettiva e ottenere il rilassamento muscolare, è necessario utilizzare soluzioni di anestetico locale più concentrate (ad esempio trimecaina 2-2,5% ). Il ripristino della sensibilità avviene nell'ordine inverso, cioè compaiono prima il tono muscolare e le sensazioni propriocettive, quindi le sensazioni di dolore e temperatura. L'effetto dell'anestesia dipende dalla quantità di anestetico che penetra per via transperineurale e provoca un adeguato blocco della soglia. Il raddoppio della concentrazione dell'anestetico iniettato prolunga l'anestesia di 1/3 e l'introduzione di un doppio volume - solo del 3-9%. Gli anestetici locali spesso portano a reazioni anafilattiche. Trimecaina: la durata d'azione è di 1-1,5 ore, la dose singola massima è di 800-1000 mg. La lidocaina (xicaina) viene utilizzata in una soluzione all'1-2%, la durata dell'anestesia è fino a 2,5-3 ore La bupivocaina (marcaina) viene utilizzata in una soluzione allo 0,5-0,75% in una dose singola massima di 150-170 mg , la durata dell'azione è di 8-12 ore Per l'uso di anestetici a lunga durata d'azione, l'aggiunta di lidocaina accelera chiaramente l'inizio dell'effetto, riducendo il periodo di latenza. 47. Anestesia del plesso cervicale (ASP) L'ACS, eseguita su uno o entrambi i lati, consente di eseguire tutti gli interventi su collo, tiroide, vasi brachiocefalici in caso di ferite da arma da fuoco, lesioni e malattie tumorali. Il plesso cervicale (us cervicalis) è formato dai rami anteriori dei quattro nervi cervicali superiori (C1-C4) che emergono dai forami intervertebrali. Si trova sulla superficie anteriore del muscolo scaleno medio e del muscolo che solleva la scapola, lateralmente ai processi trasversali delle vertebre cervicali. I nervi motori del plesso cervicale innervano i muscoli del collo e i nervi sensoriali innervano la pelle della regione occipitale della testa, le superfici anteriore e laterale del collo, la regione succlavia a livello di I e II costole e il padiglione auricolare. Il nervo più grande del plesso cervicale è il frenico (p. prenicus), che è formato da C3-C4 e meno spesso a causa di un ramo aggiuntivo da C5. La maggior parte dei nervi sensoriali esce nel mezzo da sotto il bordo posteriore del muscolo sternocleidomastoideo e diverge negli strati superficiali del collo, nella pelle della regione occipitale della testa e nella parte superiore del torace. Tecnica di anestesia 2 cm sotto l'angolo della mascella inferiore, anteriormente al muscolo sternocleidomastoideo, viene determinata la pulsazione dell'arteria carotide interna. Il ramo orizzontale dell'osso ioide corrisponde al livello del processo trasversale della vertebra C3. Il punto di iniezione dell'ago si trova all'intersezione della linea, che è una continuazione del ramo orizzontale dell'osso ioide, con il bordo anteriore del muscolo sternocleidomastoideo. A questo punto di intersezione, in condizioni asettiche, si forma una "buccia di limone" attraverso la quale viene diretto un ago per iniezione dall'esterno verso l'interno e dalla parte anteriore a quella posteriore, facendolo avanzare medialmente al muscolo sternocleidomastoideo e dietro la carotide interna arteria (nello spazio tra il muscolo sternocleidomastoideo e l'arteria carotide interna palpabile) fino a quando il paziente non sviluppa parestesie o l'ago colpisce il processo trasversale della vertebra C3. La profondità dell'iniezione non supera i 2-5 cm L'ago è fissato saldamente in questa posizione e viene eseguito un test di aspirazione, determinando se l'estremità dell'ago si trova nel lume della nave. Per l'anestesia, vengono iniettati 10-12 ml di una soluzione di trimecaina al 2% da entrambi i lati. Per migliorare l'anestesia del plesso cervicale, puoi inoltre bloccare i rami superficiali che vanno alla superficie anteriore del collo. Il luogo della loro uscita è al centro del bordo posteriore del muscolo sternocleidomastoideo. L'ago viene iniettato nel punto della loro uscita sotto la fascia superficiale del collo. Una soluzione al 2% di trimecaina viene somministrata in una quantità di 3-5 ml cranialmente e caudalmente (a forma di ventaglio). Un'adeguata anestesia si verifica dopo 8-12 minuti e fornisce un efficace sollievo dal dolore nella maggior parte dei pazienti entro 1,5-2 ore. 48. Anestesia del plesso brachiale (APS) L'APS consente di eseguire tutti gli interventi sull'arto superiore, sull'articolazione della spalla, sulla spalla, sull'avambraccio e sulla mano: amputazioni, trattamento chirurgico delle ferite con riposizionamento e fissazione di frammenti ossei, interventi sui vasi sanguigni e sui nervi, riduzione della lussazione della spalla, ecc. Un'elevata frequenza di interventi chirurgici sull'arto superiore, soprattutto in tempo di guerra, solleva la questione di metodi razionali di anestesia durante queste operazioni. Anestesia del plesso brachiale di Winnie Il paziente giace supino, la testa è girata nella direzione opposta rispetto al sito di puntura, il mento è portato al cingolo scapolare controlaterale. La mano dal lato della puntura giace lungo il corpo, leggermente abbassata. Punti di riferimento: muscolo sternocleidomastoideo, scaleno anteriore, spazio interstiziale, vena giugulare esterna, clavicola, cartilagine cricoidea. Tecnica dell'anestesia. La pelle viene trattata con una soluzione antisettica. Posteriormente al muscolo sternocleidomastoideo, che contorna nettamente con una leggera elevazione della testa, a livello della cartilagine cricoide, posizionare i polpastrelli della mano sinistra sul muscolo scaleno anteriore. Con un ulteriore spostamento laterale delle dita di 0,5-1,5 cm, si avverte lo spazio interscaleno tra i muscoli scaleni anteriore e medio. Diventa più pronunciato con un respiro profondo, quando i muscoli scaleni si contraggono. Nelle profondità dello spazio interscaleno si avvertono i processi trasversali delle vertebre cervicali (una sensazione di solida resistenza) e con una maggiore pressione con la punta del dito si verifica spesso parestesia nella spalla o nel cingolo scapolare; caudalmente nello spazio interscaleno si può palpare l'arteria succlavia. Lo spazio interscaleno nella sezione superiore è attraversato dalla vena giugulare esterna. Il punto di inserimento dell'ago si trova nella parte superiore dello spazio interscalenico a livello della cartilagine cricoide. A questo punto si forma una “buccia di limone” e attraverso di essa l'ago viene diretto medialmente e leggermente verso il basso, dalla parte anteriore a quella posteriore (dorsalmente) fino al processo trasverso di C6 con un angolo di 30 rispetto al piano sagittale. Quando l'ago si sposta verso l'interno ad una distanza di 1,5-4 cm, si verifica la parestesia e la punta dell'ago poggia sul processo trasversale della sesta vertebra cervicale. In questa posizione l'ago viene fissato o tirato verso l'alto di 6-1 mm e, dopo una prova di aspirazione, vengono prelevati 2-30 ml di una soluzione di trimecaina al 40% (lidocaina) o di bupivocaina allo 2-0,5% (marcaina). iniettato. Durante l'iniezione dei primi millilitri di soluzione anestetica locale, il paziente avverte un dolore a breve termine (“shock elettrico”), indice del corretto posizionamento della punta dell'ago. In assenza di parestesia, è possibile controllare la posizione della punta dell'ago iniettando 0,75 ml di soluzione di cloruro di sodio allo 0,5% prelevata dal frigorifero. La comparsa di una sensazione di dolore all'arto superiore indica il contatto della soluzione fredda con il nervo. 49. Anestesia dei nervi periferici nella zona del polso Per le operazioni alla mano, è necessario anestetizzare i nervi ulnare, mediano e radiale. In tutti i casi, l'ago viene iniettato a livello della piega prossimale del polso. Durante l'anestesia, il paziente giace sulla schiena, nell'area del polso, il braccio è supinato e leggermente piegato. Punti di riferimento: stiloide dell'ulna, tendine pisiforme, flessore del carpo ulnare e tendine flessore del carpo lungo. Anestesia del nervo ulnare Tecnica per l'anestesia del ramo palmare del nervo ulnare. Il punto di inserimento dell'ago è a livello della piega carpale prossimale, medialmente al tendine flessore ulnare del carpo. L'ago viene inserito ad una profondità di 1-2 cm attraverso il tessuto sottocutaneo verso l'osso pisiforme. Dopo la comparsa della parestesia e se il test di aspirazione è negativo, fissare l'ago e iniettare 3-5 ml di una soluzione di trimecaina al 2%. In assenza di parestesie, l'ago viene fatto avanzare fino al contatto con l'osso e quando viene rimosso si effettua l'infiltrazione tissutale con una soluzione di trimecaina al 2%. Tecnica per l'anestesia del ramo dorsale del nervo ulnare. Il punto di iniezione dell'ago è a livello dell'intersezione della piega prossimale del polso con il bordo mediale del tendine del muscolo flessore ulnare della mano. L'ago è diretto al processo stiloideo dell'ulna. Per ottenere la parestesia, vengono iniettati 3-5 ml di una soluzione al 2% di trimecaina. In assenza di parestesia, l'ago viene rimosso e 5-10 ml di una soluzione di trimecaina al 2% vengono infiltrati nei tessuti. anestesia del nervo mediano Tecnica di anestesia. Il punto di iniezione dell'ago si trova sulla linea della piega cutanea prossimale del polso tra il tendine del muscolo palmare lungo e il flessore radiale della mano. Dopo l'avanzamento perpendicolare dell'ago attraverso il tessuto sottocutaneo fino a una profondità di 0,5-1 cm e ottenuto la parestesia, l'ago viene fissato e vengono iniettati 3-5 ml di una soluzione di lidocaina al 2%. Se non è possibile ottenere una parestesia a una profondità di 1 cm, i tessuti vengono infiltrati a forma di ventaglio con 5-10 ml di una soluzione di trimecaina al 2% estraendo lentamente l'ago. Anestesia del nervo radiale Tecnica di anestesia. Il punto di iniezione è a livello della piega cutanea prossimale del polso lateralmente all'arteria radiale sulla sporgenza della sommità della "tabacchiera anatomica" Si effettua un'iniezione e l'ago viene diretto verso la "tabacchiera anatomica". ". Quando si verifica la parestesia, l'ago viene fissato, con un test di aspirazione negativo, vengono iniettati 3-5 ml di una soluzione di trimecaina al 2%. In assenza di parestesie, 5-10 ml di una soluzione al 2% di trimecaina vengono iniettati a ventaglio nei tessuti sottostanti, creando un "braccialetto" di infiltrazione lungo 3-3,5 cm dai tendini del corto estensore e del lungo abduttore di il pollice da un lato, al lungo estensore del pollice - con un altro. 50. Anestesia degli arti inferiori Per eseguire interventi chirurgici sull'arto inferiore è necessario anestetizzare tutti e quattro i nervi principali. Tre di loro - il nervo femorale, otturatorio e cutaneo esterno della coscia - provengono dal plesso lombare e il nervo sciatico è formato in parte dal lombare e da tre rami del plesso sacrale. Tecnica di anestesia. La pelle viene trattata con una soluzione disinfettante. Con una soluzione anestetica si forma una "buccia di limone", dopo di che l'ago viene iniettato sotto il legamento inguinale 1-1,5 cm sotto quest'ultimo e 0,5-1 cm lateralmente all'arteria femorale palpata. L'ago viene guidato attraverso il tessuto sottocutaneo un po' in direzione prossimale sotto il legamento inguinale, dove a una profondità di 3-4 cm dopo la puntura della fascia, l'ago si rompe con perdita di resistenza e può verificarsi parestesia, estendendosi alla superficie anteriore della coscia. In questa posizione, l'ago viene fissato con il pollice e l'indice della mano sinistra e il bordo del palmo della mano sinistra viene premuto con forza sui tessuti molli della coscia distalmente all'ago e 35-40 ml di un Viene iniettata una soluzione di trimecaina all'1,5%. La pressione sui tessuti molli dura 1,5-2 minuti. Pertanto, l'anestesia del nervo femorale con il bloccaggio si trasforma in anestesia del plesso lombare, eseguita dall'approccio anteriore. L'azione dell'anestesia dura 2-2,5 ore. L'anestesia del plesso lombare può essere eseguita posteriormente, mentre i nervi femorale (L2-L4) e otturatorio (L2-L3), genitofemorale (L1-L2) e il nervo cutaneo femorale laterale (L2-L3) vengono anestetizzati contemporaneamente. La posizione del paziente durante l'anestesia è su un lato sano con le gambe piegate. Punti di riferimento: processo spinoso della 4a vertebra lombare (linea che collega le creste iliache dietro); 3 cm caudali lungo le creste dei processi spinosi dal processo spinoso della 4a vertebra lombare e 5 cm lateralmente dall'ultimo punto. Tecnica di anestesia. Dal processo spinoso della 4a vertebra lombare in direzione caudale si traccia una linea lunga 3 cm, dall'estremità della quale viene ripristinata lateralmente verso l'alto una perpendicolare lunga 5 cm Il punto terminale della perpendicolare, che giace vicino alla cresta iliaca, è il punto di iniezione dell'ago. Dopo aver creato una "buccia di limone", un ago lungo 12-15 cm viene inserito perpendicolarmente alla pelle fino a quando non entra in contatto con il processo trasversale della 5a vertebra lombare. Cranialmente, scivolando fuori dal processo trasversale della 5a vertebra lombare, l'ago entra nello spessore del muscolo psoas quadrato. Allo stesso tempo, si avverte resistenza all'introduzione di una soluzione al suo interno con una siringa (o si verifica una resistenza elastica con la deformazione della bolla d'aria nella siringa). L'ago viene passato a una profondità in cui si avverte una sensazione di "perdita di resistenza" (o la bolla d'aria non è deformata). Questo test indica che l'ago si trova nella fascia tra lo psoas quadrato e lo psoas major. L'ago viene fissato a questa profondità e vengono iniettati 35-40 ml di una soluzione di trimecaina (lidocaina) all'1,5-2% per ottenere l'anestesia. 51. Anestesia del nervo sciatico Anestesia del nervo sciatico dall'approccio anteriore Tecnica dell'anestesia. Il paziente giace sulla schiena. La spina iliaca antero-superiore ed il punto più sporgente del grande trocantere del femore sono collegati tra loro da una linea retta, e dall'ultimo punto si ripristina una perpendicolare alla superficie anteriore della coscia. La lunghezza della perpendicolare è pari alla distanza tra la spina iliaca antero-superiore e il grande trocantere del femore e l'estremità di questa perpendicolare costituisce il punto di proiezione. Nella posizione fisiologica dell'arto inferiore, dopo aver trattato la pelle con una soluzione disinfettante e creato una “buccia di limone”, si dirige verticalmente verso il basso un ago lungo 12-15 cm fino ad appoggiarlo sul piccolo trocantere del femore. Dopo che l'ago scivola dal piccolo trocantere, senza cambiare la direzione principale, l'ago viene fatto passare ancora più in profondità - 4-5 cm fino a quando si verifica la parestesia. Se non è possibile ottenere la parestesia, l'ago viene riportato nell'osso e, ruotando l'arto verso l'interno di 7-10, l'ago viene fatto avanzare nuovamente fino alla comparsa della parestesia nel paziente. Anestesia del nervo sciatico dall'approccio posteriore Tecnica dell'anestesia. Il paziente giace sul fianco sano, l'arto anestetizzato è piegato alle articolazioni dell'anca e del ginocchio con un angolo di 45-60. Dalla parte più sporgente del grande trocantere del femore si traccia una linea retta fino alla spina iliaca postero-superiore, dal centro della quale si abbassa in direzione caudale una perpendicolare lunga 4-5 cm. come punto di proiezione del nervo sciatico. L'ago viene inserito con un angolo di 90 rispetto al piano frontale del corpo del paziente e fatto avanzare fino al raggiungimento della parestesia o del contatto con l'osso. Se necessario, l'ago viene tirato su e inserito circa 0,5 cm lateralmente o medialmente rispetto all'iniezione iniziale. Ottenere la parestesia è obbligatorio. Vengono somministrati 20-25 ml di una soluzione al 2% di lidocaina (trimecaina). La tecnica dell'anestesia non cambierà se il paziente giace a pancia in giù. Anestesia nella fossa poplitea Tecnica di anestesia. L'angolo superiore della fossa romboidale è a livello del bordo superiore della rotula. Il punto di iniezione si trova 1-1,5 cm sotto l'angolo superiore sulla bisettrice abbassata da questo angolo, formata dall'esterno dal tendine del bicipite femorale, dall'interno dai tendini dei muscoli semimembranoso e semitendinoso della coscia. La direzione del movimento dell'ago è rigorosamente verticale con il paziente in posizione prona fino a quando non si ottiene la parestesia del nervo tibiale. In assenza di parestesia, l'ago viene diretto a forma di ventaglio, tirandolo ogni volta verso l'alto fino al livello del tessuto sottocutaneo. Dopo un test di aspirazione, vengono iniettati 5-10 ml di una soluzione al 2% di trimecaina. Per bloccare il nervo peroneo comune dallo stesso punto, l'ago viene diretto lateralmente con un angolo di 30-45 rispetto al piano frontale. Dopo aver ricevuto la parestesia, vengono iniettati 5-10 ml di una soluzione al 2% di trimecaina. Non ci sono complicazioni o controindicazioni. 52. Complicanze dell'anestesia regionale Durante l'AR, le complicazioni si verificano abbastanza raramente e possono essere divise in due gruppi. 1. Specifici, che sono più legati agli errori tecnici della metodologia: 1) errata iniezione di anestetico locale nel canale spinale o nello spazio epidurale, per via endovenosa o intra-arteriosa (con anestesia del plesso cervicale, anestesia del plesso lombare con accesso inguinale); 2) puntura di cavità e organi (cavità pleurica, polmone); 3) la formazione di un ematoma con abbandono della puntura e danno a una grande nave; l'ematoma comprime il tessuto circostante o il fascio neurovascolare; 4) ipotensione prolungata e grave che si manifesta con un rapido riassorbimento dell'anestetico locale; 5) trauma al plesso nervoso o al conduttore con l'estremità dell'ago per iniezione durante una manipolazione approssimativa; 6) l'assenza di un effetto analgesico dopo l'anestesia del plesso o della conduzione. 2. Non specifico, manifestato principalmente da reazioni generali e locali del corpo all'azione di un anestetico locale sotto forma di reazioni tossiche e allergiche. Complicanze non specifiche possono svilupparsi a seconda del tempo, della dose e del sito di somministrazione dell'anestetico. In questo caso predominano le lesioni del sistema nervoso centrale o cardiovascolare. Le complicanze da parte del sistema nervoso centrale possono essere lievi (limitate solo all'eccitazione centrale) o gravi, che si manifestano con l'inibizione del sistema nervoso centrale con possibile paralisi totale. La natura delle complicanze non specifiche: 1) un sovradosaggio di anestetico con la somministrazione simultanea di una dose elevata (più di 1 g) di trimecaina o lidocaina per via intraarteriosa o endovenosa; 2) reazioni allergiche all'introduzione di un anestetico locale, caratterizzate da un complesso di sintomi di disturbi del sistema nervoso centrale e cardiovascolare: ansia, alterazione della coscienza, disturbi del linguaggio, contrazioni muscolari, convulsioni, respiro profondo, disturbi del ritmo cardiaco, espansione QR, abbassamento della pressione sanguigna, tachicardia, apnea, asistolia; 3) complicazioni infettive dovute a un'elaborazione di scarsa qualità del campo chirurgico nel sito dell'anestesia; 4) lo sviluppo dell'ipotensione con anestesia del plesso e della conduzione è molto meno comune rispetto all'epidurale e alla colonna vertebrale; 5) con l'introduzione di soluzioni concentrate di anestetici locali in una piccola percentuale di casi, si nota lo sviluppo della bradicardia. 53. Anestesia lombare Blocco secondo Vishnevsky Questo tipo di anestesia si ottiene iniettando un anestetico nel canale spinale. La tecnica della puntura lombare è descritta nella lezione n. 2. La particolarità è che il livello di puntura è più alto (T12-1_1, L1-L2) e dopo aver rimosso il mandrino dall'ago, viene immediatamente iniettato un anestetico. Il volume dell'anestetico è di 3-5 ml. Naropin viene somministrato in una concentrazione dello 0,5%, lidocaina - nel 2%, marcaina - nello 0,5%. La durata dell'anestesia è di 4-6 ore Questo tipo di anestesia provoca anche una grave ipotensione. Ad un livello elevato di anestesia (T12-L1), è possibile l'insufficienza respiratoria. La complicanza più comune è il mal di testa. Blocco vagosimpatico cervicale secondo A. V. Vishnevsky Il paziente viene posizionato sul tavolo sulla schiena in modo che la mano sul lato del blocco proposto penda oltre il bordo del tavolo. Il muscolo sternocleidomastoideo deve essere rilassato. Un rullo è posizionato sotto il cingolo scapolare, la testa è retratta nella direzione opposta; in questa posizione i contorni anatomici del collo sono ben delineati. Il campo viene trattato con lubrificazione con alcool e iodio. Il dottore si trova dalla parte dell'omonimo blocco. Il sito di iniezione è l'angolo formato dall'intersezione del bordo posteriore del muscolo sternocleidomastoideo con una vena. L'indice della mano sinistra è posizionato sul bordo posteriore del muscolo sternocleidomastoideo, sopra il punto in cui si incrocia con la vena giugulare esterna. Premendo con forza un dito su questo punto, cercano di spostare il fascio neurovascolare sulla linea mediana. In questo caso, il dito sente facilmente la superficie anteriore delle vertebre cervicali. L'iniezione dell'ago e il suo avanzamento devono essere eseguiti lentamente, verso l'alto e verso l'interno, concentrandosi sempre sulla superficie anteriore della colonna vertebrale. L'ago si muove lungo la soluzione di novocaina allo 2% inviata in piccole porzioni (3-0,25 cm), il che garantisce la sicurezza dell'iniezione. La siringa durante l'iniezione viene rimossa ripetutamente dall'ago a scopo di controllo. Dopo aver portato l'ago alla vertebra, sentono come si appoggia contro di essa. Quindi la pressione sull'ago si indebolisce, a causa della quale si allontana di 1-2 mm, dopo di che vengono iniettati da 40 a 60 ml di una soluzione che, diffondendosi in un infiltrato strisciante lungo l'aponeurosi prevertebrale, copre il vago, simpatico , e spesso i nervi frenici, interrompendo (bloccando) la trasmissione delle irritazioni dalla regione pleuropolmonare. L'efficacia del blocco vagosimpatico è evidenziata dalla comparsa del sintomo di Horner (restringimento della pupilla, restringimento della fessura palpebrale e retrazione del bulbo oculare). Il ritmo respiratorio e il polso diventano meno frequenti, la mancanza di respiro e la cianosi diminuiscono e le condizioni generali migliorano. Per evitare che l'ago penetri nei vasi del collo, il muscolo sternocleidomastoideo con il fascio neurovascolare sottostante deve essere spostato con sufficiente forza con l'indice sulla linea mediana. È importante dirigere l'ago verso l'alto e verso l'interno, poiché spostarlo in direzione orizzontale minaccia di introdurre una soluzione sotto l'aponeurosi prevertebrale e la successiva complicazione sotto forma di una sindrome del dolore che non si ferma durante il giorno. 54. Valutazione della gravità del paziente Valutazione della condizione somatica del paziente. 1 punto - pazienti la cui malattia è localizzata e, di regola, non causa disturbi sistemici, ad es. persone praticamente sane. 2 punti: questo include pazienti con disturbi inespressi che interrompono moderatamente l'attività vitale del corpo senza cambiamenti pronunciati nell'omeostasi. 3 punti: pazienti con disturbi sistemici vitali che interrompono in modo significativo il funzionamento del corpo, ma non portano a disabilità. 4 punti - pazienti con gravi disturbi sistemici che rappresentano un grave pericolo per la vita umana e portano alla disabilità. 5 punti - pazienti la cui condizione è considerata critica, il rischio di morte entro 24 ore è alto. Il volume e la natura dell'intervento chirurgico: 1 punto - piccole operazioni per: rimozione di tumori localizzati e localizzati superficialmente, apertura di piccoli ascessi, amputazione delle dita delle mani e dei piedi, legatura e rimozione di emorroidi, appendicectomia semplice ed erniotomia. 2 punti - operazioni di moderata gravità: rimozione di tumori maligni localizzati superficialmente che richiedono un intervento esteso; apertura di ascessi localizzati in cavità; amputazione e disarticolazione degli arti superiori e inferiori; operazioni su navi periferiche; appendicectomia complicata ed erniotomia che richiedono un ampio intervento; toracotomia e laparotomia di prova; altri simili per complessità e portata di intervento. 3 punti - interventi chirurgici estesi: operazioni radicali sugli organi addominali (tranne quelli sopra elencati); operazioni radicali sugli organi della cavità toracica. amputazioni estese degli arti, come l'amputazione transiliosacrale; neurochirurgia. 4 punti: operazioni sul cuore, vasi di grandi dimensioni e altri interventi complessi eseguiti in condizioni speciali (circolazione artificiale, ipotermia, ecc.). Classificazione dello stato oggettivo del paziente, sviluppata dall'American Society of Anesthesiologists (ASA). 1. Non ci sono disturbi sistemici. 2. Disturbi sistemici lievi senza compromissione funzionale. 3. Malattie sistemiche moderate e gravi con disfunzione. 4. Grave malattia sistemica che rappresenta costantemente una minaccia per la vita e porta al fallimento delle funzioni. 5. Stato terminale, alto rischio di morte durante il giorno, indipendentemente dall'operazione. 6. Morte cerebrale, donazione di organi per trapianto. 55. Ventilazione polmonare artificiale La ventilazione polmonare artificiale (ALV) fornisce lo scambio di gas tra l'aria circostante (o una certa miscela di gas) e gli alveoli dei polmoni, viene utilizzata come mezzo di rianimazione in caso di interruzione improvvisa della respirazione, come componente dell'anestesia e come mezzo di terapia intensiva per l'insufficienza respiratoria acuta, nonché alcune malattie del sistema nervoso e muscolare. I moderni metodi di ventilazione polmonare artificiale (ALV) possono essere suddivisi in semplici e hardware. Un metodo semplice di ventilazione meccanica viene solitamente utilizzato in situazioni di emergenza (apnea, ritmo patologico, respirazione agonale, aumento dell'ipossiemia e (o) ipercapnia e disturbi metabolici evidenti). I più semplici sono i metodi espiratori di ventilazione meccanica (respirazione artificiale) da bocca a bocca e da bocca a naso. I metodi hardware vengono utilizzati quando è necessaria una ventilazione meccanica a lungo termine (da un'ora a diversi mesi e persino anni). Il respiratore Phase-50 ha grandi capacità. Il dispositivo Vita-1 è prodotto per la pratica pediatrica. Il respiratore è collegato alle vie respiratorie del paziente tramite un tubo endotracheale o una cannula tracheostomica. La ventilazione dell'hardware viene eseguita in modalità di frequenza normale, che varia da 12 a 20 cicli al minuto. In pratica, esistono ventilazioni ad alta frequenza (più di 1 cicli al minuto), in cui il volume corrente è significativamente ridotto (fino a 60 ml o meno), la pressione positiva nei polmoni alla fine dell'inspirazione è ridotta, così come la ventilazione intratoracica. pressione e il flusso sanguigno al cuore migliora. Inoltre, con la modalità ad alta frequenza, viene facilitato l’adattamento (adattamento) del paziente al respiratore. Esistono tre metodi di ventilazione ad alta frequenza: volumetrica, oscillatoria e a getto. Il volume viene solitamente eseguito con una frequenza respiratoria di 80-100 per 1 minuto, IVL oscillatorio - 600-3600 per 1 minuto, che garantisce la vibrazione di un flusso di gas continuo o intermittente. La ventilazione a getto ad alta frequenza più diffusa con una frequenza respiratoria di 100-300 al minuto, in cui un getto di ossigeno a una pressione di 1-2 atm viene soffiato nelle vie aeree attraverso un ago o un catetere con un diametro di 2-4 mm. Viene effettuata anche la ventilazione ausiliaria, ma in questo caso viene mantenuta la respirazione spontanea del paziente. Il gas viene erogato dopo che il paziente ha effettuato un debole tentativo di inspirazione oppure il paziente è sincronizzato con una modalità di funzionamento del dispositivo selezionata individualmente. Esiste anche una modalità di ventilazione obbligatoria intermittente (PPVL), che viene utilizzata nel processo di transizione graduale dalla ventilazione artificiale alla respirazione spontanea. In questo caso il paziente respira da solo, ma nelle vie respiratorie viene inoltre immesso un flusso continuo di miscela di gas. In questo contesto, con una frequenza prestabilita (da 10 a 1 volta al minuto), il dispositivo esegue un'inalazione artificiale, coincidente (PPVL sincronizzato) o non coincidente (PPVL non sincronizzato) con l'inalazione spontanea del paziente. Una riduzione graduale dei respiri artificiali prepara il paziente alla respirazione indipendente. 56. Terapia infusionale La terapia infusionale è un'iniezione a goccia o un'infusione endovenosa o sottocutanea di farmaci e fluidi biologici al fine di normalizzare l'equilibrio idroelettrolitico, acido-base del corpo, nonché per la diuresi forzata (in combinazione con diuretici). Indicazioni per la terapia infusionale: tutti i tipi di shock, perdita di sangue, ipovolemia, perdita di liquidi, elettroliti e proteine a seguito di vomito indomabile, diarrea intensa, rifiuto di assumere liquidi, ustioni, malattie renali; violazioni del contenuto di ioni basici (sodio, potassio, cloro, ecc.), acidosi, alcalosi e avvelenamento. Le soluzioni cristalloidi sono in grado di compensare la carenza di acqua ed elettroliti. Applicare una soluzione di cloruro di sodio allo 0,85%, soluzioni di Ringer e Ringer-Locke, una soluzione di cloruro di sodio al 5%, soluzioni di glucosio al 5-40% e altre soluzioni. Vengono somministrati per via endovenosa e sottocutanea, per via orale (con grave disidratazione) e flebo, in un volume di 10-50 ml/kg o più. Gli obiettivi della terapia infusionale sono: ripristino del BCC, eliminazione dell'ipovolemia, garantire un'adeguata gittata cardiaca, mantenere e ripristinare la normale osmolarità plasmatica, garantire un'adeguata microcircolazione, prevenire l'aggregazione dei globuli, normalizzare la funzione di trasporto dell'ossigeno del sangue. Le soluzioni colloidali sono soluzioni di sostanze macromolecolari. Contribuiscono alla ritenzione di liquidi nel letto vascolare. Vengono utilizzati emodez, poliglucina, reopoliglyukin, reogluman. Con la loro introduzione sono possibili complicazioni, che si manifestano sotto forma di reazione allergica o pirogena. Vie di somministrazione: per via endovenosa, meno spesso per via sottocutanea e gocciolante. La dose giornaliera non supera i 30-40 ml/kg. Hanno una qualità disintossicante. Come fonte di nutrizione parenterale, vengono utilizzati in caso di prolungato rifiuto di mangiare o impossibilità di alimentarsi per via orale. I destrani sono sostituti del plasma colloidale, il che li rende altamente efficaci nel rapido recupero del BCC. I destrani hanno specifiche proprietà protettive contro le malattie ischemiche e la riperfusione, il cui rischio è sempre presente durante gli interventi chirurgici maggiori. Il plasma fresco congelato è un prodotto prelevato da un singolo donatore. La FFP viene separata dal sangue intero e congelata immediatamente entro 6 ore dalla raccolta del sangue. Conservato a 30°C in sacchetti di plastica per 1 anno. Data la labilità dei fattori della coagulazione, la FFP deve essere trasfusa entro le prime 2 ore dopo lo sbrinamento rapido a 37°C. La trasfusione di plasma fresco congelato (FFP) presenta un rischio elevato di contrarre infezioni pericolose come HIV, epatite B e C, ecc. La frequenza delle reazioni anafilattiche e pirogene durante la trasfusione di FFP è molto alta, quindi deve essere presa in considerazione la compatibilità secondo il sistema ABO. E per le giovani donne è necessario tenere conto della compatibilità Rh. Autore: Kolesnikova MA
▪ Chirurgia dei bambini. Culla
Pelle artificiale per l'emulazione del tocco
15.04.2024 Lettiera per gatti Petgugu Global
15.04.2024 L'attrattiva degli uomini premurosi
14.04.2024
▪ Un buco nero non può diventare più pesante di 50 miliardi di soli ▪ Le bustine di tè sono pericolose per l'uomo ▪ Pneumatico per bicicletta Metl ▪ Custodie con sensore di impronte digitali per dispositivi Android ▪ È ora di porre fine alla rivolta con la benzina
▪ sezione Firmware del sito. Selezione dell'articolo ▪ articolo Immunologia generale e clinica. Culla ▪ articolo Cosa rende il cibo buono? Risposta dettagliata ▪ articolo Otto scorrevole. Suggerimenti turistici ▪ articolo Caricatore antico. Enciclopedia dell'elettronica radio e dell'ingegneria elettrica
Homepage | Biblioteca | Articoli | Mappa del sito | Recensioni del sito www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese

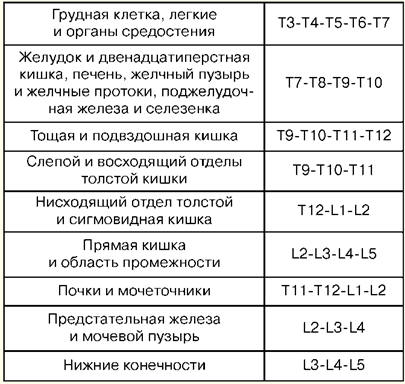


 Vedi altri articoli sezione
Vedi altri articoli sezione 