
|
|
STORIA DELLA TECNOLOGIA, DELLA TECNOLOGIA, DEGLI OGGETTI INTORNO A NOI
Dinamite. Storia dell'invenzione e della produzione
Elenco / La storia della tecnologia, della tecnologia, degli oggetti che ci circondano La dinamite è una miscela esplosiva, assorbente (ad esempio farina fossile), impregnata di nitroglicerina. Può contenere anche altri componenti (salnitro, ecc.). L'intera massa viene solitamente compressa in una forma cilindrica e posta in imballaggi di carta o plastica. La carica viene fatta esplodere utilizzando una capsula detonatrice. La dinamite fu brevettata da Alfred Nobel il 25 novembre 1867.
Per diversi secoli, la gente conosceva un solo esplosivo: la polvere nera, ampiamente utilizzata sia in guerra che in esplosioni pacifiche. Ma la seconda metà del XIX secolo fu segnata dall'invenzione di un'intera famiglia di nuovi esplosivi, il cui potere distruttivo era centinaia e migliaia di volte maggiore di quello della polvere da sparo. La loro creazione è stata preceduta da numerose scoperte. Già nel 1838 Peluz condusse i primi esperimenti sulla nitrazione di sostanze organiche. L'essenza di questa reazione sta nel fatto che molte sostanze carboniose, se trattate con una miscela di acido nitrico e solforico concentrato, rinunciano al loro idrogeno, prendono in cambio il gruppo nitro NO2 e trasformarsi in potenti esplosivi. Altri chimici hanno studiato questo interessante fenomeno. In particolare, Shenbein, cotone nitrurato, ricevette la pirossilina nel 1846. Nel 1847, agendo in modo simile sulla glicerina, Sobrero scoprì la nitroglicerina, un esplosivo che aveva un tremendo potere distruttivo. All'inizio, la nitroglicerina non interessava a nessuno. Lo stesso Sobrero tornò ai suoi esperimenti solo 13 anni dopo e descrisse l'esatto metodo di nitrazione del glicerolo. Successivamente, la nuova sostanza ha trovato impiego nell'industria mineraria. Inizialmente veniva versato nel pozzo, tappato con argilla e sabbiato per mezzo di una cartuccia immersa in esso. Tuttavia, l'effetto migliore è stato ottenuto accendendo un cappuccio a percussione con fulminato di mercurio. Cosa spiega l'eccezionale potere esplosivo della nitroglicerina? Si è scoperto che durante l'esplosione si decompone, a seguito della quale si formano per la prima volta gas CO2, CO, H2, CH4, N2 e NO, che interagiscono ancora tra loro rilasciando un'enorme quantità di calore. La reazione finale può essere espressa dalla formula: 2C3H5(N3)3 = 6CO2 + 5H2O+3N+0,5O2. Riscaldati a una temperatura enorme, questi gas si espandono rapidamente, esercitando un'enorme pressione sull'ambiente. I prodotti finali dell'esplosione sono completamente innocui. Tutto ciò sembrava rendere la nitroglicerina indispensabile per le esplosioni sotterranee, ma presto si è scoperto che la produzione, lo stoccaggio e il trasporto di questo esplosivo liquido erano carichi di molti pericoli. In generale, la nitroglicerina pura è abbastanza difficile da accendere da una fiamma libera. Un fiammifero acceso marciva senza conseguenze. Ma d'altra parte, la sua sensibilità agli urti e alle commozioni cerebrali (detonazione) era molte volte superiore a quella della polvere nera. All'impatto, spesso del tutto insignificante, negli strati soggetti a scuotimento si è verificato un rapido aumento della temperatura fino all'inizio della reazione esplosiva. La mini-esplosione dei primi strati ha prodotto un nuovo impatto sugli strati più profondi, e questo è continuato fino a quando si è verificata l'esplosione dell'intera massa di materia. A volte, senza alcuna influenza esterna, la nitroglicerina iniziava improvvisamente a decomporsi in acidi organici, si scuriva rapidamente, e quindi bastava il più insignificante scuotimento della bottiglia per provocare una terribile esplosione. Dopo una serie di incidenti, l'uso della nitroglicerina è stato quasi universalmente vietato. Agli industriali che hanno avviato la produzione di questo esplosivo erano rimaste due opzioni: trovare una condizione in cui la nitroglicerina fosse meno sensibile alla detonazione o ridurre la loro produzione. Uno dei primi ad interessarsi alla nitroglicerina fu l'ingegnere svedese Alfred Nobel, che fondò uno stabilimento per la sua produzione. Nel 1864 la sua fabbrica decolla con gli operai. Cinque persone sono morte, incluso il fratello di Alfred, Emil, che aveva appena 20 anni. Dopo questo disastro, Nobel è stato minacciato di perdite significative: non è stato facile convincere le persone a investire in un'impresa così pericolosa. Per diversi anni ha studiato le proprietà della nitroglicerina e alla fine è riuscito a stabilirne una produzione completamente sicura. Ma il problema del trasporto è rimasto. Dopo molti esperimenti, Nobel ha scoperto che la nitroglicerina disciolta nell'alcol è meno sensibile alla detonazione. Tuttavia, questo metodo non ha fornito una completa affidabilità. La ricerca è continuata e poi un incidente inaspettato ha contribuito a risolvere brillantemente il problema. Durante il trasporto delle bottiglie di nitroglicerina, per ammorbidire lo scuotimento, venivano poste in farina fossile, una speciale farina fossile estratta ad Hannover. Kieselguhr consisteva in gusci di selce di alghe con molte cavità e tubuli. E una volta, durante la spedizione, una bottiglia di nitroglicerina si è rotta e il suo contenuto si è rovesciato a terra. Nobel ebbe l'idea di fare degli esperimenti con questa farina fossile impregnata di nitroglicerina. Si è scoperto che le proprietà esplosive della nitroglicerina non sono diminuite affatto dal fatto che è stata assorbita dalla terra porosa, ma la sua sensibilità alla detonazione è diminuita più volte. In questo stato, non è esploso né per attrito, né per un debole colpo, né per bruciatura. Ma d'altra parte, quando una piccola quantità di fulminato di mercurio è stata accesa in una capsula metallica, si è verificata un'esplosione della stessa forza che ha dato nitroglicerina pura nello stesso volume. In altre parole, era esattamente ciò di cui aveva bisogno, e anche molto di più di ciò che Nobel sperava di ottenere. Nel 1867 ottenne un brevetto per un composto che scoprì, che chiamò dinamite. La potenza esplosiva della dinamite è enorme quanto quella della nitroglicerina: 1 kg di dinamite in 1/50000 di secondo sviluppa una forza di 1000000 di kgm, cioè sufficiente per sollevare 1000000 di kg per 1 m. in gas per 1 secondi, quindi 0 kg di dinamite in 01 secondi. Ma con tutto questo, la dinamite ben fatta è esplosa solo per un colpo molto forte. Acceso dal tocco del fuoco, bruciò gradualmente senza esplosioni, con una fiamma bluastra. L'esplosione è avvenuta solo quando è stata accesa una grande massa di dinamite (più di 1 kg). È stato meglio minare la dinamite, come la nitroglicerina, usando la detonazione. A tale scopo, Nobel nello stesso anno 1867 inventò un detonatore di innesco rumoroso. Dynamite trovò subito la più ampia applicazione nella costruzione di autostrade, gallerie, canali, ferrovie e altri oggetti, che predeterminarono in gran parte la rapida crescita della fortuna del suo inventore. Nobel fondò la prima fabbrica per la produzione di dinamite in Francia, poi ne avviò la produzione in Germania e Inghilterra. Per trent'anni, il commercio della dinamite ha portato a Nobel un'enorme ricchezza: circa 35 milioni di corone.
Il processo di produzione della dinamite è stato ridotto a diverse operazioni. Prima di tutto, era necessario ottenere la nitroglicerina. Questo è stato il momento più difficile e pericoloso dell'intera produzione. La reazione di nitrazione si è verificata quando 1 parte di glicerolo è stata trattata con 6 parti di acido nitrico concentrato in presenza di XNUMX parti di acido solforico concentrato. L'equazione era simile a questa: C3H5(OH)3 + 3 HNO3 = C3H5(NO3)3 + 3H2O. L'acido solforico non partecipava al composto, ma la sua presenza era necessaria, in primo luogo, per assorbire l'acqua rilasciata a seguito della reazione, che altrimenti, diluendo l'acido nitrico, impedirebbe così la completezza della reazione, e, in secondo luogo, per isolare la nitroglicerina risultante da una soluzione in acido nitrico, poiché, essendo altamente solubile in questo acido, non si scioglieva nella sua miscela con acido solforico. La nitrazione è stata accompagnata da un forte rilascio di calore. Inoltre, se, a causa del riscaldamento, la temperatura della miscela supera i 50 gradi, il corso della reazione andrebbe nella direzione opposta: inizierebbe l'ossidazione della nitroglicerina, accompagnata da un rapido rilascio di ossidi di azoto e da un riscaldamento ancora maggiore , che provocherebbe un'esplosione. Pertanto, la nitrazione doveva essere effettuata con un raffreddamento costante della miscela di acidi e glicerolo, aggiungendo quest'ultimo a poco a poco e mescolando continuamente ogni porzione. La nitroglicerina formata direttamente a contatto con gli acidi, avente una densità inferiore rispetto alla miscela acida, galleggiava in superficie e poteva essere facilmente raccolta dopo che la reazione era stata completata. La preparazione della miscela acida presso le fabbriche Nobel avveniva in grandi recipienti cilindrici di ghisa, da dove la miscela entrava nel cosiddetto apparato di nitrazione.
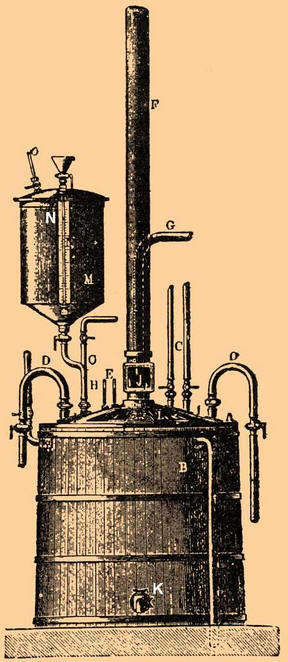
L'apparecchio era costituito da un recipiente di piombo A, che veniva posto in una vasca di legno B e chiuso con un coperchio di piombo L, che veniva imbrattato di cemento durante il funzionamento. Le estremità di due bobine di piombo D, situate all'interno dell'apparecchio, passavano attraverso il coperchio (l'acqua fredda veniva costantemente fornita attraverso di esse). Aria fredda è stata anche fornita all'apparecchio attraverso il tubo C per agitare la miscela. Il tubo F rimuoveva i vapori di acido nitrico dall'apparecchio; il tubo G è servito per versare una quantità misurata della miscela acida; il glicerolo è stato versato attraverso la provetta H. Nel recipiente M è stata misurata la quantità richiesta di tale sostanza, che è stata poi iniettata nella miscela di azoto mediante aria compressa immessa attraverso il tubo O. In un tale impianto si potevano lavorare circa 150 kg di glicerolo alla volta. Dopo aver fatto entrare la quantità richiesta della miscela acida e averla raffreddata (facendo passare aria compressa fredda e acqua fredda attraverso le bobine) a 15-20 gradi, hanno iniziato a spruzzare la glicerina raffreddata. Allo stesso tempo, si sono assicurati che la temperatura nell'apparato non superasse i 30 gradi. Se la temperatura della miscela iniziasse a salire rapidamente e si avvicinasse al livello critico, il contenuto della vasca potrebbe essere rapidamente rilasciato in un grande recipiente di acqua fredda. L'operazione di formazione della nitroglicerina è durata circa un'ora e mezza. Successivamente, la miscela è entrata nel separatore - una scatola rettangolare di piombo con fondo conico e due rubinetti, uno dei quali si trovava sul fondo e l'altro - sul lato. Una volta che la miscela si è stabilizzata e separata, la nitroglicerina è stata rilasciata attraverso il rubinetto superiore e la miscela acida attraverso il fondo. La nitroglicerina risultante è stata lavata più volte per rimuovere gli acidi in eccesso, poiché l'acido potrebbe reagire con essa e provocarne la decomposizione, che inevitabilmente portava a un'esplosione. Per evitare ciò, nella vasca ermetica è stata alimentata acqua con nitroglicerina e la miscela è stata miscelata con aria compressa. L'acido si dissolse nell'acqua, e poiché le densità dell'acqua e della nitroglicerina differivano molto, non era difficile separarle l'una dall'altra. Per rimuovere l'acqua residua, la nitroglicerina è stata fatta passare attraverso diversi strati di feltro e sale da cucina. Come risultato di tutte queste azioni si otteneva un liquido oleoso giallastro, inodore e molto velenoso (l'avvelenamento poteva avvenire sia per inalazione di vapori che per contatto di gocce di nitroglicerina sulla pelle). Quando riscaldato oltre i 180 gradi, esplose con una terribile forza distruttiva. La nitroglicerina preparata è stata miscelata con farina fossile. Prima di questo, la farina fossile veniva lavata e accuratamente macinata. L'impregnazione con nitroglicerina avveniva in cassette di legno rivestite di piombo all'interno. Dopo aver mescolato con nitroglicerina, la dinamite è stata strofinata attraverso un setaccio e inserita in cartucce di pergamena. Nella dinamite kieselguhr, solo la nitroglicerina è stata coinvolta nella reazione esplosiva. Successivamente, Nobel ha avuto l'idea di impregnare vari tipi di polvere da sparo con nitroglicerina. In questo caso, anche la polvere da sparo ha partecipato alla reazione e ha aumentato significativamente la forza dell'esplosione. Autore: Ryzhov KV
▪ carta
L’esistenza di una regola entropica per l’entanglement quantistico è stata dimostrata
09.05.2024 Mini condizionatore Sony Reon Pocket 5
09.05.2024 Energia dallo spazio per Starship
08.05.2024
▪ Il serpente più grande e più piccolo ▪ Genius Cam Mouse con fotocamera integrata ▪ Lettore PocketBook 640 resistente all'umidità e alla polvere ▪ Anche gli insetti invecchiano
▪ sezione del sito amplificatori di potenza RF. Selezione dell'articolo ▪ articolo Storia della cultura. Note di lettura ▪ articolo Chi nacque dall'Immacolata Concezione? Risposta dettagliata ▪ Articolo di Kanufer. Leggende, coltivazione, metodi di applicazione
Homepage | Biblioteca | Articoli | Mappa del sito | Recensioni del sito www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese



 Vedi altri articoli sezione
Vedi altri articoli sezione 