
|
|
ENCICLOPEDIA DELLA RADIOELETTRONICA ED ELETTRICA Caratteristiche comparative degli elementi galvanici di taglia AA. Enciclopedia dell'elettronica radio e dell'ingegneria elettrica
Enciclopedia della radioelettronica e dell'elettrotecnica / Caricabatterie, batterie, celle galvaniche Oggi nei negozi e nei mercati puoi trovare molte diverse celle galvaniche. Quali scegliere? Questo articolo ti aiuterà a prendere la decisione giusta. Le celle e le batterie galvaniche sono ampiamente utilizzate per alimentare varie apparecchiature elettroniche. Gli elementi di dimensione AA sono i più utilizzati. Sugli scaffali puoi trovare prodotti simili di diverse aziende, principalmente due sistemi elettrochimici: salino e alcalino. Più recentemente, Energizer ha lanciato batterie al litio AA da 1,5 V. La caratteristica più importante di una cella galvanica - la capacità (la quantità di energia elettrica che è in grado di cedere al carico) - non è quasi mai indicata in etichetta. L'acquirente è lasciato a concentrarsi sugli spot televisivi sulle celle che "funzionano fino a dieci volte più a lungo del sale convenzionale", o prendere la parola di Energizer, che afferma che le sue nuove celle AA al litio e2 durano cinque volte di più rispetto a quelle alcaline convenzionali [1 ]. Inoltre, non è del tutto chiaro quali elementi siano chiamati "ordinari". Per confrontare quantitativamente i parametri di elementi di diversi sistemi elettrochimici, è necessario testarli nelle stesse condizioni. Tali test sono stati effettuati con tre tipi di celle: sale Philips Long Life (emf di una cella "fresca" - 1,65 V), alcalina Duracell Ultra M1,62 (2 V) e litio Energizer e1,8 (15 V). Ciascuno di essi è stato caricato con un resistore da 100 ohm, che corrisponde a una corrente di scarica iniziale di circa 1 mA. Per elementi di dimensioni AA, tale corrente di carico è tipica. Lo scarico è stato effettuato in cicli di diverse ore al giorno, che corrispondono alle reali condizioni operative. Questo spiega i picchi di tensione nelle curve di scarica mostrate nelle Figg. XNUMX. La curva in blu corrisponde all'elemento sale, rosso - alcalino e verde - litio. Durante il "riposo" la tensione sull'elemento di qualsiasi tipo è leggermente aumentata, ma dopo che il carico è stato collegato, è rapidamente diminuita al minimo nel ciclo precedente. I punti segnano i valori dell'EMF degli elementi: le tensioni su di essi senza carico.
Se prendiamo come criterio per la scarica completa della cella una diminuzione della tensione al suo carico a 0,9 V, la capacità sperimentalmente determinata della cella salina era 1 Ah, la cella alcalina era 2,9 Ah e la cella litio era 3,5 Ah. Di conseguenza, non è necessario parlare di differenze di cinque o dieci volte nella capacità degli elementi di diversi sistemi elettrochimici. Sulla fig. 2 mostra un'altra serie di curve.
Mostrano come è cambiata la resistenza interna degli elementi durante il processo di scarica. La corrispondenza tra tipo di elemento e colore della curva è la stessa di Fig. 1. I valori della resistenza interna R, sono stati calcolati con la formula
dove E è l'EMF dell'elemento; U - tensione sotto carico; RH è la resistenza di carico. La resistenza interna degli elementi salini e alcalini aumenta monotona man mano che vengono scaricati. E la resistenza del litio, essendo diminuita drasticamente all'inizio della scarica, rimane praticamente invariata fino alla fine, per poi aumentare altrettanto bruscamente. Naturalmente, gli esperimenti effettuati non possono essere definiti esaustivi. La capacità di un elemento non è un valore strettamente fisso, dipende da molti fattori esterni. Per diversi elementi, il suo massimo può essere raggiunto in condizioni di scarica significativamente diverse. Per tenere conto di tutto ciò, bisognerebbe condurre una serie molto ampia di esperimenti, irrealistici in condizioni amatoriali. Tuttavia, proviamo a verificare i risultati ottenuti mediante calcolo. Per stimare teoricamente la capacità massima possibile degli elementi di vari sistemi elettrochimici, è necessario conoscere la composizione chimica dei loro elettrodi, elettroliti e la reazione chimica che avviene nell'elemento. Nelle celle saline e alcaline, il catodo è zinco e l'anodo è biossido di manganese. È per questo motivo che tali elementi sono chiamati collettivamente manganese-zinco. Ma l'elettrolita in essi contenuto è diverso: sale (solitamente cloruro di ammonio) o alcali (idrossido di potassio). Secondo [2], la reazione avviene in un elemento sale manganese-zinco
e in alcalino
Non ci sono informazioni affidabili sul materiale degli elettrodi e sulla reazione chimica nella cella al litio. Possiamo solo supporre che gli elettrodi siano litio e biossido di manganese e che l'elettrolita sia una soluzione di perclorato di litio in carbonato di propilene. Se questa congettura è corretta, secondo [2], la cella al litio subisce la reazione
Usando la legge di Faraday, otteniamo un'espressione per determinare la capacità di una cella galvanica C, Ah:
dove m è la massa delle sostanze reagenti F = 96,5-103 C/g-eq è il numero di Faraday; n - valenza (per celle galvaniche saline e alcaline - 2, per litio - 1); M è il peso molecolare totale dei reagenti. Pesiamo celle galvaniche di dimensioni AA: sale - 17 g, alcalino - 24 g, litio - 15 g. ) è trascurabile e può essere trascurato. Calcoliamo il peso molecolare totale delle sostanze reagenti dalle precedenti equazioni delle reazioni chimiche: per sale - 346 g, per alcalino - 257 g, per litio - 94 g Sostituendo i valori numerici nella formula, otteniamo il capacità massima possibile dell'elemento salino - 2,6 Ah , alcalino - 5 Ah, litio - 4,3 Ah. Le differenze tra i valori di capacità calcolati e quelli misurati possono essere spiegate da ipotesi piuttosto approssimative fatte nel calcolo. Quindi non sono state trovate differenze di cinque e dieci volte. La capacità teorica di una cella alcalina è circa il doppio di quella di una cella salina e il litio non ha alcun vantaggio rispetto a quello alcalino a questo riguardo. Ciò è coerente con i risultati sperimentali. Sulla base dei risultati di tutto il lavoro svolto, possiamo concludere quanto segue: 1. Le celle galvaniche al litio hanno la tensione più stabile, la resistenza interna più bassa, che praticamente non dipende dal grado di scarica, e la capacità più grande, anche se non molto. È preferibile utilizzarli per alimentare apparecchiature con un elevato consumo di corrente, nonché in dispositivi che si spengono automaticamente quando la tensione di alimentazione diminuisce (ad esempio fotocamere digitali). 2. Le celle alcaline hanno una capacità paragonabile a quella del litio, e sono anche in grado di erogare una corrente elevata al carico, ma a una tensione inferiore. Sono utilizzati al meglio in dispositivi con un consumo di corrente medio senza controllo automatico della tensione. In molti casi, le celle alcaline sono preferite al litio perché sono da tre a quattro volte più economiche. 3. Le celle saline hanno la più piccola capacità e la più alta resistenza interna. Si consiglia di utilizzarli in apparecchiature a basso consumo di corrente. Letteratura
Autore: I.Podushkin, Mosca
Un nuovo modo di controllare e manipolare i segnali ottici
05.05.2024 Tastiera Seneca Premium
05.05.2024 Inaugurato l'osservatorio astronomico più alto del mondo
04.05.2024
▪ Il satellite non guidato cade sulla Terra ▪ Sistemi di Videosorveglianza Digitale Trassir ▪ Batteria esterna ZMI 20 Power Bank con caricabatteria da 120W ▪ Dispositivo anti-sonno di Ford
▪ sezione del sito Grande Enciclopedia per bambini e adulti. Selezione dell'articolo ▪ articolo Zelinsky Nikolay. Biografia di uno scienziato ▪ articolo Master della sezione vapore (locale caldaia). Descrizione del lavoro ▪ articolo Indicatore di campo. Enciclopedia dell'elettronica radio e dell'ingegneria elettrica
Commenti sull'articolo: ospite Articolo esplicativo, grazie.
Homepage | Biblioteca | Articoli | Mappa del sito | Recensioni del sito www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






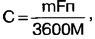
 Lascia il tuo commento su questo articolo:
Lascia il tuo commento su questo articolo: